08/06/2009
Det Europæiske Lægemiddelagentur (EMA) står over for en af de mest turbulente perioder i sin historie. Som en direkte konsekvens af Storbritanniens beslutning om at forlade EU, blev agenturet tvunget til at finde et nyt hjem, en proces der kulminerede i en dramatisk afgørelse. Samtidig med denne enorme logistiske udfordring fortsatte agenturet sit kerne-arbejde med at beskytte og fremme folke- og dyresundheden i hele Europa. EMA's årsrapport for 2017 giver et fascinerende indblik i de resultater og initiativer, der blev opnået i et år præget af usikkerhed og forandring. Denne artikel dykker ned i begge historier: den nervepirrende flytning til Amsterdam og de markante fremskridt, der blev fremhævet i årsrapporten.
En Ny Begyndelse i Amsterdam: EMA's Flytning efter Brexit
Afgørelsen om EMA's nye placering var ikke blot en administrativ formalitet; det var en højspændt politisk proces, der involverede intens lobbyisme og flere måneders forhandlinger mellem EU's medlemslande. Med Storbritanniens udtræden af EU den 1. april 2019 var det afgørende, at agenturet, som godkender nye lægemidler for EU, Island, Liechtenstein og Norge, forblev inden for EU's grænser. Hele 16 byer kæmpede om at blive den nye værtsby, herunder København, Milano, Barcelona og Bratislava.
En Afgørelse ved Lodtrækning
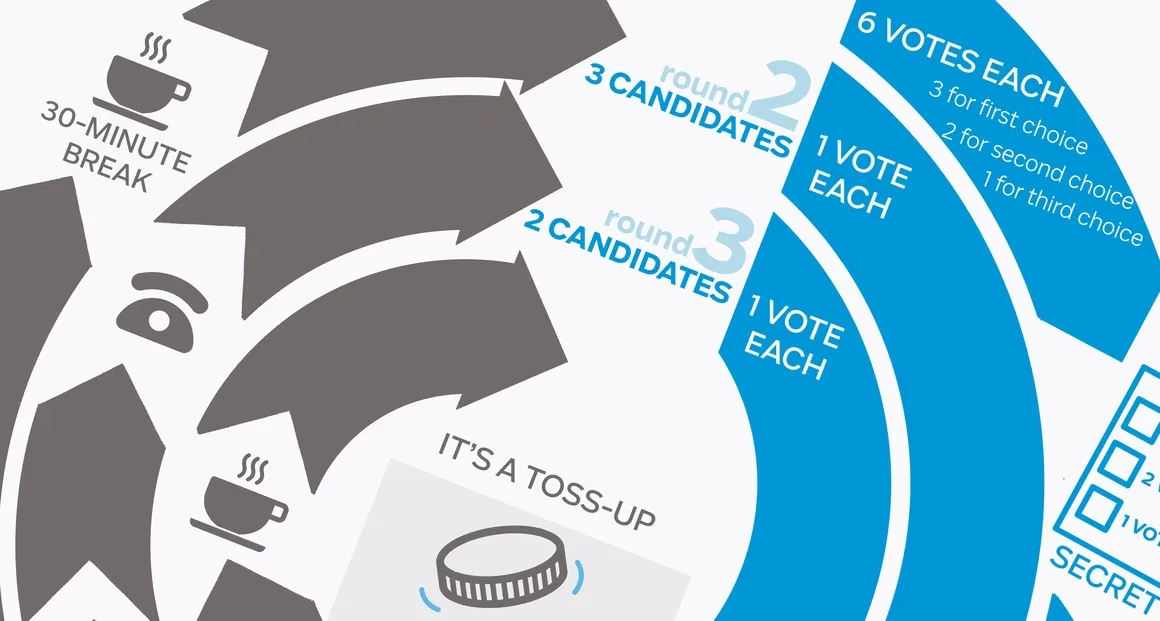
Selve afstemningen blandt de 27 EU-udenrigsministre i Bruxelles udviklede sig til en sand gyser. Processen bestod af tre afstemningsrunder. Efter første runde førte Milano med 25 stemmer, tæt fulgt af Amsterdam og København, begge med 20 stemmer. I anden runde blev København slået ud, hvilket efterlod en direkte duel mellem Milano med 12 stemmer og Amsterdam med 9. Den afgørende tredje runde endte i et dødt løb med 13 stemmer til hver by. Da reglerne ikke tillod yderligere afstemninger, blev den endelige vinder fundet ved en simpel lodtrækning. Loddet faldt ud til Amsterdams fordel, hvilket afsluttede den uforudsigelige og hårdt kæmpede konkurrence.
Flere tidlige favoritter, som Bratislava, faldt fra undervejs. Barcelonas kandidatur blev markant svækket af den politiske krise omkring Cataloniens uafhængighedsbestræbelser, hvilket understreger, hvordan storpolitik spillede en afgørende rolle i beslutningen.
Udfordringerne ved en Gigantisk Flytning
Valget af Amsterdam var kun begyndelsen på en enorm opgave. Byen skulle nu på rekordtid sikre, at agenturet kunne være fuldt operationelt fra den 1. april 2019. Dette indebar ikke kun at finde og klargøre en passende kontorbygning, men også at facilitere flytningen af 890 højt specialiserede medarbejdere og deres familier. Kravene var omfattende: fremragende transportforbindelser for de cirka 36.000 årlige besøgende (regulatorer og forskere), gode uddannelsesfaciliteter til omkring 600 børn, adgang til sundhedsydelser og jobmuligheder for medfølgende partnere.
En medarbejderundersøgelse foretaget af EMA selv havde tidligere vist, at Amsterdam var en af de foretrukne destinationer sammen med Barcelona, København, Milano og Wien. Dette var afgørende, da den største risiko ved flytningen var tabet af ekspertise. At fastholde så mange medarbejdere som muligt var vitalt for at sikre kontinuiteten i agenturets kritiske funktioner. Industrigrupper som European Federation of Pharmaceutical Industries and Associations (EFPIA) reagerede positivt på valget, men understregede netop vigtigheden af at minimere forstyrrelser, der kunne påvirke patienters adgang til medicin.
Flytningen var også en dyr affære. Den britiske kampagneleder Ben Goldacre beskrev opgaven med at flytte 890 medarbejdere som "svimlende dyr og enormt skadelig for patienter, både i Europa og i Storbritannien." EMA havde allerede mærket de økonomiske konsekvenser af Brexit, da faldet i pundets værdi over for euroen påvirkede budgettet, og agenturet måtte sætte visse arbejdsopgaver i bero for at fokusere på flytteplanlægningen.
Årsrapport 2017: Et Tilbageblik på Væsentlige Præstationer
På trods af den skygge, som Brexit kastede over agenturet, fremhæver årsrapporten for 2017 en række betydelige resultater og innovative projekter. Rapporten viser et agentur i fuld gang med at modernisere og forbedre sine processer til gavn for patienter og medicinalindustrien.
Et af de store fremskridt var afholdelsen af den første offentlige høring nogensinde. Dette initiativ øger gennemsigtigheden og giver patienter og offentligheden en direkte stemme i vurderingen af lægemidlers sikkerhed. Et andet markant skridt var lanceringen af det nye EudraVigilance-system. Dette avancerede system er afgørende for overvågningen af lægemidlers sikkerhed efter markedsføring, da det indsamler og analyserer indberetninger om formodede bivirkninger fra hele Europa, hvilket gør det muligt hurtigere at identificere potentielle risici.
Rapporten markerede også etårsdagen for PRIME-initiativet (PRIority MEdicines). Denne ordning er designet til at fremskynde udviklingen og godkendelsen af lægemidler, der adresserer udækkede medicinske behov. Ved at tilbyde tidlig og forbedret videnskabelig rådgivning hjælper PRIME udviklere med at generere robuste data, så lovende behandlinger hurtigere kan nå ud til de patienter, der har mest brug for dem. Endelig fremhævede rapporten et nyt samarbejde med den akademiske verden, som skal styrke båndene mellem regulatoriske myndigheder og forskningsinstitutioner.

Nøgletal og Tendenser
Årsrapporten er fyldt med data, der illustrerer omfanget af EMA's arbejde. Selvom de specifikke tal varierer fra år til år, giver rapporten et overblik over centrale aktiviteter. Nedenstående tabel giver et eksempel på de typer af data, der typisk præsenteres.
| Kategori | Beskrivelse |
|---|---|
| Nye Lægemidler | Statistik over antallet af ansøgninger om og godkendelser af nye lægemidler til både mennesker og dyr. |
| Bivirkningsrapporter | Data om antallet af indberettede formodede bivirkninger, som behandles i det nye EudraVigilance-system. |
| PRIME-ansøgninger | Antallet af lægemidler, der har ansøgt om og opnået status under prioritetsordningen for at fremskynde udviklingen. |
| Videnskabelig Rådgivning | Antallet af procedurer, hvor EMA har ydet videnskabelig rådgivning til lægemiddeludviklere for at optimere udviklingsprogrammer. |
Fremtidens Perspektiver: Fra Personlig Medicin til Brexit-Forberedelser
Årsrapporten ser ikke kun tilbage, men også fremad. Den indeholder refleksioner fra partnere og eksperter om nogle af de mest presserende emner inden for medicin og sundhed. Et centralt tema er Personlig medicin, hvor behandlinger skræddersys til den enkelte patient baseret på genetiske eller andre biomarkører. Dette felt er i hastig udvikling og stiller nye krav til de regulatoriske myndigheder.
Et andet vigtigt emne er rollen for Farmakovigilans (lægemiddelovervågning) i en tid med hastig innovation. Med nye og mere komplekse behandlinger, som f.eks. celle- og genterapier, bliver det endnu vigtigere at have robuste systemer som EudraVigilance til at overvåge sikkerheden på lang sigt. Rapporten fremhæver også det voksende behov for tættere samarbejde mellem regulatoriske myndigheder som EMA og de nationale organer, der vurderer medicinteknologi (Health Technology Assessment, HTA) og prissætning. Et sådant samarbejde kan sikre, at patienter ikke kun får adgang til sikre og effektive lægemidler, men også at sundhedssystemerne har råd til dem.
Ofte Stillede Spørgsmål (FAQ)
Her er svar på nogle af de mest almindelige spørgsmål om EMA's flytning og arbejde.
Hvorfor skulle Det Europæiske Lægemiddelagentur flytte fra London?
EMA er et EU-agentur og skal derfor have sit hovedsæde i et EU-medlemsland. Da Storbritannien stemte for at forlade EU (Brexit), blev det nødvendigt at flytte agenturet fra London til en by inden for EU's grænser for at sikre dets juridiske og operationelle funktion.
Hvorfor blev Amsterdam valgt som den nye værtsby?
Amsterdam blev valgt efter en intens konkurrence med 15 andre byer. Valget blev truffet gennem en afstemningsproces blandt EU's medlemslande. I den sidste og afgørende runde stod det lige mellem Amsterdam og Milano, og den endelige afgørelse blev truffet ved lodtrækning.
Hvad var de største udfordringer ved flytningen?
De primære udfordringer var at sikre kontinuiteten i agenturets arbejde uden afbrydelser, at fastholde dets næsten 900 højt specialiserede medarbejdere og deres familier, og at håndtere de enorme logistiske og økonomiske omkostninger ved flytningen inden for en meget stram tidsfrist.
Hvad er PRIME-initiativet, som nævnes i årsrapporten?
PRIME (PRIority MEdicines) er en ordning, der har til formål at yde tidlig og forbedret videnskabelig og regulatorisk støtte til lægemidler, der har potentiale til at imødekomme udækkede medicinske behov hos patienter. Målet er at fremskynde udviklingen og godkendelsen af disse lovende behandlinger.
Samlet set tegner situationen omkring EMA et billede af en organisation i en historisk brydningstid. På den ene side er der de konkrete og imponerende resultater fra 2017, som viser et agentur på forkant med videnskaben og dedikeret til at forbedre folkesundheden. På den anden side er der den monumentale og forstyrrende opgave med at flytte hele sin eksistens til et nyt land. EMA's evne til at navigere i denne dobbelte virkelighed vil være afgørende for millioner af patienters sundhed og velvære i hele Europa i de kommende år.
Hvis du vil læse andre artikler, der ligner EMA: Brexit-flytning og Årets Højdepunkter, kan du besøge kategorien Sundhed.

