31/07/2020
At navigere i landskabet for medicinsk udstyr i Den Europæiske Union kræver en dyb forståelse af de regulatoriske rammer, især EU's forordning om medicinsk udstyr (MDR - Medical Device Regulation). En central del af denne forordning er definitionen og ansvarsfordelingen mellem de såkaldte økonomiske aktører. Disse aktører udgør rygraden i forsyningskæden og sikrer, at medicinsk udstyr, der bringes på markedet, er sikkert, effektivt og i overensstemmelse med lovgivningen. For enhver virksomhed, der opererer inden for dette felt, er det ikke blot en fordel, men en absolut nødvendighed at kende til disse roller og deres forpligtelser.

Begrebet 'økonomisk aktør' dækker over enhver virksomhed eller organisation, der leverer varer, arbejder eller tjenester på et marked. Inden for MDR er dette begreb blevet afgørende for at definere de specifikke juridiske enheder, der har et ansvar for et produkt gennem hele dets livscyklus, fra design og produktion til distribution og overvågning efter markedsføring. Denne guide vil bryde de komplekse krav ned og give et klart overblik over de fire primære økonomiske aktører og deres indbyrdes samspil.
Hvem er de Økonomiske Aktører under MDR?
EU's MDR (Forordning 2017/745) identificerer fire distinkte juridiske enheder som økonomiske aktører. Hver af disse har unikke, men ofte overlappende, ansvarsområder, der er designet til at skabe et robust system for sporbarhed og sikkerhed. Det er afgørende at forstå, at en enkelt virksomhed kan udfylde flere roller, men forpligtelserne for hver rolle skal stadig opfyldes separat.
1. Producenten
Producenten er den juridiske enhed, der designer og/eller fremstiller et medicinsk udstyr med henblik på at markedsføre det under eget navn eller varemærke. Det er vigtigt at bemærke, at producenten ikke nødvendigvis er den, der fysisk samler produktet. De kan outsource produktionen til en underleverandør, men de bevarer det fulde juridiske ansvar for produktets overensstemmelse med MDR. Deres forpligtelser er de mest omfattende og er detaljeret beskrevet i MDR, artikel 10. Nogle af de centrale ansvarsområder inkluderer:
- Udarbejdelse og vedligeholdelse af teknisk dokumentation.
- Implementering af et kvalitetsstyringssystem (QMS).
- Gennemførelse af klinisk evaluering.
- Tildeling af en UDI (Unique Device Identifier) til deres produkter.
- Etablering af et system til overvågning efter markedsføring (Post-Market Surveillance, PMS).
- Indberetning af alvorlige hændelser og iværksættelse af sikkerhedsrelaterede korrigerende handlinger.
2. Den Autoriserede Repræsentant (AR)
Når en producent er baseret uden for EU, skal de udpege en autoriseret repræsentant, der er etableret i Unionen. Den autoriserede repræsentant (ofte forkortet AR eller EC Rep) fungerer som det primære kontaktpunkt mellem den ikke-EU-baserede producent og de nationale kompetente myndigheder. Deres rolle er ikke blot administrativ; de deler et juridisk ansvar med producenten for defekte produkter. Deres forpligtelser, som findes i MDR, artikel 11, omfatter:
- Verificering af, at producenten har udført den korrekte overensstemmelsesvurdering og udarbejdet den tekniske dokumentation.
- At have en kopi af den tekniske dokumentation tilgængelig for myndighederne.
- At samarbejde med myndighederne om eventuelle korrigerende handlinger.
- At blive identificeret på produktets mærkning, emballage eller i brugsanvisningen.
3. Importøren
En importør er enhver person eller virksomhed, der er etableret i EU, og som bringer et medicinsk udstyr fra et tredjeland (uden for EU) på EU-markedet for første gang. Importøren overtager det finansielle ejerskab af produktet, når det krydser grænsen. Deres rolle er afgørende for at sikre, at kun produkter, der overholder reglerne, kommer ind på markedet. I henhold til MDR, artikel 13, skal importøren:
- Verificere, at produktet er CE-mærket og har en EU-overensstemmelseserklæring.
- Sikre, at producenten har udpeget en autoriseret repræsentant.
- Angive deres eget navn, registrerede firmanavn og adresse på produktet, emballagen eller i et medfølgende dokument. Dette er afgørende for forsyningskædens sporbarhed.
- Føre et register over klager, produkter, der ikke er i overensstemmelse, og tilbagekaldelser.
- Informere producenten og den autoriserede repræsentant, hvis de har grund til at tro, at et produkt udgør en alvorlig risiko.
4. Distributøren
En distributør er enhver person eller virksomhed i forsyningskæden, ud over producenten eller importøren, som gør et medicinsk udstyr tilgængeligt på markedet. Dette kan være grossister, apoteker eller andre forhandlere. Deres primære ansvar, beskrevet i MDR, artikel 14, er at handle med fornøden omhu for at sikre, at de produkter, de håndterer, overholder reglerne. Deres opgaver inkluderer:
- At verificere, at produktet har CE-mærke, EU-overensstemmelseserklæring og den nødvendige mærkning (herunder oplysninger om importøren, hvis relevant).
- At sikre, at opbevarings- og transportbetingelserne, som specificeret af producenten, overholdes.
- At samarbejde med andre økonomiske aktører og myndighederne ved at videregive klager og indberetninger om hændelser.
- At deltage i sporingsaktiviteter for at identificere, hvem de har leveret et produkt til, og hvem de har modtaget det fra.
Samspillet mellem Aktørerne: To Scenarier
For at illustrere, hvordan disse roller fungerer i praksis, kan vi se på to forenklede eksempler.

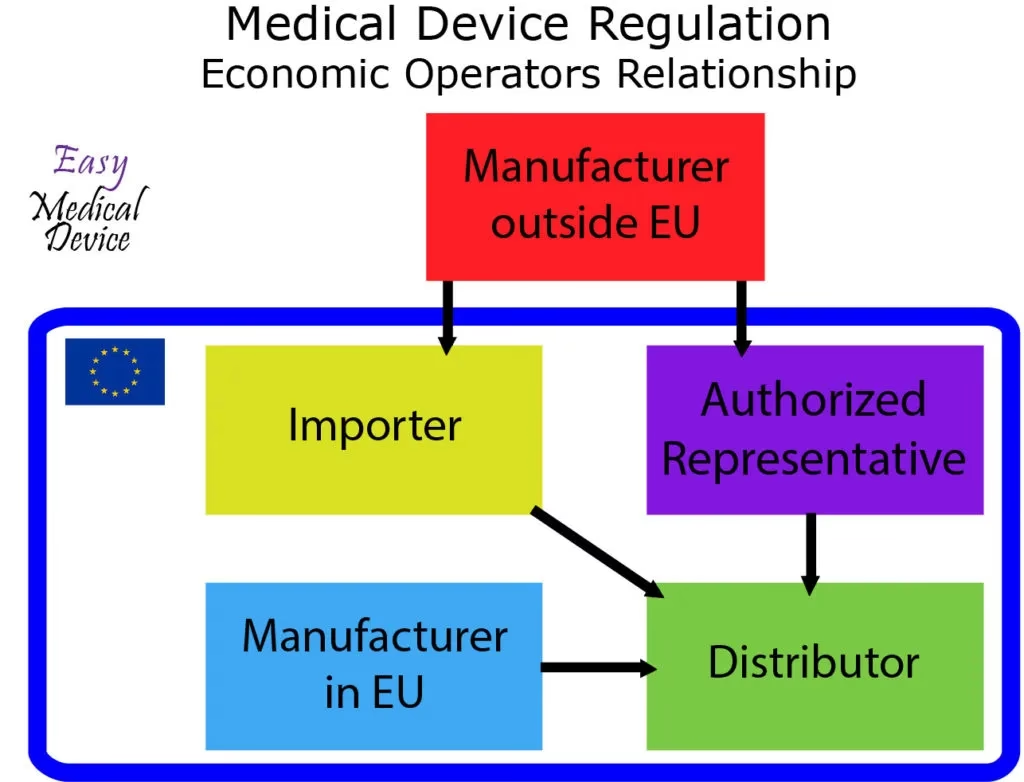
Scenarie 1: Producenten er baseret i EU
Forestil dig en producent i Tyskland, der får sine komponenter fra Kina. De samler og steriliserer det endelige produkt i Tyskland. Når produktet sendes til distributører i Spanien og Italien, er der kun to typer økonomiske aktører involveret: producenten (i Tyskland) og distributørerne (i Spanien og Italien). Da producenten er i EU, er der ikke behov for en autoriseret repræsentant. Og da producenten selv bringer varen ind i EU's toldområde og bevarer ejerskabet, er der heller ikke en 'importør' i MDR's forstand, selvom der kan være en importør i toldmæssig forstand.
Scenarie 2: Producenten er baseret uden for EU
Lad os nu tage en producent i USA. De producerer udstyret i USA og ønsker at sælge det i EU. Her bliver kæden mere kompleks. Den amerikanske producent skal først udpege en autoriseret repræsentant i et EU-land, f.eks. Irland. Derefter skal de have en aftale med en importør, f.eks. et firma i Holland, som køber produkterne og bringer dem ind i EU. Denne importørs navn og adresse skal påføres produktet. Fra Holland kan produkterne så sælges videre til distributører i f.eks. Frankrig og Polen. I dette tilfælde er alle fire økonomiske aktører aktive: producenten (USA), den autoriserede repræsentant (Irland), importøren (Holland) og distributørerne (Frankrig, Polen).
Tabel over Ansvarsområder
Denne tabel giver et hurtigt overblik over de primære forpligtelser for hver aktør.
| Økonomisk Aktør | Kerneansvar | MDR Artikel |
|---|---|---|
| Producent | Sikre produktets overensstemmelse, teknisk dokumentation, QMS, PMS. | Artikel 10 |
| Autoriseret Repræsentant | Fungere som kontaktpunkt for ikke-EU-producenter, verificere dokumentation. | Artikel 11 |
| Importør | Verificere overensstemmelse ved markedsføring, sikre sporbarhed via mærkning. | Artikel 13 |
| Distributør | Handle med fornøden omhu, verificere mærkning, sikre korrekte opbevaringsforhold. | Artikel 14 |
Strategier for at Sikre Overholdelse og Effektivitet
For en producent kan det virke overvældende at styre en kompleks forsyningskæde med flere økonomiske aktører. Men med en strategisk tilgang kan processen gøres mere håndterbar.
- Kortlæg din forsyningskæde: Det første skridt er at skabe et fuldstændigt overblik over alle juridiske enheder, der er involveret. Hvem er din importør? Hvor mange distributører har du? Hvilke lande opererer de i? En detaljeret kortlægning afslører potentielle risici og ansvarsområder.
- Kommuniker kravene tydeligt: Det er ikke nok blot at henvise dine partnere til MDR-teksten. Oversæt de juridiske krav til konkrete, operationelle procedurer. Hvad betyder det i praksis at 'verificere' et produkt? Hvordan og hvornår skal det dokumenteres? Klare aftaler og træning er afgørende.
- Forenkl hvor det er muligt: Overvej at strømline din forsyningskæde. At bruge én enkelt importør for hele EU kan drastisk reducere kompleksiteten med mærkning og registrering i EUDAMED (den europæiske database for medicinsk udstyr). Ligeledes kan en reduktion i antallet af distributører gøre det lettere at sikre ensartet kvalitet og overholdelse i hele kæden.
Ofte Stillede Spørgsmål (FAQ)
Hvad er den største forskel på en importør og en distributør?
Den primære forskel er, at importøren er den første enhed, der bringer et produkt fra et land uden for EU ind på EU-markedet. Distributøren opererer længere nede i forsyningskæden, efter at produktet allerede er på EU-markedet. Importøren har desuden en specifik forpligtelse til at påføre sit navn og sin adresse på produktet for at sikre sporbarhed.
Skal en producent i EU have en autoriseret repræsentant?
Nej. Kravet om en autoriseret repræsentant gælder kun for producenter, der ikke er fysisk etableret i et EU-land.

Hvem er ansvarlig, hvis et medicinsk udstyr viser sig at være defekt?
Producenten bærer det primære juridiske ansvar for produktets sikkerhed og ydeevne. Dog har MDR skabt et system med delt ansvar. Hvis en importør eller distributør ikke har opfyldt deres verifikations- og overvågningspligter, kan de også holdes ansvarlige. For ikke-EU-producenter er den autoriserede repræsentant juridisk medansvarlig sammen med producenten.
Hvad er EUDAMED?
EUDAMED er den europæiske database for medicinsk udstyr. Den er designet til at forbedre gennemsigtighed og koordinering mellem medlemsstater, økonomiske aktører og offentligheden. Alle økonomiske aktører (undtagen distributører, i de fleste tilfælde) skal registrere sig i EUDAMED for at få et unikt registreringsnummer (SRN - Single Registration Number).
At forstå og korrekt implementere rollerne for de økonomiske aktører er fundamentalt for at opnå og vedligeholde adgang til det europæiske marked for medicinsk udstyr. Det er ikke kun en øvelse i regulatorisk overholdelse; det er en integreret del af at levere sikre og effektive produkter til patienter og sundhedspersonale i hele Europa.
Hvis du vil læse andre artikler, der ligner Økonomiske Aktører under EU MDR: En Komplet Guide, kan du besøge kategorien Sundhed.
