09/12/2002
Hver dag tager millioner af mennesker medicin, der forbedrer deres livskvalitet, bekæmper sygdomme og endda redder liv. Men bag hver pille, vaccine eller infusion ligger en lang og utroligt kompleks rejse. En rejse, der starter med en enkelt idé eller et uventet fund i et laboratorium og kan strække sig over et årti, før den ender på apotekets hylder. Denne proces, kendt som lægemiddelopdagelse, er en af de mest vitale og udfordrende discipliner inden for moderne videnskab. Den kombinerer biologi, kemi, farmakologi og avanceret teknologi i en utrættelig søgen efter nye måder at behandle og helbrede menneskelige lidelser på. I denne artikel vil vi udforske den fascinerende historie, de grundlæggende principper og de innovative metoder, der driver opdagelsen af fremtidens medicin.
En historisk rejse: Fra tilfældighed til design
Historien om lægemiddelopdagelse er en fortælling om en bemærkelsesværdig udvikling. Før midten af det 20. århundrede var processen ofte præget af held, tilfældigheder og observationer. Mange tidlige lægemidler blev opdaget ved at screene et stort antal naturlige produkter eller syntetiske forbindelser uden en dybere forståelse for, hvordan de virkede. Et klassisk eksempel er opdagelsen af penicillin af Alexander Fleming i 1928, som skete ved et rent tilfælde, da en skimmelkultur kontaminerede en af hans bakterieprøver. Denne æra var domineret af, hvad man kan kalde "blind screening", hvor man testede tusindvis af stoffer i håb om at finde et, der havde en gavnlig effekt.
Vendepunktet kom i 1950'erne. Med store fremskridt inden for organisk kemi og en voksende forståelse for menneskelig biologi og sygdomsmekanismer, begyndte en ny æra: rationelt lægemiddeldesign. Forskere begyndte at bevæge sig væk fra den tilfældige tilgang og hen imod en mere logisk og målrettet metode. I stedet for blot at lede efter et stof, der virkede, begyndte de at spørge *hvorfor* det virkede. Dette skift i tankegang lagde grundlaget for den moderne farmakologi og den systematiske tilgang, vi anvender i dag.
Hvad er et "mål"? Hjertet i moderne lægemiddelopdagelse
For at forstå moderne lægemiddelopdagelse er det afgørende at forstå begrebet et "target" eller et "mål". I farmaceutisk sammenhæng er et mål typisk en specifik cellulær eller molekylær struktur i kroppen, der er involveret i en bestemt sygdomsproces. Målet for et lægemiddel er det sted, hvor lægemidlet skal binde sig og udøve sin virkning for at modvirke sygdommen. Man kan tænke på det som en lås (målet) og en nøgle (lægemidlet). Kun den rigtige nøgle kan åbne låsen og skabe den ønskede effekt.
Disse mål er oftest proteiner, såsom enzymer, receptorer på celleoverfladen (som G-protein-koblede receptorer) eller proteinkinaser. Forskere skelner generelt mellem to typer af mål:
- Etablerede mål: Dette er mål, som er velkendte og grundigt beskrevet i den videnskabelige litteratur. Der er en solid forståelse for, hvordan de fungerer i både en sund krop og under sygdom. At udvikle lægemidler mod etablerede mål er ofte forbundet med lavere risiko, da den biologiske baggrund er velbelyst.
- Nye mål: Dette er mål, som er mindre forståede, eller som først for nylig er blevet identificeret som potentielt involveret i en sygdom. Arbejdet med nye mål er mere risikabelt og uforudsigeligt, men det har potentialet til at føre til helt nye og banebrydende behandlinger for sygdomme, hvor der i dag mangler effektive løsninger.
Identificeringen og valideringen af et godt mål er det første og måske vigtigste skridt i hele processen med lægemiddeludvikling.

Veje til opdagelse: De primære metoder
I dag anvender forskere flere forskellige strategier til at finde nye lægemiddelkandidater. Disse kan groft inddeles i tre hovedkategorier.
1. Ny indsigt i sygdomsprocesser (Målrettet design)
Dette er kernen i rationelt lægemiddeldesign. Processen starter med en dybdegående forståelse af en sygdoms biologi. Forskere identificerer et specifikt mål – for eksempel et overaktivt enzym, der driver kræftvækst. Med denne viden kan kemikere designe og syntetisere molekyler, der er skræddersyet til at binde sig til og hæmme netop dette enzym. Dette kaldes målrettet design og er en meget præcis og vidensdrevet tilgang, som har ført til mange af de mest effektive lægemidler på markedet i dag, især inden for onkologi.
2. Screening af molekylære forbindelser
Selvom vi er blevet bedre til at designe lægemidler, spiller screening stadig en afgørende rolle. Dette er den moderne, højteknologiske version af den gamle metode. Ved hjælp af robotteknologi kan forskere udføre "High-Throughput Screening" (HTS), hvor hundredtusindvis eller endda millioner af forskellige kemiske forbindelser automatisk testes mod et specifikt sygdomsmål. Disse forbindelser kan komme fra store syntetiske "biblioteker" eller fra naturen (planter, svampe, marine organismer). De forbindelser, der viser en ønsket aktivitet, kaldes "hits", og de bliver udgangspunktet for yderligere kemisk optimering.
3. Uventede effekter af eksisterende lægemidler (Drug Repurposing)
Nogle gange kommer de største opdagelser fra uventede steder. "Drug repurposing" eller "drug repositioning" er processen, hvor man finder nye anvendelser for allerede godkendte lægemidler. Et lægemiddel, der er udviklet til én sygdom, kan vise sig at have uventede, gavnlige effekter på en helt anden. Et berømt eksempel er Sildenafil, der oprindeligt blev testet til behandling af hjerte-kar-sygdomme, men som viste sig at have en markant effekt på erektil dysfunktion og efterfølgende blev markedsført som Viagra. Denne tilgang er attraktiv, fordi lægemidlet allerede har gennemgået omfattende sikkerhedstest, hvilket kan forkorte udviklingstiden og reducere omkostningerne betydeligt.

Sammenligning af opdagelsesmetoder
| Metode | Fordele | Ulemper |
|---|---|---|
| Målrettet Design | Høj specificitet, færre bivirkninger, vidensdrevet. | Kræver dyb biologisk forståelse, tidskrævende i designfasen. |
| High-Throughput Screening | Kan teste millioner af stoffer hurtigt, kan afsløre uventede kemiske strukturer. | Mange falske positiver, "hits" kræver ofte omfattende optimering. |
| Drug Repurposing | Hurtigere og billigere, kendt sikkerhedsprofil. | Begrænset til eksisterende lægemidler, oprindelig patent kan være udløbet. |
Fra laboratorium til patient: En lang og kompleks proces
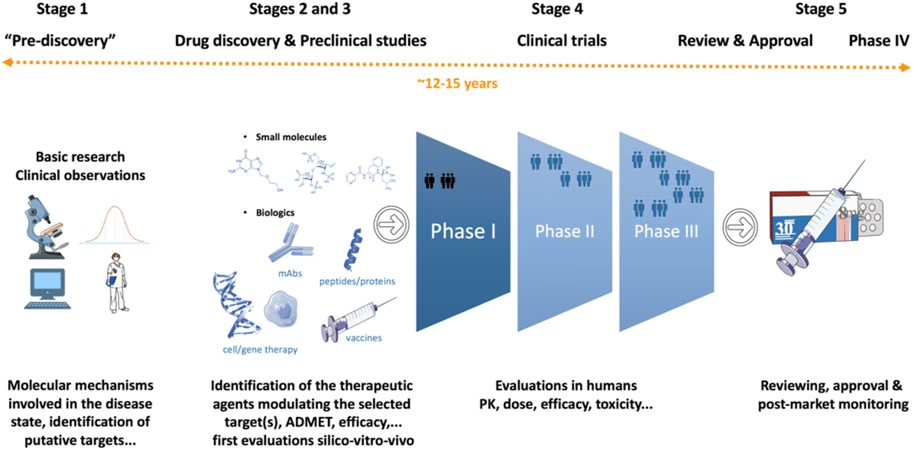
At opdage en lovende lægemiddelkandidat er kun begyndelsen. Herefter følger en lang og strengt reguleret udviklingsproces, før et lægemiddel kan godkendes og nå patienterne. Denne proces inkluderer:
- Prækliniske studier: Kandidaten testes grundigt i laboratoriet (in vitro) og i dyremodeller for at vurdere dens effektivitet og sikkerhed.
- Kliniske forsøg: Hvis de prækliniske studier er succesfulde, fortsætter processen med kliniske forsøg på mennesker. Disse er opdelt i tre faser:
- Fase I: Tester sikkerhed og dosering på en lille gruppe raske frivillige.
- Fase II: Tester effektivitet og bivirkninger på en mellemstor gruppe patienter med den pågældende sygdom.
- Fase III: Tester effektivitet og sikkerhed i stor skala på en stor gruppe patienter, ofte sammenlignet med eksisterende behandlinger eller placebo.
- Godkendelse: Hvis lægemidlet viser sig at være både sikkert og effektivt i fase III, indsendes alle data til de relevante sundhedsmyndigheder (f.eks. Det Europæiske Lægemiddelagentur, EMA, eller Lægemiddelstyrelsen i Danmark). Myndighederne gennemgår dokumentationen og beslutter, om lægemidlet kan godkendes til markedsføring.
Fremtiden for lægemiddelopdagelse
Feltet for lægemiddelopdagelse er i konstant udvikling, drevet af teknologiske fremskridt. Fremtiden byder på endnu mere sofistikerede metoder. Kunstig intelligens (AI) og machine learning bliver i stigende grad brugt til at analysere enorme datamængder, forudsige hvordan molekyler vil interagere med biologiske mål, og designe helt nye lægemiddelkandidater. Samtidig åbner personlig medicin, baseret på en patients unikke genetiske profil, op for muligheden for at skræddersy behandlinger til den enkelte. Teknologier som CRISPR-genredigering giver os også helt nye værktøjer til at forstå og potentielt korrigere de genetiske årsager til sygdomme. Denne fortsatte innovation lover en fremtid med endnu mere effektive og målrettede behandlinger.
Ofte Stillede Spørgsmål
Hvor lang tid tager det at udvikle et nyt lægemiddel?
Fra den indledende opdagelse til den endelige godkendelse tager processen typisk 10-15 år. Det er en lang og ressourcekrævende rejse, hvor langt de fleste kandidater falder fra undervejs.
Hvorfor er ny medicin så dyr?
De høje omkostninger afspejler de enorme investeringer i forskning og udvikling. For hvert lægemiddel, der når markedet, er der tusindvis af kandidater, der har fejlet i udviklingsprocessen. Omkostningerne til disse fejlslagne projekter skal dækkes af de succesfulde produkter.
Hvad er forskellen på et syntetisk og et naturligt lægemiddel?
Forskellen ligger i deres oprindelse. Et naturligt lægemiddel stammer direkte fra en levende organisme (f.eks. en plante, svamp eller bakterie), som penicillin. Et syntetisk lægemiddel er skabt udelukkende i et kemisk laboratorium. Ofte fungerer et naturligt stof som inspiration for udviklingen af et mere potent eller sikkert syntetisk lægemiddel.
Hvis du vil læse andre artikler, der ligner Fra laboratorium til apotek: Opdagelsen af ny medicin, kan du besøge kategorien Sundhed.
