25/11/2024
Når du modtager medicin fra apoteket, tager du det for givet, at den er sikker og virker som den skal. Men bag hver eneste pille, vaccine eller flydende medicin ligger en utrolig kompleks og streng proces, der er designet til at beskytte folkesundheden. I Danmark er det Lægemiddelstyrelsen, der står i spidsen for denne vigtige opgave. Processen hviler på to fundamentale søjler: en grundig inspektion af produktionsfaciliteterne for at sikre høj kvalitet og en dybdegående videnskabelig evaluering af lægemidlets effekt og sikkerhed, før det overhovedet når markedet. Denne artikel vil guide dig gennem hele rejsen, fra inspektørens besøg på fabrikken til den endelige godkendelse, der gør medicinen tilgængelig for danske patienter.
Hvad er God Fremstillingspraksis (GMP)?
Før vi dykker ned i selve godkendelsesprocessen for et lægemiddel, er det afgørende at forstå fundamentet for al lægemiddelproduktion: God Fremstillingspraksis, bedre kendt som GMP (Good Manufacturing Practice). GMP er et internationalt anerkendt regelsæt, der sikrer, at lægemidler produceres og kontrolleres i henhold til de højeste kvalitetsstandarder. Det handler ikke kun om det endelige produkt, men om hele produktionskæden.
GMP dækker alle aspekter af produktionen, herunder:
- Råmaterialer: Krav til kvalitet, oprindelse og kontrol af alle indgående materialer.
- Faciliteter og udstyr: Bygninger skal være designet til at forhindre krydskontaminering, og udstyr skal være korrekt kalibreret og vedligeholdt.
- Personale: Medarbejdere skal have den rette uddannelse, erfaring og hygiejnestandarder for at udføre deres opgaver.
- Dokumentation: Hvert eneste skridt i produktionsprocessen skal dokumenteres omhyggeligt. Dette sikrer sporbarhed og gør det muligt at undersøge eventuelle fejl.
- Kvalitetskontrol: Løbende tests og analyser under og efter produktionen for at sikre, at produktet lever op til specifikationerne.
Ved at overholde GMP minimerer producenterne risikoen for fejl, forurening og forvekslinger, som potentielt kan have katastrofale konsekvenser for patienterne. Det er Lægemiddelstyrelsens ansvar at inspicere virksomheder for at sikre, at de lever op til disse strenge krav.
Lægemiddelstyrelsens Inspektionsproces
For at verificere, at en lægemiddelproducent overholder GMP-reglerne, udfører Lægemiddelstyrelsens inspektører regelmæssige inspektioner. Disse inspektioner er en central del af tilsynet med lægemiddelindustrien i Danmark og i udlandet for virksomheder, der leverer til det danske marked.
Processen starter med, at virksomheden skal være registreret i EMA's (Det Europæiske Lægemiddelagentur) centrale database, OMS (Organisation Management Service). Denne registrering er en forudsætning for at kunne modtage et certifikat.
Efter en vellykket inspektion, og når eventuelle opfølgende punkter er blevet adresseret tilfredsstillende, udsteder Lægemiddelstyrelsen et GMP-certifikat. Dette sker typisk inden for 90 dage efter inspektionen. Certifikatet er et officielt bevis på, at virksomheden på en bestemt adresse overholder GMP-reglerne for de specifikke aktiviteter, der er blevet inspiceret. Et GMP-certifikat er gyldigt i tre år fra inspektionsdatoen. Herefter kræves en ny inspektion for at forny det.
Alle udstedte GMP-certifikater samt meddelelser om manglende overholdelse bliver offentliggjort i den fælleseuropæiske database EudraGMDP. Dette skaber gennemsigtighed og gør det muligt for myndigheder og virksomheder i hele EU at verificere en producents status. I dag udstedes certifikaterne digitalt og kan findes direkte i databasen, hvilket har erstattet de tidligere papirversioner.
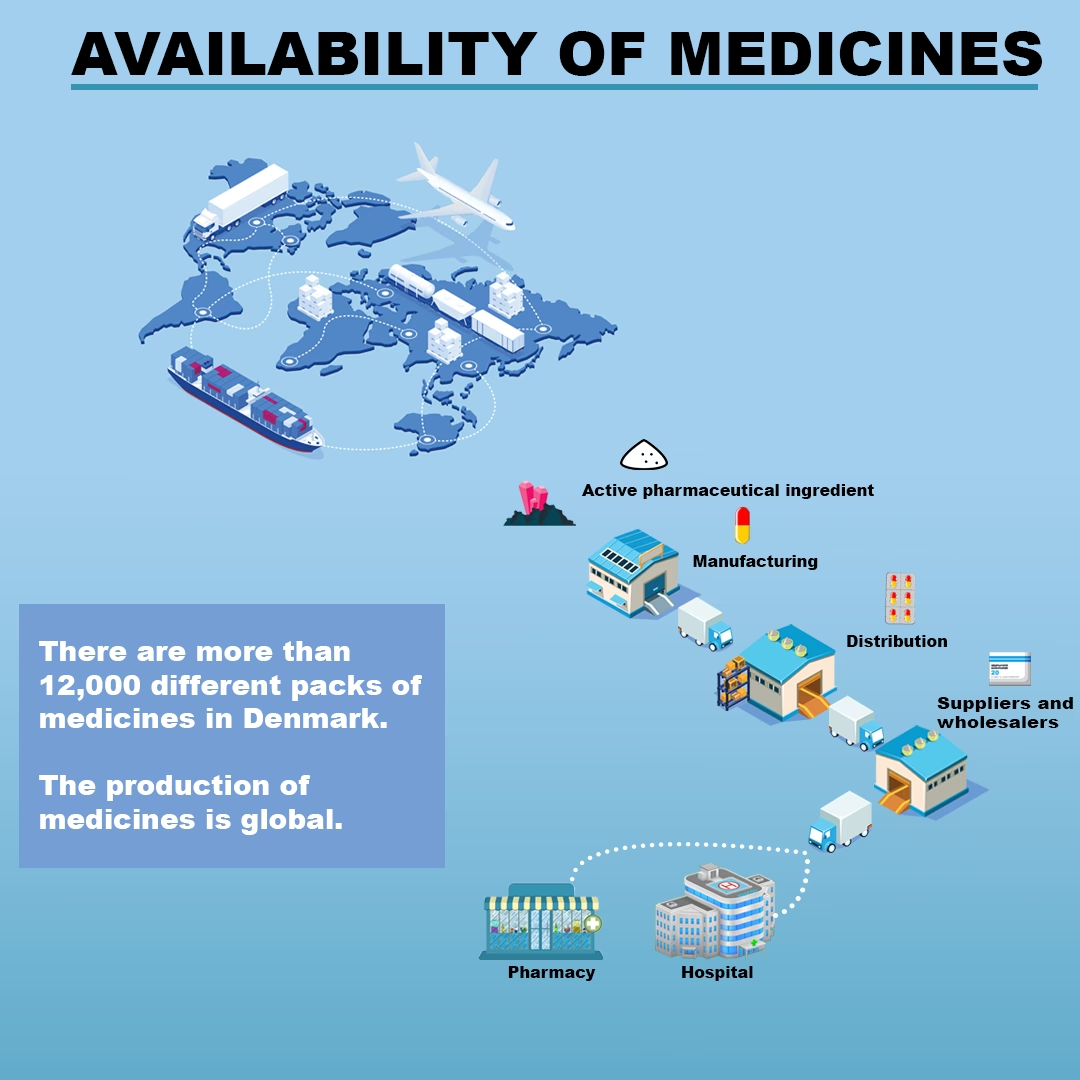
Vejen til Godkendelse: Fra Laboratorium til Patient
Når en virksomhed har styr på sin produktion (GMP), begynder den lange og omkostningstunge proces med at få et nyt lægemiddel godkendt. Denne proces er designet til at bevise, at lægemidlet er både effektivt til at behandle den pågældende sygdom og sikkert for patienterne at anvende.
1. Præklinisk Fase
Før et lægemiddel kan testes på mennesker, skal det gennemgå en omfattende præklinisk fase. Her udføres tests i laboratoriet (in vitro) og i dyreforsøg (in vivo) for at undersøge lægemidlets farmakologiske egenskaber, dets toksicitet (giftighed) og for at få en første indikation af dets potentielle effekt. Kun hvis resultaterne fra denne fase er lovende, kan virksomheden søge om tilladelse til at starte kliniske forsøg med mennesker.
2. Kliniske Forsøg
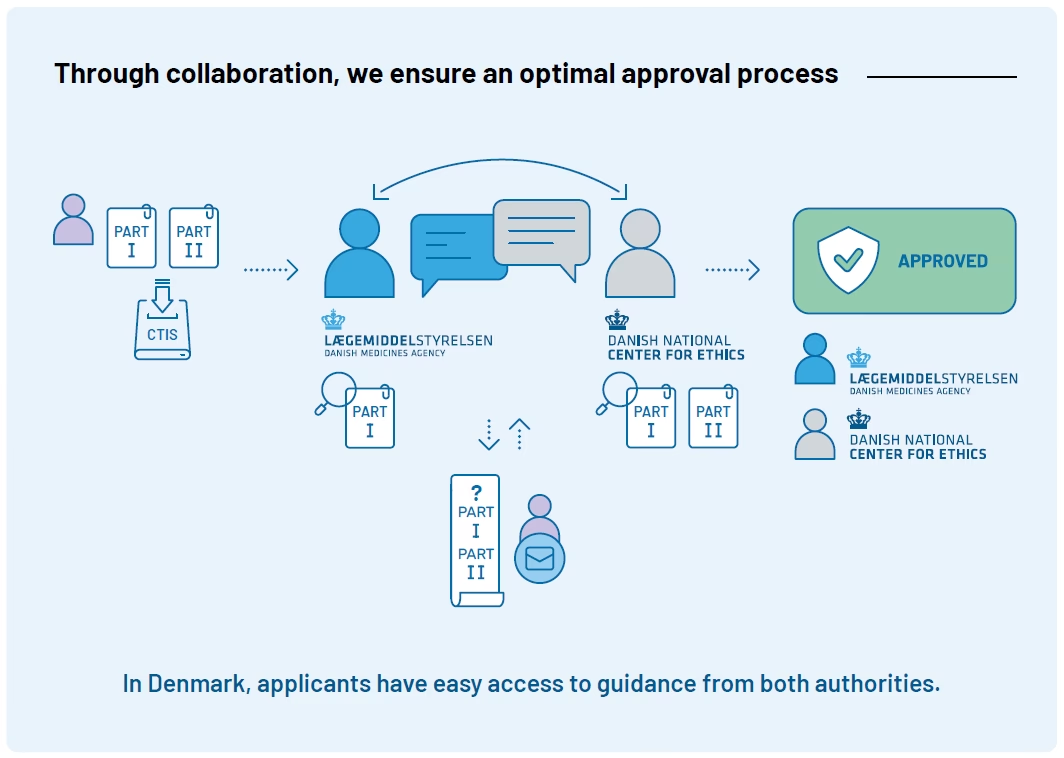
Kliniske forsøg er den mest kritiske del af udviklingsprocessen. De er strengt reguleret og skal godkendes af både Lægemiddelstyrelsen og en Videnskabsetisk Komité for at sikre deltagernes rettigheder og sikkerhed. Forsøgene er opdelt i tre hovedfaser:
| Fase | Primært Formål | Typiske Deltagere |
|---|---|---|
| Fase I | At vurdere sikkerhed, tolerabilitet og hvordan lægemidlet omsættes i kroppen. Doseringen fastlægges. | En lille gruppe (20-80) raske, frivillige deltagere. |
| Fase II | At undersøge lægemidlets effektivitet på en specifik sygdom og identificere almindelige bivirkninger. | En mellemstor gruppe (100-300) patienter med den pågældende sygdom. |
| Fase III | At bekræfte effektiviteten i en stor patientgruppe, overvåge bivirkninger og sammenligne lægemidlet med eksisterende standardbehandlinger. | En stor gruppe (ofte tusindvis) af patienter, ofte på tværs af flere lande. |
Gennem alle faser er informeret samtykke altafgørende. Deltagerne skal være fuldt informerede om forsøgets formål, potentielle risici og fordele, før de beslutter sig for at deltage, og de kan til enhver tid trække sig uden konsekvenser.
3. Ansøgning om Markedsføringstilladelse
Hvis de kliniske forsøg viser, at fordelene ved lægemidlet opvejer risiciene, samler virksomheden al dokumentation fra hele udviklingsforløbet – fra de tidligste laboratorieforsøg til de store fase III-studier – i en ansøgning om markedsføringstilladelse (Marketing Authorisation Application, MAA). Denne ansøgning indsendes til Lægemiddelstyrelsen (for en national godkendelse) eller oftere til EMA (for en central godkendelse, der gælder i hele EU). Myndighedernes eksperter gennemgår derefter omhyggeligt alle data for at vurdere lægemidlets kvalitet, sikkerhed og effekt, før en endelig afgørelse træffes.
Overvågning efter Godkendelse: Sikkerhed i Fokus
Arbejdet stopper ikke, når et lægemiddel er blevet godkendt. Faktisk begynder en ny og lige så vigtig fase: farmakovigilans, også kendt som lægemiddelovervågning. Selvom kliniske forsøg giver et solidt grundlag, udføres de under kontrollerede forhold på en afgrænset patientgruppe. Når lægemidlet tages i brug af en meget større og mere forskelligartet befolkning i den virkelige verden, kan sjældne bivirkninger eller interaktioner med andre lægemidler dukke op.

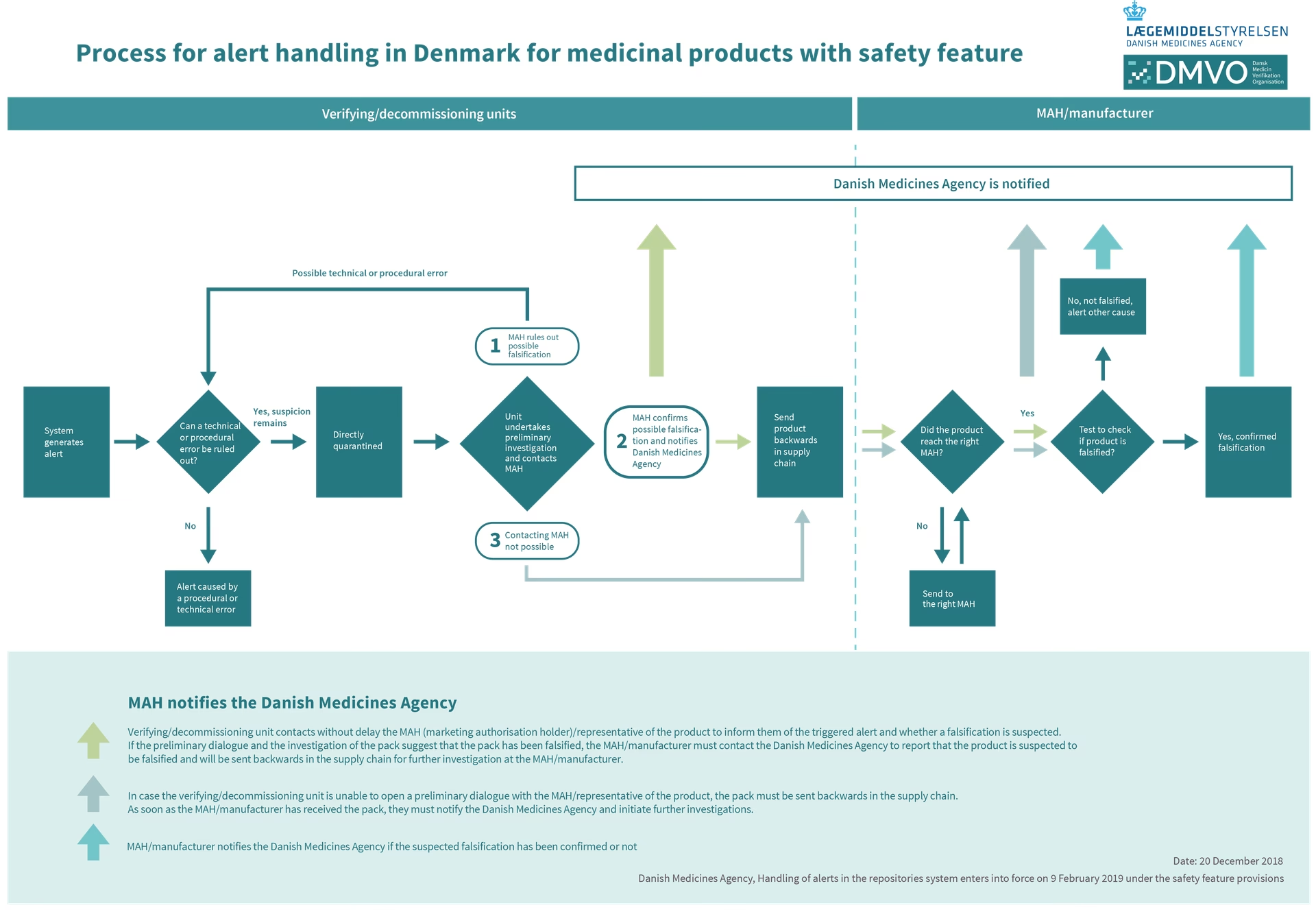
Både lægemiddelvirksomheder og myndigheder har ansvaret for løbende at indsamle og analysere data om bivirkninger. Læger, apotekere og patienter opfordres kraftigt til at indberette alle formodede bivirkninger til Lægemiddelstyrelsen. Denne konstante overvågning sikrer, at balancen mellem fordele og risici for et lægemiddel forbliver positiv gennem hele dets levetid. Hvis der opstår nye, alvorlige sikkerhedsproblemer, kan det føre til opdaterede advarsler i indlægssedlen, begrænsninger i brugen eller i yderste konsekvens, at lægemidlet trækkes tilbage fra markedet.
Ofte Stillede Spørgsmål (FAQ)
Hvad sker der, hvis en virksomhed ikke overholder GMP-reglerne?
Manglende overholdelse af GMP kan have alvorlige konsekvenser. Lægemiddelstyrelsen kan udstede en erklæring om manglende overholdelse, som offentliggøres i EudraGMDP-databasen. Dette kan føre til, at virksomhedens produktionstilladelse suspenderes eller inddrages. Derudover kan det resultere i store bøder og krav om tilbagekaldelse af produkter, der allerede er på markedet.
Hvem betaler for udviklingen og godkendelsen af ny medicin?
Det er lægemiddelvirksomhederne selv, der finansierer hele processen, fra forskning og udvikling til de dyre kliniske forsøg og ansøgningsgebyrer til myndighederne. Det er en langvarig og risikofyldt investering, da mange potentielle lægemidler falder fra undervejs i processen.
Kan jeg som patient se, hvilke kliniske forsøg der foregår i Danmark?
Ja, der er en høj grad af gennemsigtighed. Mange kliniske forsøg registreres i offentligt tilgængelige databaser, såsom den europæiske EU Clinical Trials Register, hvor man kan søge efter information om igangværende og afsluttede forsøg.
Hvorfor tager det så lang tid at få ny medicin godkendt?
Den lange tidsramme skyldes den grundighed, der kræves for at sikre patienternes sikkerhed. De prækliniske studier og de tre faser af kliniske forsøg tager mange år at gennemføre og analysere. Selve myndighedernes sagsbehandling tager også tid, da enorme mængder data skal gennemgås af eksperter. Det er en nødvendig balance mellem hurtig adgang til ny behandling og en garanti for, at medicinen er sikker og effektiv.
Hvis du vil læse andre artikler, der ligner Sådan sikres din medicin i Danmark, kan du besøge kategorien Sundhed.