09/09/2007
I hjertet af Europas sundhedssystem ligger en afgørende institution: Det Europæiske Lægemiddelagentur, bedre kendt som EMA. For de fleste borgere er det en organisation, der arbejder i kulisserne, men dens rolle er fundamental for vores sundhed og velvære. EMA er portvagten, der sikrer, at den medicin, vi finder på apotekets hylder og modtager på hospitalerne, er både sikker og effektiv. En nylig og omfattende reform af denne institution er sat i værk, med et løfte om at modernisere og optimere processerne. Målet er klart: at gøre nye og livsvigtige lægemidler hurtigere tilgængelige for patienterne i hele EU, herunder Danmark, uden at gå på kompromis med sikkerheden.
Denne reform er ikke blot en teknisk justering af bureaukratiske procedurer. Den repræsenterer et paradigmeskifte i, hvordan vi tænker på lægemiddelgodkendelse i en verden, der konstant udvikler sig med nye teknologier og sundhedsudfordringer. Men hvad indebærer denne reform helt præcist? Hvordan vil den påvirke den almindelige borger, medicinalindustrien og selve sundhedsvæsenet? Denne artikel dykker ned i kernen af EMA-reformen for at give dig et klart overblik over ændringerne og deres betydning.
Forståelsen af EMA's nuværende rolle
Før vi kan forstå betydningen af reformen, er det vigtigt at have et solidt greb om, hvad EMA gør i dag. Når et medicinalfirma udvikler et nyt lægemiddel, kan det ikke bare sendes på markedet. Det skal igennem en yderst grundig og videnskabelig evaluering for at vurdere dets kvalitet, sikkerhed og effekt. I Europa er det EMA, der står i spidsen for denne centrale procedure.
Processen fungerer således, at et firma indsender en ansøgning om markedsføringstilladelse til EMA. Agenturet koordinerer derefter en videnskabelig vurdering, der udføres af ekspertkomitéer bestående af repræsentanter fra de nationale lægemiddelmyndigheder i alle EU's medlemslande. Når EMA's komitéer har afgivet en positiv anbefaling, er det op til Europa-Kommissionen at udstede den endelige markedsføringstilladelse. Denne tilladelse er gyldig i hele EU, hvilket betyder, at et lægemiddel, der er godkendt centralt, kan sælges i alt fra Danmark til Cypern. Dette system sikrer en ensartet høj standard og sparer virksomhederne for at skulle ansøge i hvert enkelt land.
Selvom dette system har tjent Europa godt og sikret et højt beskyttelsesniveau for patienterne, har det også været kritiseret for at være langsommeligt og administrativt tungt. Den regulatoriske byrde for virksomhederne kan være enorm, og de lange godkendelsestider kan betyde, at patienter med alvorlige sygdomme må vente unødigt længe på nye, potentielt livreddende behandlinger.
Kernen i reformen: De tre hovedmål
EMA-reformen er designet til at adressere disse udfordringer direkte. Den hviler på tre centrale søjler, der tilsammen skal skabe et mere agilt, effektivt og fremtidssikret lægemiddelagentur.
1. Øget effektivitet og strømlining
Et af de primære mål er at gøre hele godkendelsesprocessen mere effektiv. Dette indebærer en dybdegående gennemgang af interne arbejdsgange hos EMA. Reformen sigter mod at digitalisere flere processer, reducere unødvendigt papirarbejde og forbedre kommunikationen mellem de forskellige videnskabelige komitéer og de nationale myndigheder. Ved at optimere ressourceallokeringen og fjerne flaskehalse i systemet, forventes det, at sagsbehandlingstiden kan nedbringes markant. Det handler om at arbejde smartere, ikke mindre grundigt.
2. Reduktion af den regulatoriske byrde
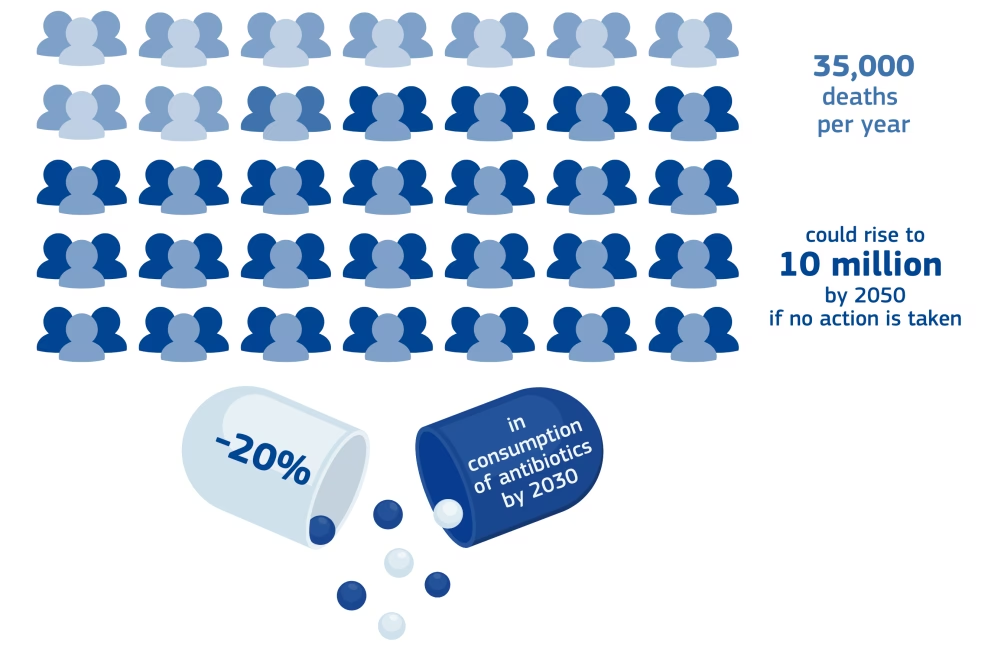
For medicinalvirksomheder, især mindre biotekfirmaer og akademiske forskningsgrupper, kan den nuværende regulatoriske proces virke uoverskuelig og omkostningstung. Reformen søger at lette denne byrde. Det kan for eksempel ske ved at indføre mere fleksible ansøgningsformater, forenkle kravene til dokumentation (hvor det er forsvarligt) og tilbyde bedre og tidligere videnskabelig rådgivning. Målet er at gøre det lettere for innovatører at navigere i systemet, hvilket kan fremme udviklingen af nye lægemidler, især inden for områder med udækkede medicinske behov, såsom sjældne sygdomme eller nye former for antibiotika.
3. Hurtigere godkendelsestider for lægemidler
Det mest direkte og mærkbare resultat for patienter vil være hurtigere adgang til ny medicin. Ved at opnå større effektivitet og en lavere regulatorisk byrde bliver det muligt at forkorte den samlede tid fra en ansøgning indsendes, til et lægemiddel er godkendt og tilgængeligt på markedet. Dette er især kritisk for patienter med livstruende sygdomme som kræft eller alvorlige kroniske lidelser, hvor hver eneste dag tæller. Reformen skal sikre, at videnskabelige gennembrud omsættes til konkrete behandlinger for patienterne så hurtigt som muligt, uden at gå på kompromis med de strenge sikkerheds- og effektkrav.
Sammenligning: Før og efter reformen
For at illustrere de forventede ændringer, kan vi opstille en sammenligningstabel:
| Aspekt | Før reformen (Traditionel proces) | Efter reformen (Forventet resultat) |
|---|---|---|
| Godkendelsestid | Lang og ofte uforudsigelig. Kan tage over et år. | Markant reduceret og mere forudsigelig. |
| Regulatorisk byrde | Høj, med omfattende papirarbejde og komplekse krav. | Reduceret gennem digitalisering og forenklede procedurer. |
| Processer | Primært sekventielle og papirbaserede. | Mere parallelle, digitale og data-drevne. |
| Adgang for patienter | Forsinkelser kan opstå pga. lange administrative processer. | Hurtigere adgang til innovative og livsvigtige behandlinger. |
Hvad betyder reformen for dig som patient i Danmark?
Selvom EMA opererer på et europæisk niveau, har reformen direkte konsekvenser for danske patienter. Når et lægemiddel godkendes af EMA, kan det markedsføres i Danmark. En hurtigere proces hos EMA betyder derfor, at danske læger og hospitaler hurtigere kan tage nye behandlingsmuligheder i brug. For en kræftpatient kan det betyde adgang til en ny immunterapi måneder tidligere end før. For en person med en sjælden genetisk sygdom kan det være den første effektive behandling, der nogensinde bliver tilgængelig. Denne øgede effektivitet er derfor ikke bare en administrativ øvelse; den kan oversættes direkte til forbedret livskvalitet og i nogle tilfælde overlevelse.
Det er dog vigtigt at understrege, at reformen ikke ændrer på de grundlæggende krav til sikkerhed. Sikkerheden for patienterne er og vil altid være den højeste prioritet for Det Europæiske Lægemiddelagentur. De videnskabelige standarder for, hvad der kræves for at bevise et lægemiddels effekt og sikkerhed, forbliver urørte. Reformen handler om at fjerne unødvendig ventetid og bureaukrati – ikke om at slække på kravene.
Ofte Stillede Spørgsmål (FAQ)
Betyder en hurtigere godkendelse, at medicinen er mindre sikker?
Nej, absolut ikke. Reformens formål er at optimere de administrative processer, ikke at springe over videnskabelige evalueringer. De strenge krav til data om sikkerhed, kvalitet og effekt vil være de samme. Sikkerhedsovervågningen af lægemidler, også efter de er kommet på markedet, vil fortsat være en kerneopgave for EMA og de nationale myndigheder.
Hvornår vil vi mærke effekten af denne reform?
Implementeringen af en så stor reform er en gradvis proces. Nogle ændringer vil kunne mærkes relativt hurtigt, mens andre, især dem der kræver store digitale omstillinger, vil tage flere år at implementere fuldt ud. Man forventer dog at se en gradvis forbedring i sagsbehandlingstiderne over de kommende år.
Vil reformen gøre medicin billigere?
Reformen fokuserer primært på godkendelsesprocessen og ikke direkte på prissætning af medicin, som er et nationalt anliggende. Dog kan en lavere regulatorisk byrde og hurtigere vej til markedet potentielt reducere udviklingsomkostningerne for virksomhederne. Om dette vil afspejle sig i lavere priser for forbrugerne er dog et komplekst spørgsmål, der afhænger af mange andre faktorer.
Konklusion: En fremtid med hurtigere og bedre behandling
Reformen af Det Europæiske Lægemiddelagentur er et ambitiøst og nødvendigt skridt mod et mere moderne og patientfokuseret sundhedssystem i Europa. Ved at strømline processer, reducere bureaukrati og omfavne digitalisering sigter reformen mod at fjerne de barrierer, der unødigt forsinker adgangen til ny og innovativ medicin. For patienter i Danmark og resten af EU er budskabet klart: Hjælpen er på vej hurtigere, uden at der gås på kompromis med den sikkerhed og tryghed, som EMA er garant for. Det er en investering i en sundere fremtid for alle europæere.
Hvis du vil læse andre artikler, der ligner EMA-reformen: Hurtigere medicin til patienterne, kan du besøge kategorien Sundhed.