14/11/2023
I en verden, hvor medicinske fremskridt sker med lynets hast, er få teknologier så omtalte og potentielt revolutionerende som CRISPR gen-redigering. Forestil dig en molekylær saks, der med kirurgisk præcision kan gå ind i vores arvemasse, finde en specifik fejl – en mutation, der forårsager en alvorlig sygdom – og rette den. Dette er ikke længere science fiction, men den virkelighed, som CRISPR-teknologien åbner døren for. Med potentialet til at korrigere sygdomsfremkaldende gener, er CRISPR en af de mest ventede teknologier i moderne medicin og lover at omforme landskabet for genetisk definerede sygdomme for altid. Det globale marked for CRISPR-teknologi forventes at vokse til over 10 milliarder dollars inden 2027, drevet af en voksende forståelse for sygdommes genetiske oprindelse og fremkomsten af personlig medicin.
Hvad er CRISPR-Cas9 helt præcist?
CRISPR er et akronym for "Clustered Regularly Interspaced Short Palindromic Repeats". Det lyder kompliceret, men konceptet er mere ligetil. Systemet blev oprindeligt opdaget i bakterier, hvor det fungerer som et adaptivt immunsystem. Bakterier bruger det til at genkende og ødelægge DNA fra invaderende vira. Forskere, især Emmanuelle Charpentier og Jennifer Doudna, som vandt Nobelprisen i kemi i 2020 for deres opdagelse, indså, at dette naturlige forsvarssystem kunne omprogrammeres til at redigere gener i næsten enhver organisme, inklusiv mennesker.
Systemet består primært af to nøglekomponenter:
- Cas9-enzymet: Dette fungerer som den førnævnte 'molekylære saks'. Det er et protein, der kan klippe i DNA-strenge.
- Guide-RNA (gRNA): Dette er en lille stump RNA, der er designet til at matche en specifik DNA-sekvens. Det fungerer som en GPS, der guider Cas9-saksen til det helt rigtige sted i genomet, hvor klippet skal foretages.
Når Cas9 har klippet DNA'et, træder cellens egne naturlige reparationsmekanismer i kraft. Forskere kan udnytte denne proces til at slukke for et gen (ved at lade cellen reparere bruddet på en lidt rodet måde) eller indsætte en ny, korrekt DNA-sekvens (ved at levere en skabelon, som cellen kan bruge til reparationen). Denne præcision og relative enkelthed er, hvad der gør CRISPR så kraftfuld sammenlignet med tidligere metoder til gen-redigering.
Potentialet: Hvilke sygdomme kan CRISPR behandle?
Potentialet for CRISPR er enormt og strækker sig over et bredt spektrum af medicinske områder. Teknologien er især lovende for behandling af monogenetiske sygdomme – sygdomme forårsaget af en fejl i et enkelt gen. Men forskningen ser også på mere komplekse lidelser.
Monogenetiske sygdomme
Dette er det mest oplagte og umiddelbare anvendelsesområde. Sygdomme som seglcelleanæmi, cystisk fibrose, Huntingtons sygdom og Duchennes muskeldystrofi er alle forårsaget af veldefinerede genetiske mutationer. Med CRISPR er det teoretisk muligt at korrigere disse mutationer direkte i patientens celler. For eksempel er der allerede kliniske forsøg i gang, hvor man tager stamceller ud fra patienter med seglcelleanæmi, redigerer det defekte gen i laboratoriet med CRISPR, og derefter transplanterer de korrigerede celler tilbage i patienten. De første resultater har været yderst lovende og har vist potentialet til at kurere patienter for denne livslange og smertefulde sygdom.
Kræftbehandling
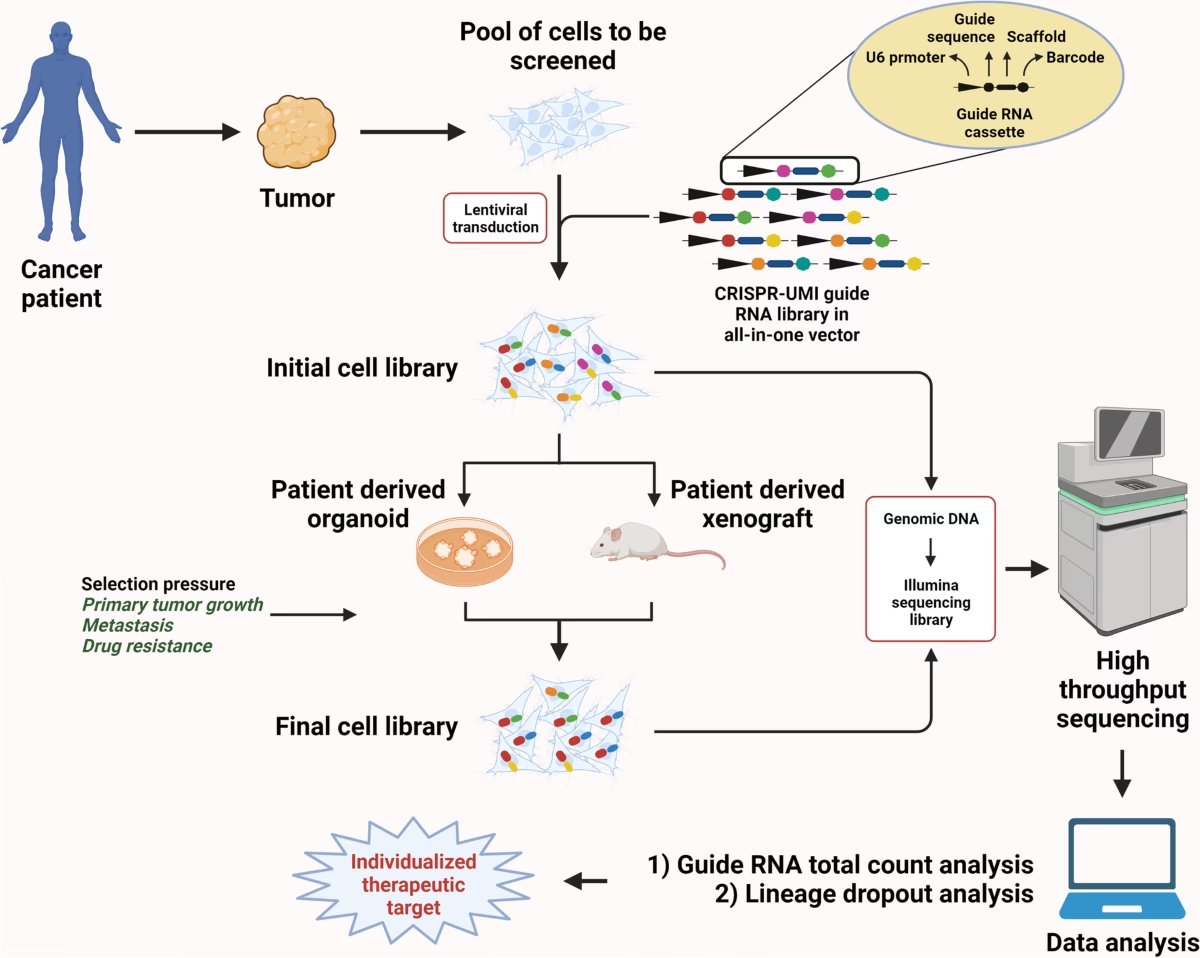
CRISPR er også ved at revolutionere kræftbehandlingen, især inden for immunterapi. En lovende tilgang er CAR-T-celleterapi, hvor en patients egne T-celler (en type immunceller) tages ud, og ved hjælp af gen-redigering omprogrammeres de til at genkende og angribe kræftceller. CRISPR kan gøre denne proces mere effektiv og sikker ved at foretage flere præcise ændringer i T-cellerne på én gang, hvilket forbedrer deres evne til at bekæmpe tumorer og reducerer risikoen for bivirkninger.
Infektionssygdomme
Forskere udforsker også brugen af CRISPR til at bekæmpe infektionssygdomme. For vira som HIV, der integrerer sit eget genetiske materiale i værtscellens DNA, kunne CRISPR teoretisk set bruges til at finde og klippe virus-DNA'et ud af de inficerede celler og dermed fjerne infektionen permanent.
Sammenligning: CRISPR vs. Traditionelle Genterapier
For at forstå, hvorfor CRISPR er så banebrydende, kan det være nyttigt at sammenligne det med ældre former for genterapi.

| Egenskab | CRISPR-Cas9 | Traditionel Genterapi (f.eks. viral vektor) |
|---|---|---|
| Præcision | Meget høj. Kan målrettes mod en specifik DNA-sekvens. | Lavere. Indsætter ofte et nyt gen tilfældigt i genomet, hvilket kan forstyrre andre gener. |
| Funktion | Kan klippe, fjerne, erstatte eller deaktivere gener. Meget alsidig. | Primært designet til at tilføje en funktionel kopi af et defekt gen. |
| Brugervenlighed | Relativt nemt og hurtigt at designe og implementere i et laboratorium. | Kompleks og tidskrævende proces. |
| Omkostninger | Lavere omkostninger til forskning og udvikling. | Typisk meget høje omkostninger. |
Udfordringer og etiske overvejelser
Trods det enorme potentiale er vejen til bred klinisk anvendelse af CRISPR brolagt med betydelige udfordringer og etiske dilemmaer. Sikkerhed er den primære bekymring for forskere og myndigheder.
Off-target effekter
Den største tekniske udfordring er risikoen for 'off-target' effekter. Dette sker, hvis CRISPR-systemet klipper et forkert sted i genomet, altså et sted der ligner målsekvensen, men ikke er identisk. Sådanne utilsigtede klip kan have alvorlige konsekvenser, f.eks. ved at deaktivere et vigtigt gen eller aktivere et kræftfremkaldende gen. Forskere arbejder intenst på at udvikle mere præcise versioner af Cas-enzymer og forbedrede computermodeller for at forudsige og minimere disse risici.
Levering til de rigtige celler
En anden stor udfordring er levering (delivery). Hvordan får man CRISPR-systemet – et relativt stort molekylært kompleks – ind i de specifikke celler eller væv i kroppen, hvor redigeringen er nødvendig? For blodsygdomme er det muligt at tage celler ud, redigere dem og sætte dem tilbage (ex vivo). Men for sygdomme, der påvirker organer som hjernen, hjertet eller lungerne, skal systemet leveres direkte ind i kroppen (in vivo), hvilket er langt mere kompliceret og kræver sofistikerede leveringsmetoder, f.eks. ved hjælp af modificerede vira eller nanopartikler.
Etiske spørgsmål
Ud over de tekniske udfordringer rejser CRISPR dybe etiske spørgsmål. Den mest intense debat omhandler forskellen mellem somatisk og kimlinje-redigering.
- Somatisk redigering: Ændringer foretages i en patients kropsceller (f.eks. blod- eller lungeceller). Disse ændringer påvirker kun den enkelte patient og nedarves ikke. Der er bred enighed om, at dette er et etisk acceptabelt mål for at behandle sygdomme.
- Kimlinje-redigering: Ændringer foretages i kønsceller (sæd- eller ægceller) eller embryoner. Disse ændringer vil blive nedarvet til fremtidige generationer. Dette åbner for muligheden for at udrydde arvelige sygdomme, men også for 'designer-babyer', hvor man potentielt kan vælge egenskaber som intelligens eller udseende. På grund af de uoverskuelige konsekvenser er der et næsten globalt moratorium for klinisk anvendelse af kimlinje-redigering.
Ofte Stillede Spørgsmål (FAQ)
Er CRISPR-behandlinger tilgængelige på hospitaler nu?
Nej, ikke for den brede offentlighed. De fleste CRISPR-baserede behandlinger er stadig på forsknings- eller klinisk forsøgsstadium. Det betyder, at de kun er tilgængelige for en lille, udvalgt gruppe patienter som en del af videnskabelige studier. Der vil sandsynligvis gå flere år, før de første CRISPR-behandlinger bliver godkendt og kommer på markedet.
Er CRISPR 100% sikkert?
Ingen medicinsk behandling er 100% sikker. Som nævnt er den største risiko ved CRISPR 'off-target' effekter, hvor der klippes forkerte steder i DNA'et. Forskere har gjort enorme fremskridt i at forbedre teknologiens præcision, men risikoen kan endnu ikke elimineres fuldstændigt. Sikkerhed er det absolutte hovedfokus i alle kliniske forsøg.
Kan CRISPR bruges til at forbedre mennesker, f.eks. gøre os klogere eller stærkere?
Teoretisk set ja, men dette falder ind under den etisk kontroversielle kategori af kimlinje-redigering og 'human enhancement'. Den globale videnskabelige konsensus er, at teknologien på nuværende tidspunkt udelukkende bør bruges til at behandle alvorlige genetiske sygdomme, ikke til at forbedre normale menneskelige egenskaber. Lovgivningen i de fleste lande forbyder dette.
Hvad er fremtiden for CRISPR?
Fremtiden for CRISPR ser utroligt lys ud. Ud over at behandle sygdomme, bruges teknologien allerede i dag til at accelerere forskning i sygdommes grundlæggende mekanismer, udvikle bedre diagnostiske værktøjer og forbedre landbruget. Inden for medicin forventer vi at se flere og flere kliniske forsøg for en bredere vifte af sygdomme i de kommende år. Teknologien udvikler sig konstant, med nye og forbedrede versioner som 'base editing' og 'prime editing', der tilbyder endnu større præcision og færre risici. CRISPR er ikke bare et værktøj; det er en platform, der vil definere fremtiden for personlig medicin og give håb til millioner af mennesker verden over.
Hvis du vil læse andre artikler, der ligner CRISPR: Fremtidens Gen-redigering er her, kan du besøge kategorien Sundhed.
