04/03/2000
Udviklingen af nye lægemidler er en lang og kompleks proces, hvor sikkerhed er den absolut højeste prioritet. Før et nyt lægemiddel kan testes på mennesker, skal det gennemgå en række grundige prækliniske tests for at vurdere dets potentielle skadelige virkninger. En af de mest centrale dele af denne sikkerhedsvurdering er toksicitetsstudier med gentagen dosis. Disse studier har til formål at karakterisere den toksikologiske profil af et teststof efter gentagen administration over en bestemt periode. Det er her, forskere afdækker, hvordan kroppen reagerer på langvarig eksponering, og identificerer potentielle risici, før de når patienterne.
Hovedformålet med toksicitetsstudier med gentagen dosis
Det primære mål med disse studier er at opbygge et detaljeret billede af, hvordan et stof påvirker en levende organisme over tid. Dette omfatter flere kritiske aspekter:
- Identifikation af målorganer for toksicitet: Hvilke organer (f.eks. lever, nyrer, hjerte) er mest sårbare over for stoffets virkning? Ved at undersøge væv fra forsøgsdyr efter studieperioden kan forskere identificere specifikke organskader.
- Analyse af eksponerings- og responsforhold: Studierne hjælper med at fastslå, hvordan toksiciteten ændrer sig med forskellige doser. Dette er afgørende for at bestemme et sikkert dosisniveau. Man finder frem til det såkaldte NOAEL (No Observed Adverse Effect Level), som er den højeste dosis, hvor der ikke observeres nogen skadelige virkninger. Denne værdi er fundamental for at beregne den startdosis, der skal bruges i kliniske forsøg med mennesker.
- Vurdering af reversibilitet: Hvis der observeres toksiske effekter, er det vigtigt at vide, om de er permanente eller reversible. Forsvinder skaderne, når administrationen af stoffet ophører? Dette undersøges ofte ved hjælp af en "satellitgruppe" af dyr, der observeres i en periode efter, at behandlingen er stoppet.
En kort historisk rejse gennem toksikologien
Videnskaben om giftstoffer, toksikologi, har rødder, der går århundreder tilbage. En af pionererne var Paracelsus (1493–1541), der berømt sagde: "Alle ting er gift, og intet er uden gift; alene dosis gør, at en ting ikke er en gift." Dette princip om dosis-respons er stadig en grundsten i moderne toksikologi.
I midten af det 20. århundrede blev systematisk toksicitetstestning mere formaliseret. Indførelsen af LD50-testen (den dosis, der er dødelig for 50% af en testpopulation) og Draize-testen for hud- og øjenirritation var tidlige skridt. En tragisk begivenhed i 1960'erne, thalidomid-skandalen, hvor tusindvis af børn blev født med misdannelser, blev et vendepunkt. Det førte til en markant stramning af kravene til lægemiddelsikkerhed og etableringen af internationale retningslinjer fra organisationer som OECD (Organisation for Economic Co-operation and Development) og ICH (International Conference on Harmonisation).
Forskellige typer af toksicitetsstudier
Toksicitetsstudier kan opdeles efter varigheden og formålet med eksponeringen. Hver type test giver unik information om et stofs sikkerhedsprofil.
Akut toksicitetstestning
Dette er den første test, der udføres. Den undersøger effekten af en enkelt, høj dosis af et stof. Forsøgsdyrene, typisk en gnaver- og en ikke-gnaversart, observeres i 14 dage for tegn på toksicitet og dødelighed. Formålet er ikke længere primært at bestemme LD50 på grund af det høje antal dyr, det kræver. I stedet anvendes mere raffinerede metoder som:
- Fixed Dose Procedure (FDP): Vurderer ikke-dødelig toksicitet ved faste doser.
- Acute Toxic Category (ATC): En trinvis metode, der bruger færre dyr.
- Up-and-Down Procedure (UDP): En sekventiel metode, der yderligere reducerer antallet af anvendte dyr.
Studier med gentagen dosis (subakut, subkronisk og kronisk)
Disse studier er designet til at efterligne den måde, mennesker ofte bruger medicin på – dagligt over en længere periode. De adskiller sig primært i varighed:
| Testtype | Varighed | Primært formål |
|---|---|---|
| Gentagen dosis (Subakut) | Typisk 28 dage | Identificere målorganer for toksicitet og fastlægge NOAEL for kortere tids eksponering. |
| Subkronisk | Typisk 90 dage | Vurdere toksiske effekter og dosis-respons over en mellemlang periode. Giver data til længerevarende kliniske forsøg. |
| Kronisk | 6 måneder til 2 år (eller længere) | Evaluere de langsigtede sundhedseffekter ved kronisk eksponering, herunder potentialet for kræftudvikling. |
Under disse studier overvåges dyrene nøje for ændringer i vægt, adfærd, blodkemi og generel sundhed. Efter studiets afslutning aflives dyrene humant, og deres organer og væv undersøges grundigt histopatologisk (under mikroskop) for at identificere eventuelle skader.
Specialiserede toksikologiske undersøgelser
Ud over de generelle toksicitetsstudier findes der en række specialiserede tests, der undersøger specifikke risici.
Karcinogenicitetstest
Disse langvarige studier (ofte 2 år for rotter) har til formål at afgøre, om et stof kan forårsage kræft. Testen er afgørende for lægemidler, der er beregnet til langvarig eller livslang behandling. Dette er en undersøgelse af et stofs karcinogenicitet.
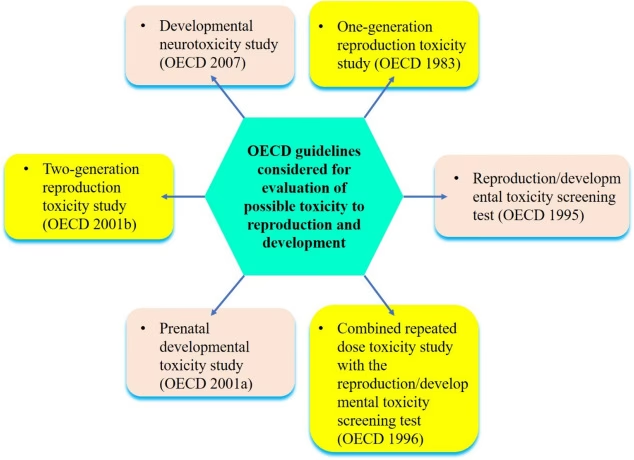
Reproduktionstoksicitet og udviklingstoksicitet
Disse studier undersøger, om et stof påvirker forplantningsevnen eller skader et foster under udvikling. Reproduktionstoksicitet vurderes ofte i en- eller to-generationsstudier, hvor man ser på effekter på fertilitet, parring, graviditet og afkommets sundhed. Udviklingstoksicitetsstudier fokuserer specifikt på eksponering under graviditeten for at identificere risikoen for fødselsdefekter.

Genotoksicitet
Genotoksicitet er et stofs evne til at beskadige genetisk materiale (DNA). Disse tests udføres ofte *in vitro* (i reagensglas) på bakterier eller pattedyrceller, men kan også udføres *in vivo* (i levende dyr). Et positivt resultat kan indikere en potentiel risiko for kræft eller arvelige sygdomme.
Etiske overvejelser og fremtidens toksikologi
Brugen af dyr i forskning er underlagt streng lovgivning og etiske retningslinjer. Alle dyreforsøg skal godkendes af et dyreetisk udvalg, og forskere er forpligtet til at følge principperne om de 3 R'er:
- Replacement (Erstatning): At erstatte dyreforsøg med alternativer, når det er muligt (f.eks. cellekulturer, computersimuleringer).
- Reduction (Reduktion): At bruge det mindst mulige antal dyr til at opnå statistisk valide resultater.
- Refinement (Forfinelse): At forbedre metoderne for at minimere smerte, lidelse og stress for dyrene.
Fremtiden inden for toksikologi bevæger sig i retning af flere avancerede *in vitro*-modeller, såsom organ-on-a-chip-teknologier og komplekse computermodeller, der kan forudsige toksicitet med større præcision og færre dyreforsøg. Disse metoder vil dog i overskuelig fremtid supplere, snarere end fuldstændigt erstatte, dyreforsøg, da det stadig er nødvendigt at forstå, hvordan et stof opfører sig i en hel, kompleks organisme.
Ofte Stillede Spørgsmål (FAQ)
Hvorfor bruges dyr stadig i toksicitetstest?
Selvom alternative metoder udvikles konstant, kan de endnu ikke fuldt ud efterligne den komplekse interaktion mellem organer i en levende krop. Dyreforsøg er i øjeblikket den mest pålidelige måde at vurdere den systemiske effekt af et nyt lægemiddel og er et lovkrav i de fleste lande for at sikre menneskers sikkerhed.
Hvad er "No Observed Adverse Effect Level" (NOAEL)?
NOAEL er den højeste dosis af et stof, der er blevet testet i et dyrestudie, hvor der ikke blev observeret nogen statistisk eller biologisk signifikante skadelige virkninger. Denne værdi bruges som et afgørende udgangspunkt for at fastsætte en sikker dosis for de første kliniske forsøg på mennesker.
Er alle stoffer, der er giftige for dyr, også giftige for mennesker?
Ikke nødvendigvis. Der er biologiske forskelle mellem arter. Resultater fra dyrestudier kan dog give en stærk indikation af potentielle risici. Forskere bruger komplekse modeller til at "oversætte" eller ekstrapolere data fra dyr til mennesker, men den endelige sikkerhed kan kun fastslås gennem forsigtigt designede kliniske forsøg.
Hvad sker der med dyrene efter et forsøg?
Efter afslutningen af et toksicitetsstudie bliver dyrene humant aflivet. Dette er en nødvendig del af processen, da en detaljeret undersøgelse af deres indre organer og væv (histopatologi) er afgørende for at identificere eventuelle toksiske effekter, der ikke var synlige, mens dyret var i live.
Hvis du vil læse andre artikler, der ligner Toksicitetsstudier med gentagen dosis forklaret, kan du besøge kategorien Sundhed.
