08/11/2013
Vores krop er i en konstant kamp mod usynlige fjender som bakterier. Når vi udsættes for en infektion, især fra gramnegative bakterier, iværksætter vores immunforsvar en række komplekse forsvarsmekanismer. En af de mest centrale spillere i denne proces er et protein kaldet CD14. Selvom det måske ikke er et velkendt navn for de fleste, er dets rolle som en frontlinjesensor og regulator afgørende for, hvordan vores krop opdager og reagerer på bakterielle trusler. At forstå CD14 er at forstå en fundamental del af, hvordan inflammation starter, og hvorfor denne proces nogle gange kan løbe løbsk og føre til livstruende tilstande som sepsis.
Hvad er CD14 og LPS?
For at forstå CD14's funktion, skal vi først kende dets modpart: Lipopolysaccharid, bedre kendt som LPS. LPS er en essentiel komponent i ydermembranen af gramnegative bakterier, som f.eks. E. coli. Når disse bakterier invaderer kroppen, fungerer LPS som et kraftigt signalstof – et såkaldt endotoksin – der advarer immunsystemet om en igangværende infektion. Det er her, CD14 kommer ind i billedet.
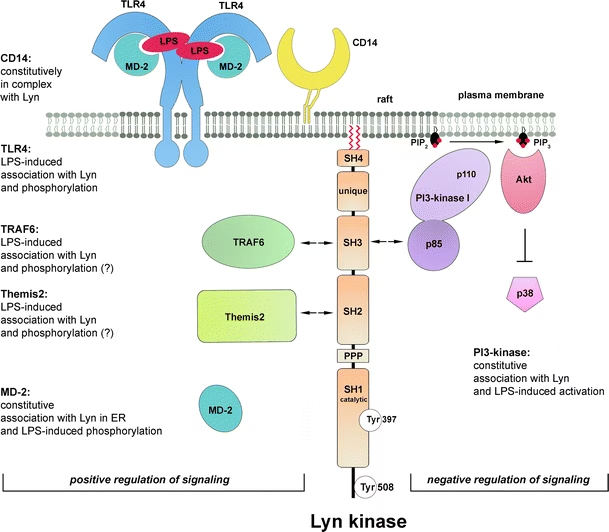
CD14 er en receptor, der findes på overfladen af immunceller, især makrofager og monocytter. Dets primære opgave er at genkende og binde sig til LPS. Man kan forestille sig CD14 som en vagtpost, der patruljerer celleoverfladen. Når den opdager LPS-molekyler, griber den fat i dem og præsenterer dem for en anden, endnu vigtigere receptor-kompleks: Toll-like receptor 4 (TLR4) og dets co-receptor MD-2. Det er denne overdragelse fra CD14 til TLR4, der for alvor starter den inflammatoriske kaskade.
CD14: Mere end blot en passiv hjælper
I mange år blev CD14 primært betragtet som en molekylær 'postbud', hvis eneste rolle var at koncentrere og levere LPS til TLR4. Forskning har dog afsløret, at dets rolle er langt mere aktiv og nuanceret. Studier på mus har været afgørende for at belyse dette. Mus, der genetisk var modificeret til at mangle CD14, udviklede ikke septisk chok, selv når de blev udsat for dødelige doser af LPS. Deres blod ophobede ikke de pro-inflammatoriske cytokiner (signalproteiner), som normalt driver den voldsomme reaktion. Omvendt var mus, der var modificeret til at udtrykke ekstra meget humant CD14, overfølsomme over for LPS.
Disse resultater viser, at CD14 ikke blot er en hjælper, men en afgørende forstærker af den inflammatoriske respons. Uden CD14 er TLR4-signaleringen markant svagere og langsommere. Dette er en fordel ved lokale infektioner, hvor en hurtig og kraftig reaktion er nødvendig for at bekæmpe invaderende bakterier. Men under en systemisk infektion, hvor bakterier er i blodet, kan denne CD14-drevne forstærkning blive fatal og føre til den overdrevne inflammation, der kendetegner sepsis.
To Signalveje: MyD88 og TRIF
Når TLR4 aktiveres af LPS, udløser det to primære signalveje inde i cellen. Disse veje fører til produktionen af forskellige typer inflammatoriske molekyler. At forstå disse to veje er nøglen til at forstå CD14's komplekse rolle.
- MyD88-afhængig vej: Dette er den 'klassiske' og hurtige vej. Den fører til aktivering af NF-κB og MAP-kinaser, hvilket resulterer i en hurtig produktion af pro-inflammatoriske cytokiner som TNF-α og IL-1β. Disse er de molekyler, der skaber de velkendte symptomer på inflammation som feber og hævelse.
- TRIF-afhængig vej: Denne vej er lidt langsommere og fører til aktivering af IRF3, hvilket resulterer i produktionen af type I interferoner. Disse molekyler er vigtige for det antivirale forsvar, men spiller også en rolle i den bakterielle respons.
Nyere forskning har vist, at CD14 er specielt afgørende for aktiveringen af den TRIF-afhængige vej. Studier på mus med en mutation i CD14-genet viste, at mens MyD88-vejen i nogle tilfælde kunne aktiveres uden CD14, var TRIF-vejen fuldstændig afhængig af et funktionelt CD14-protein. Dette peger på, at CD14 har en specifik funktion, der går ud over blot at levere LPS.
Glat vs. Ru LPS: En Vigtig Strukturel Forskel
Ikke alt LPS er ens. Bakterier kan producere forskellige former, primært klassificeret som 'glat' (sLPS) og 'ru' (rLPS). Forskellen ligger i en lang polysakkaridkæde (O-antigenet), som sLPS har, men rLPS mangler. Denne strukturelle forskel har stor betydning for, hvordan immunsystemet reagerer, og hvor afhængig responsen er af CD14.
sLPS, med sin lange 'hale', er stærkt afhængig af CD14 for at kunne aktivere TLR4 effektivt. Uden CD14 er sLPS meget dårlig til at starte en inflammatorisk respons. rLPS, derimod, er mere hydrofobisk (vandafvisende) på grund af den manglende sukkerkæde. Dette gør det i stand til, især ved høje koncentrationer, at interagere mere direkte med cellemembranen og aktivere TLR4 uden hjælp fra CD14. Dog er responsen stadig svagere end med CD14's hjælp.
Sammenligning af Glat og Ru LPS
| Egenskab | Glat LPS (sLPS) | Ru LPS (rLPS) |
|---|---|---|
| Struktur | Har en lang O-polysakkaridkæde. | Mangler O-polysakkaridkæden. |
| Afhængighed af CD14 | Meget høj. Kræver CD14 for effektiv signalering. | Lavere. Kan aktivere TLR4 direkte ved høje koncentrationer. |
| Aktivering af TRIF-vej | Fuldt afhængig af CD14. | Kan ved høje doser aktivere TRIF-vejen uden CD14. |
| Hydrofobicitet | Lavere. | Højere, hvilket letter interaktion med cellemembranen. |
Internaliseringsprocessen: Nøglen til TRIF-signalering
Den afgørende rolle, CD14 spiller for TRIF-vejen, er tæt knyttet til en proces kaldet endocytose – det vil sige, at TLR4-receptoren bliver trukket ind i cellen, efter den har bundet sig til LPS. Forskning viser, at MyD88-signaleringen primært sker fra celleoverfladen, mens TRIF-signaleringen først aktiveres, når TLR4-komplekset er inde i cellen i små blærer kaldet endosomer.
CD14 er dirigenten for denne internaliseringsproces. Studier har vist, at i celler, der mangler CD14, forbliver TLR4 på celleoverfladen efter LPS-stimulering, og TRIF-vejen aktiveres aldrig. CD14 ser ud til at igangsætte en specifik type endocytose kaldet makropinocytose. Denne proces involverer en række andre proteiner og en omorganisering af cellens skelet, hvilket fører til, at en del af cellemembranen med LPS/CD14/TLR4-komplekset bliver opslugt. Det er denne CD14-kontrollerede bevægelse fra overfladen til cellens indre, der er den fysiske mekanisme bag skiftet fra MyD88- til TRIF-signalering.
Afsluttende bemærkninger
Proteinet CD14 er langt mere end en simpel 'leverandør' af bakterielle signaler. Det er en sofistikeret og essentiel regulator af vores medfødte immunrespons. Ved at genkende LPS, forstærke signaleringen og styre den rumlige placering af TLR4-receptoren, dikterer CD14 både styrken og typen af den inflammatoriske reaktion. Selvom denne funktion er livsvigtig for at bekæmpe lokale infektioner, er den også en akilleshæl, der kan føre til den ødelæggende og ukontrollerede inflammation, der ses ved sepsis. Fortsat forskning i de præcise mekanismer, hvorved CD14 fungerer, er derfor afgørende for udviklingen af nye behandlinger rettet mod at modulere immunresponset og forhindre de fatale konsekvenser af systemiske infektioner.
Ofte Stillede Spørgsmål (FAQ)
Er CD14 altid pro-inflammatorisk og 'dårligt'?
Nej, CD14's pro-inflammatoriske rolle er fundamental for et effektivt immunforsvar. Det er den hurtige og kraftige reaktion, som CD14 muliggør, der gør os i stand til at bekæmpe de fleste infektioner, før de bliver alvorlige. Problemet opstår, når infektionen bliver systemisk (i hele kroppen), og denne normalt beskyttende mekanisme løber løbsk og forårsager skade på kroppens egne væv.
Hvad sker der, hvis man mangler CD14?
Som vist i dyreforsøg, medfører en mangel på CD14 en markant nedsat følsomhed over for LPS. Dette beskytter mod septisk chok, men det betyder også, at den indledende immunrespons på en lokal infektion er svagere. Det kan potentielt gøre en person mere sårbar over for at nedkæmpe infektioner i første omgang.
Hvorfor er der forskel på, hvordan kroppen reagerer på 'glat' og 'ru' LPS?
Det skyldes deres fysiske og kemiske forskelle. 'Glat' LPS med sin lange sukkerkæde har brug for CD14 til at blive 'præsenteret' korrekt for TLR4. 'Ru' LPS er mere 'nøgent' og hydrofobisk, hvilket gør det i stand til lettere at interagere direkte med fedtstofferne i cellemembranen, og dermed kan det i nogle tilfælde aktivere TLR4 uden hjælp fra CD14.
Hvis du vil læse andre artikler, der ligner CD14: Nøglen til kroppens inflammationsrespons, kan du besøge kategorien Sundhed.
