04/05/2020
Kliniske forsøg er hjørnestenen i moderne medicin og en afgørende motor for udviklingen af nye og forbedrede behandlinger. De udgør den proces, hvorved forskere og læger kan afgøre, om en ny medicin, en ny kirurgisk procedure eller en anden form for behandling er både sikker og mere effektiv end de eksisterende muligheder. Uden disse omhyggeligt planlagte og etisk overvågede studier ville fremskridt inden for sundhedssektoren gå i stå. Denne artikel vil guide dig igennem, hvad et klinisk forsøg er, hvordan det udføres, og hvad der er vigtigt at vide, uanset om du er patient, pårørende eller sundhedsprofessionel.
Hvad er et klinisk forsøg helt præcist?
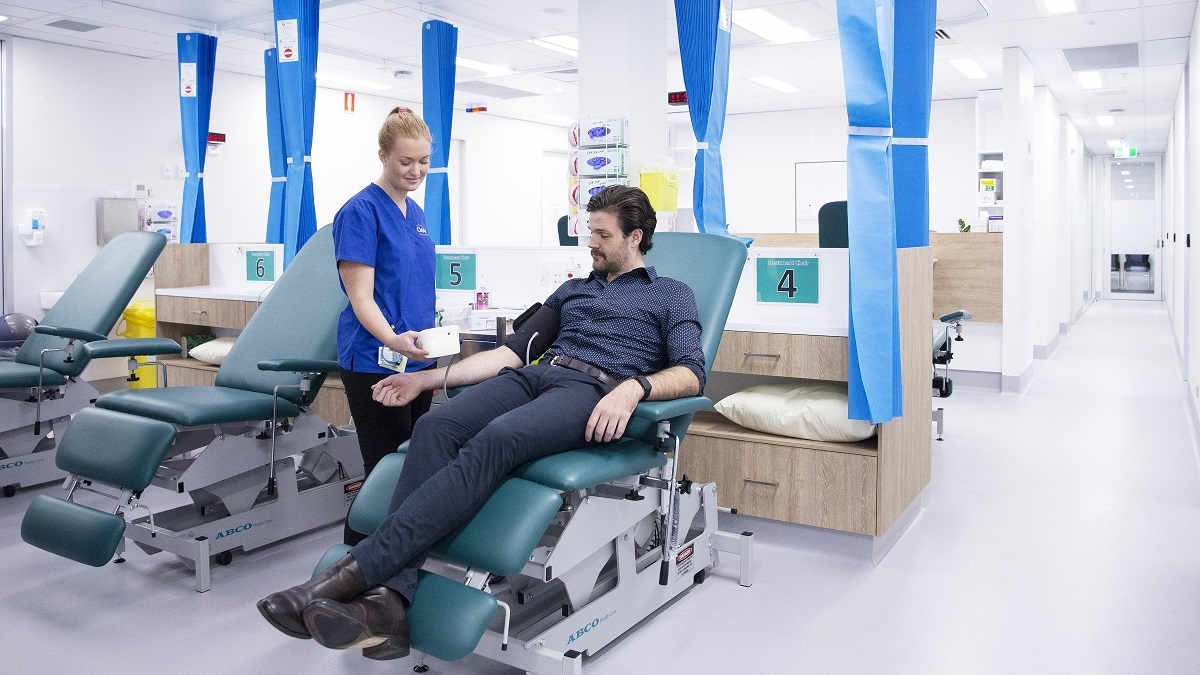
Et klinisk forsøg er et forskningsprojekt, der udføres på mennesker med det formål at evaluere en medicinsk, kirurgisk eller adfærdsmæssig intervention. Det er den primære måde, hvorpå forskere finder ud af, om en ny behandling, som f.eks. et nyt lægemiddel, en diæt eller et medicinsk udstyr, er sikker og effektiv for mennesker. Ofte sammenligner et klinisk forsøg en ny behandling med en standardbehandling, en placebo (en inaktiv substans) eller slet ingen intervention. Resultaterne fra disse forsøg genererer evidens af høj kvalitet, som danner grundlag for lægers beslutninger og patienters behandlingsvalg.
Interventionen, der undersøges, kan være mange ting:
- Et nyt lægemiddel eller en ny kombination af lægemidler.
- En ny kirurgisk procedure eller et nyt medicinsk udstyr.
- En ny måde at anvende en eksisterende behandling på.
- En ny metode til at ændre adfærd for at forbedre sundheden, f.eks. en ny diæt eller et træningsprogram.
Kliniske forsøg er en essentiel del af processen for evidensbaseret praksis og er afgørende for, at nye lægemidler kan opnå godkendelse fra sundhedsmyndighederne, som f.eks. Lægemiddelstyrelsen i Danmark, og blive tilgængelige for patienter.
Hvordan bliver man involveret i kliniske forsøg?
For patienter, der ønsker at deltage, eller forskere, der ønsker at starte et forsøg, er der flere veje at gå. Kliniske forsøg udføres bredt i det danske sundhedsvæsen, og forsknings- og udviklingsafdelingen på dit lokale hospital vil have en oversigt over alle aktive kliniske forsøg. Mange forsøg er også registreret i nationale og internationale databaser, som er søgbare og kan identificere forsøg inden for specifikke sygdomme eller med specifikke behandlinger. Eksempler på sådanne databaser er ClinicalTrials.gov og WHO's International Clinical Trials Registry Platform.
Mange kliniske forsøg, især dem, der involverer et nyt lægemiddel eller foregår på tværs af flere hospitaler, styres af en 'Clinical Trials Unit' (CTU) eller en 'Contract Research Organisation' (CRO). Disse organisationer specialiserer sig i design, ledelse og analyse af kliniske forsøg og kan være et godt kontaktpunkt for information om igangværende forskning i dit område.
Processen: Hvad indebærer det at udføre et klinisk forsøg?
At gennemføre et klinisk forsøg er en kompleks og omhyggeligt reguleret proces, der kræver minutiøs planlægning og involvering af et tværfagligt team. Processen kan opdeles i flere faser:
1. Idé og design
Et klinisk forsøg bør overvejes, når der er reel usikkerhed om, hvilken af flere behandlingsmuligheder eller forebyggende strategier der er mest effektiv. Når behovet for et nyt forsøg er fastslået på et medicinsk, etisk og økonomisk grundlag, skal selve forsøget designes. Dette er en multidisciplinær aktivitet, der kræver input fra klinikere, forsøgsmetodologer, farmaceuter, statistikere og sundhedsøkonomer for at sikre, at forsøget vil levere evidens af højest mulig kvalitet.
2. Finansiering og godkendelser
Når forsøget er designet, skal der findes finansiering. Midlerne kan komme fra medicinalindustrien, som finansierer forsøg som en del af udviklingen af et nyt produkt, eller fra offentlige forskningsfonde og private velgørenhedsorganisationer som f.eks. Kræftens Bekæmpelse eller Hjerteforeningen. Efter sikring af finansiering skal alle nødvendige tilladelser indhentes, herunder godkendelse fra De Videnskabsetiske Komitéer og tilladelse fra Lægemiddelstyrelsen, hvis der testes medicin.
3. Uddannelse og udførelse
Alle involverede i forsøget skal have træning i de juridiske og etiske ansvarsområder. Dette sker ofte gennem kurser i 'Good Clinical Practice' (GCP), som er en international standard for kvalitet i design, udførelse, registrering og rapportering af kliniske forsøg. Selve udførelsen indebærer rekruttering af deltagere, administration af behandlingen og omhyggelig indsamling af data.
Er et klinisk forsøg altid den rette løsning?
Før man påbegynder et klinisk forsøg, er det afgørende at fastslå, om et nyt forsøg er nødvendigt. Man skal undersøge, hvilken forskning der allerede er udført. Findes der eksisterende forsøg, der kan give tilstrækkelig evidens til at besvare det spørgsmål, man ønsker at adressere? Forskningsfonde er forpligtede til at undgå spild i forskning, og en unødvendig gentagelse af et forsøg vil sandsynligvis ikke blive finansieret.
Det anbefales, at alle kliniske forsøg starter med et systematisk review af den eksisterende forskning. Dette kan afsløre, at der allerede er tilstrækkelig evidens til at besvare forskningsspørgsmålet, eller det kan levere solid information til at retfærdiggøre og hjælpe med designet af det nye forsøg.
Der findes også andre forskningsmuligheder, som kan være mere passende i visse situationer.
Sammenligning af forskningstyper
| Type af studie | Formål | Hvornår det er passende |
|---|---|---|
| Klinisk Forsøg | At sammenligne effektiviteten af to eller flere interventioner. | Når der er reel usikkerhed om den bedste behandling, og der er tilstrækkelig forhåndsviden til at retfærdiggøre et forsøg. |
| Pilotstudie | At vurdere gennemførligheden af et større klinisk forsøg. | Før et stort og dyrt forsøg for at teste procedurer, rekrutteringsstrategier og beregne nødvendig stikprøvestørrelse. |
| Observationsstudie | At observere sammenhænge og resultater uden at gribe ind. | Når der er usikkerhed om de mest robuste effektmål, eller når mekanismen bag en potentiel ny behandling ikke er fastlagt. |
Tidsramme og almindelige faldgruber
Tiden, der kræves for at designe et klinisk forsøg, udarbejde den detaljerede forsøgsprotokol og sikre alle tilladelser, er betydelig og kan let tage 6-12 måneder. Tiden, der kræves for at udføre selve forsøget, vil variere meget og afhænger af den nødvendige stikprøvestørrelse, hvor hurtigt deltagere kan rekrutteres, og opfølgningsperioden for hver deltager.
Selv med den bedste planlægning er der flere potentielle faldgruber:
- Underskrevet tidsforbrug: Mange undervurderer den tid, det tager at udvikle protokollen og få alle godkendelser på plads, før forsøget kan starte.
- Rekrutteringsproblemer: Manglende evne til at rekruttere deltagere inden for den fastsatte tidsramme er en betydelig faldgrube. Det er en risiko at overvurdere, hvor let specifikke patientgrupper vil være villige til at deltage, hvilket kan føre til urealistiske tidsplaner.
- Alvorlige uønskede hændelser: Omhyggelig overvågning for alvorlige bivirkninger er essentiel. Hvis sådanne hændelser opstår, vil de blive gennemgået af den etiske komité og af en uafhængig dataovervågningskomité, som har beføjelse til at stoppe et studie tidligt, hvis der er mistanke om, at den undersøgte intervention forårsager skade.
Ofte Stillede Spørgsmål (FAQ)
Hvor lang tid tager et klinisk forsøg?
Det varierer meget. Forberedelsesfasen med design og godkendelser tager typisk 6-12 måneder. Selve forsøgets varighed kan strække sig fra få måneder til mange år, afhængigt af sygdommen, antallet af deltagere og længden af opfølgningsperioden.
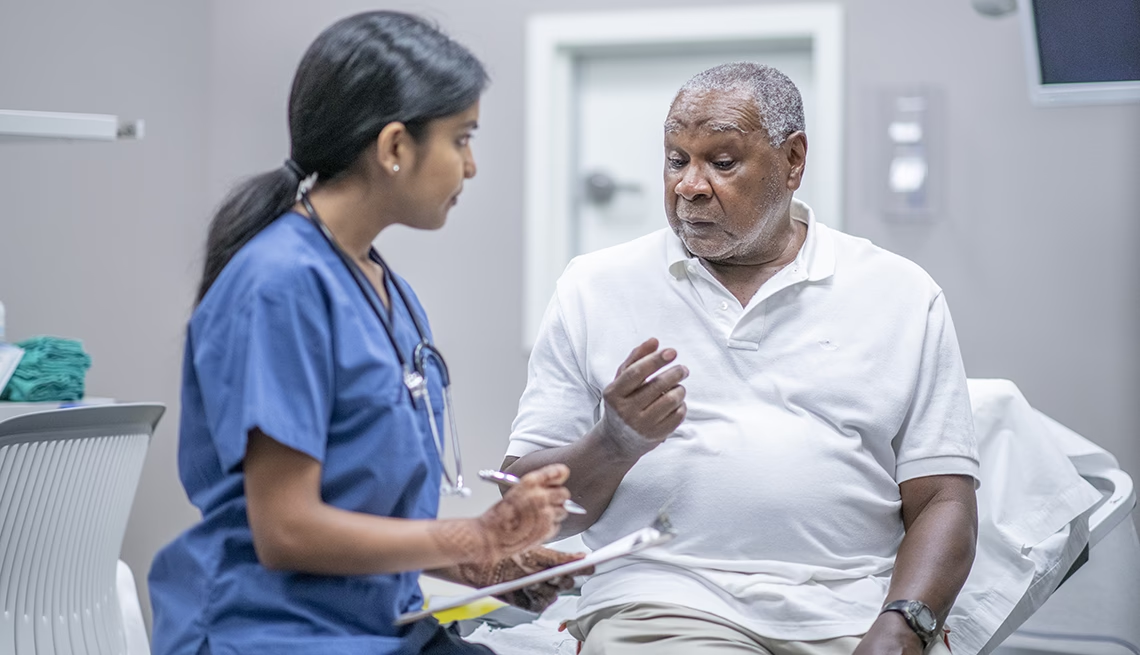
Hvem kan deltage i et klinisk forsøg?
Hvert forsøg har specifikke kriterier for, hvem der kan deltage (inklusions- og eksklusionskriterier). Disse kriterier kan omfatte alder, køn, sygdomstype og -stadie samt tidligere behandlingshistorik. Formålet er at sikre, at forskerne kan besvare deres spørgsmål korrekt og beskytte deltagerne.
Er det sikkert at deltage i et klinisk forsøg?
Sikkerhed er den højeste prioritet. Alle kliniske forsøg skal godkendes af en videnskabsetisk komité, der vurderer, om forsøget er etisk forsvarligt, og om potentielle risici er acceptable i forhold til de forventede fordele. Deltagerne overvåges nøje for bivirkninger under hele forsøget.
Hvad er forskellen på et lægemiddel under udvikling og et godkendt lægemiddel?
Et lægemiddel under udvikling er endnu ikke godkendt af sundhedsmyndighederne til almindelig brug. Dets sikkerhed og effektivitet er stadig ved at blive undersøgt i kliniske forsøg. Et godkendt lægemiddel har gennemgået denne proces og er blevet vurderet til at have en positiv balance mellem fordele og risici for en specifik patientgruppe.
Afslutningsvis er kliniske forsøg en uundværlig, omend kompleks, del af medicinsk forskning. De bygger bro mellem videnskabelige opdagelser i laboratoriet og bedre behandlinger for patienter i den virkelige verden, og sikrer, at fremtidens medicin er baseret på solid og pålidelig evidens.
Hvis du vil læse andre artikler, der ligner Kliniske forsøg: Din komplette guide, kan du besøge kategorien Sundhed.