28/11/2017
Den Stille Revolution inden for Helbredelse: Ekstracellulære Vesikler
Inden for moderne medicin udgør regenerativ medicin et af de mest lovende og hurtigst voksende felter. Målet er at reparere, erstatte eller regenerere beskadigede celler, væv eller organer for at genoprette normal funktion. I årtier har fokus primært været på brugen af stamceller – kroppens egne mesterbyggere – til at opnå dette. Men en ny og spændende spiller er trådt ind på scenen: ekstracellulære vesikler (EV'er). Disse mikroskopiske partikler, som engang blev betragtet som cellulært affald, viser sig nu at være afgørende kommunikationsværktøjer mellem celler og kan potentielt tilbyde mange af de samme fordele som celleterapi, men uden nogle af de tilknyttede risici. Denne artikel dykker ned i verdenen af EV'er, deres terapeutiske potentiale, og hvordan de sammen med stamcelleterapier former fremtiden for behandling af sygdomme.
Hvad er Ekstracellulære Vesikler (EV'er)?
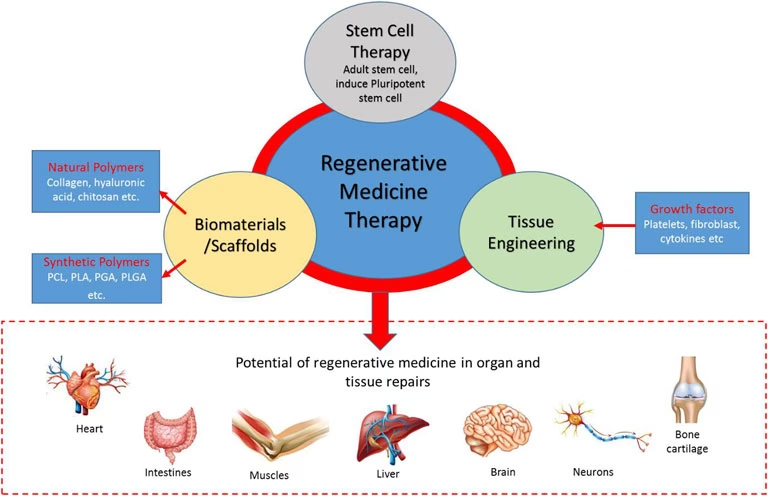
Ekstracellulære vesikler er en samlebetegnelse for små, membran-indkapslede partikler, der naturligt frigives fra næsten alle celletyper i kroppen. De fungerer som små postpakker, der transporterer en last af proteiner, lipider og genetisk materiale (som mRNA og miRNA) fra en celle til en anden. Denne proces, kendt som intercellulær kommunikation, er afgørende for at koordinere komplekse biologiske processer, både i en sund krop og under sygdom.
EV'er kan groft inddeles i tre hovedkategorier baseret på, hvordan de dannes:
- Exosomer (50-150 nm): Disse dannes inde i cellen i en struktur kaldet multivesikulære legemer (MVB'er). Når MVB'erne smelter sammen med cellens ydre membran, frigives exosomerne til det ekstracellulære miljø.
- Mikrovesikler (100-1000 nm): Disse er større end exosomer og dannes ved direkte udposning eller 'afknopning' fra cellens overflademembran.
- Apoptotiske legemer (over 500 nm): Disse frigives fra celler, der gennemgår programmeret celledød (apoptose).
På grund af overlap i størrelse og den tekniske udfordring ved at skelne præcist mellem dem, anvendes den overordnede betegnelse ekstracellulære vesikler (EV'er) i stigende grad. Deres last afhænger fuldstændigt af oprindelsescellen og dens tilstand. En stamcelle vil frigive EV'er med et regenerativt og anti-inflammatorisk indhold, mens en kræftcelle vil frigive EV'er, der fremmer sygdommens spredning. Det er netop denne evne til at afspejle deres oprindelse, der gør dem så interessante som både diagnostiske markører og terapeutiske værktøjer.
EV'er som Terapeutiske Værktøjer: Acellulær Regenerativ Medicin
Forskning har vist, at mange af de positive virkninger, der observeres ved stamcelleterapi, ikke nødvendigvis skyldes, at stamcellerne selv integreres og danner nyt væv. I stedet stammer effekten i høj grad fra de stoffer, stamcellerne udskiller – en såkaldt parakrin effekt. EV'er er en central del af denne effekt. Dette har ført til udviklingen af acellulære terapier, hvor man i stedet for at transplantere hele celler, anvender de EV'er, de producerer. Denne tilgang har flere potentielle fordele: lavere risiko for immunafstødning, ingen risiko for dannelse af tumorer (teratomer), og lettere produktion og opbevaring.
Potentiale inden for specifikke sygdomsområder:
1. Heling af Hudsår
Heling af komplekse hudsår, f.eks. fra forbrændinger eller hos diabetikere, er en kompliceret proces. EV'er, især dem fra mesenkymale stamceller (MSC'er), har vist et bemærkelsesværdigt potentiale til at fremme alle faser af sårheling. De kan dæmpe den indledende inflammatoriske reaktion ved at påvirke immunceller (makrofager) til at skifte fra en pro-inflammatorisk til en anti-inflammatorisk, helende tilstand. Derudover stimulerer de hudceller (keratinocytter og fibroblaster) til at dele sig og migrere, øger produktionen af kollagen, og fremmer dannelsen af nye blodkar (angiogenese). Forskere eksperimenterer med at indarbejde EV'er i bandager og hydrogeler for at sikre en vedvarende og lokal frigivelse direkte i såret.

2. Reparation af Hjertet
Efter en blodprop i hjertet (myokardieinfarkt) dør en del af hjertemuskulaturen, hvilket efterlader arvæv og nedsat hjertefunktion. Studier i dyremodeller har vist, at administration af EV'er fra hjerte- eller stamceller kan reducere skadens omfang markant. EV'erne beskytter de overlevende hjertemuskelceller mod celledød, reducerer inflammation og fibrose (arvævsdannelse) og stimulerer dannelsen af nye blodkar for at forbedre blodforsyningen til det beskadigede område. Dette fører samlet set til en forbedret hjertefunktion. Ligesom med hudsår undersøges muligheden for at levere EV'er via et 'plaster' af biomateriale, der kan sutureres direkte på hjertet for en langvarig effekt.
3. Behandling af Øjensygdomme
I øjensygdomme som retinitis pigmentosa (RP) og aldersrelateret makuladegeneration (AMD), hvor de lysfølsomme celler (fotoreceptorer) går tabt, kan EV'er spille en vigtig rolle. Forskning tyder på, at EV'er kan beskytte fotoreceptorerne ved at dæmpe den skadelige inflammation i nethinden, som driver sygdomsprogressionen. De kan også reducere unormal blodkardannelse, som er et kendetegn ved 'våd' AMD. Ved at levere EV'er tidligt i sygdomsforløbet håber man at kunne bremse eller stoppe tabet af syn, hvilket potentielt kan udskyde behovet for mere invasive celletransplantationer.
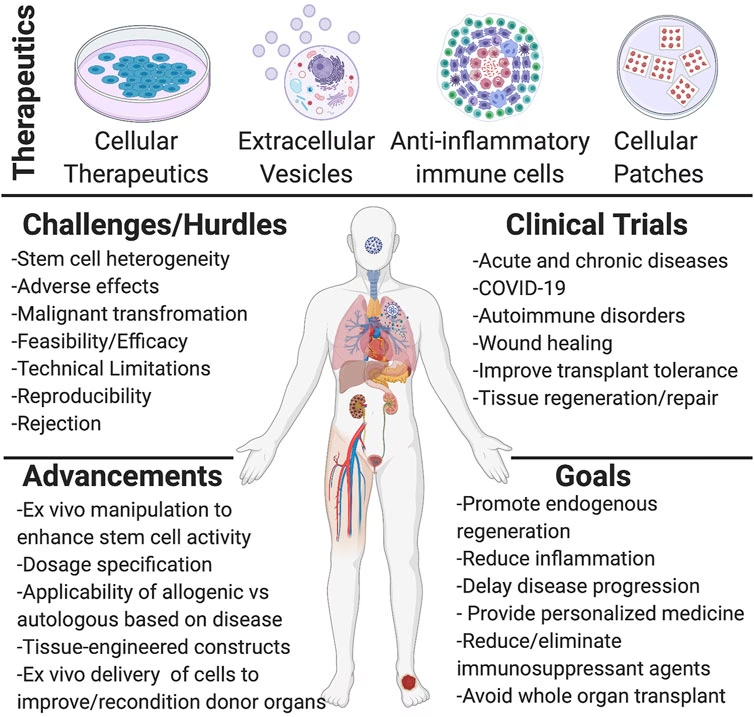
Udfordringer ved Celletansplantation og Fremtidens Løsninger
Selvom acellulær EV-terapi er lovende, er traditionel stamcelle-baseret regenerativ medicin stadig afgørende, især når hele celler skal erstattes. Den største hindring for succesfuld transplantation af celler fra en donor (allogen transplantation) er immunafstødning. Modtagerens immunsystem genkender de transplanterede celler som fremmede og angriber dem. Forskere arbejder på flere fronter for at overvinde denne udfordring.
Strategier til at Undgå Immunafstødning
| Strategi | Beskrivelse | Fordele og Ulemper |
|---|---|---|
| Immunsuppressive Lægemidler | Standardbehandling, hvor patienten modtager medicin, der dæmper hele immunsystemet for at forhindre afstødning. | Fordel: Velkendt og effektivt. Ulempe: Alvorlige bivirkninger, herunder øget risiko for infektioner, kræft og organskader. |
| HLA-Matching | Man matcher donor- og modtagerceller baseret på humane leukocytantigener (HLA), som er immunsystemets 'ID-kort'. Der oprettes banker med stamcellelinjer, der dækker de mest almindelige HLA-typer. | Fordel: Reducerer risikoen for afstødning betydeligt. Ulempe: Svært at finde et perfekt match for alle, især for personer med sjældne HLA-typer. |
| Genetisk Modificerede 'Universelle' Celler | Ved hjælp af teknologier som CRISPR/Cas9 fjerner man HLA-molekylerne fra stamcellernes overflade, så de bliver 'usynlige' for immunsystemet. Man kan også tilføje signaler, der aktivt hæmmer immunangreb. | Fordel: Kan potentielt skabe en enkelt cellelinje, der passer til alle patienter. Ulempe: Sikkerhedsbekymringer; fjernelse af HLA kan gøre cellerne sårbare over for andre immunceller (NK-celler) og potentielt øge risikoen for kræft. |
| Induktion af Tolerance | Strategier, der sigter mod at 'opdrage' modtagerens immunsystem til at acceptere de nye celler som sine egne, f.eks. ved at anvende specifikke regulatoriske immunceller (Tregs). | Fordel: Kan skabe langvarig accept uden behov for konstant medicinering. Ulempe: Komplekst og stadig på et tidligt forskningsstadie. |
| Celleindkapsling | De terapeutiske celler placeres i en semipermeabel kapsel eller enhed af biomateriale. Kapslen tillader næringsstoffer og ilt at trænge ind og terapeutiske stoffer at komme ud, men forhindrer immunceller i at nå og ødelægge cellerne. | Fordel: Fysisk barriere mod immunangreb. Ulempe: Risiko for arvævsdannelse omkring kapslen, og udfordringer med at sikre langvarig overlevelse og funktion af de indkapslede celler. |
Fremtiden er Synergi
Fremtidens regenerative medicin vil sandsynligvis ikke handle om at vælge én enkelt tilgang, men om at kombinere dem for at opnå den bedst mulige effekt. Man kan forestille sig et scenarie, hvor en patient med en hjertesygdom modtager en transplantation af HLA-matchede eller genetisk modificerede hjertemuskelceller for at erstatte det tabte væv. Samtidig modtager patienten en behandling med EV'er, der dæmper inflammation, fremmer blodkarvækst og understøtter de nye cellers overlevelse og integration. Denne skræddersyede, multidimensionelle tilgang, der er tilpasset den enkelte patient, sygdom og transplantationssted, repræsenterer det ultimative mål inden for regenerativ medicin.
Ofte Stillede Spørgsmål (OSS)
Er EV-terapi sikrere end stamcelleterapi?
EV-terapi har potentielle sikkerhedsfordele. Da det er en acellulær behandling, er der ingen risiko for, at de administrerede enheder deler sig ukontrolleret og danner tumorer. De menes også at have en lavere immunogenicitet, hvilket reducerer risikoen for en kraftig immunreaktion. Dog er feltet stadig nyt, og der er brug for flere kliniske studier for fuldt ud at fastslå sikkerhedsprofilen.
Hvad er den største forskel på exosomer og mikrovesikler?
De primære forskelle ligger i deres dannelsesproces (biogenese) og deres størrelse. Exosomer er generelt mindre (50-150 nm) og dannes internt i cellen via endosomale veje, før de frigives. Mikrovesikler er større (100-1000 nm) og dannes ved direkte afknopning fra cellens overflade.
Kan EV'er bruges til at levere medicin?
Ja, absolut. Deres naturlige evne til at transportere molekyler mellem celler og beskytte deres last mod nedbrydning gør dem til yderst attraktive kandidater for målrettet lægemiddellevering. Forskere arbejder på at 'fylde' EV'er med specifik medicin, som de derefter kan levere direkte til syge celler, f.eks. kræftceller, hvilket kan øge effektiviteten og reducere bivirkninger.
Hvad er HLA-matching, og hvorfor er det vigtigt?
Humane leukocytantigener (HLA) er proteiner på overfladen af næsten alle kroppens celler. Immunsystemet bruger dem til at skelne mellem 'selv' (kroppens egne celler) og 'ikke-selv' (fremmede celler som bakterier eller transplanterede celler). Ved at matche HLA-typerne mellem donor og modtager så tæt som muligt, reducerer man risikoen for, at modtagerens immunsystem identificerer de nye celler som fremmede og starter en afstødningsreaktion.
Hvis du vil læse andre artikler, der ligner Stamceller & EV'er: Regenerativ Medicins Fremtid, kan du besøge kategorien Medicin.
