12/01/1999
Vores krop er udstyret med et utroligt komplekst og effektivt forsvarssystem: immunforsvaret. En af de mest afgørende soldater i denne hær er T-cellen, en type hvid blodcelle, der er specialiseret i at identificere og ødelægge inficerede celler og kræftceller. Men i den langvarige og opslidende kamp mod en kræftsvulst kan disse T-celler blive trætte og miste deres kampgejst. Denne tilstand, kendt som T-celleudmattelse, er en af de primære årsager til, at kræft kan undslippe kroppens eget forsvar. At forstå og vende denne proces er blevet en af de hellige graler inden for moderne kræftbehandling, og det danner grundlaget for de revolutionerende fremskridt inden for immunterapi.
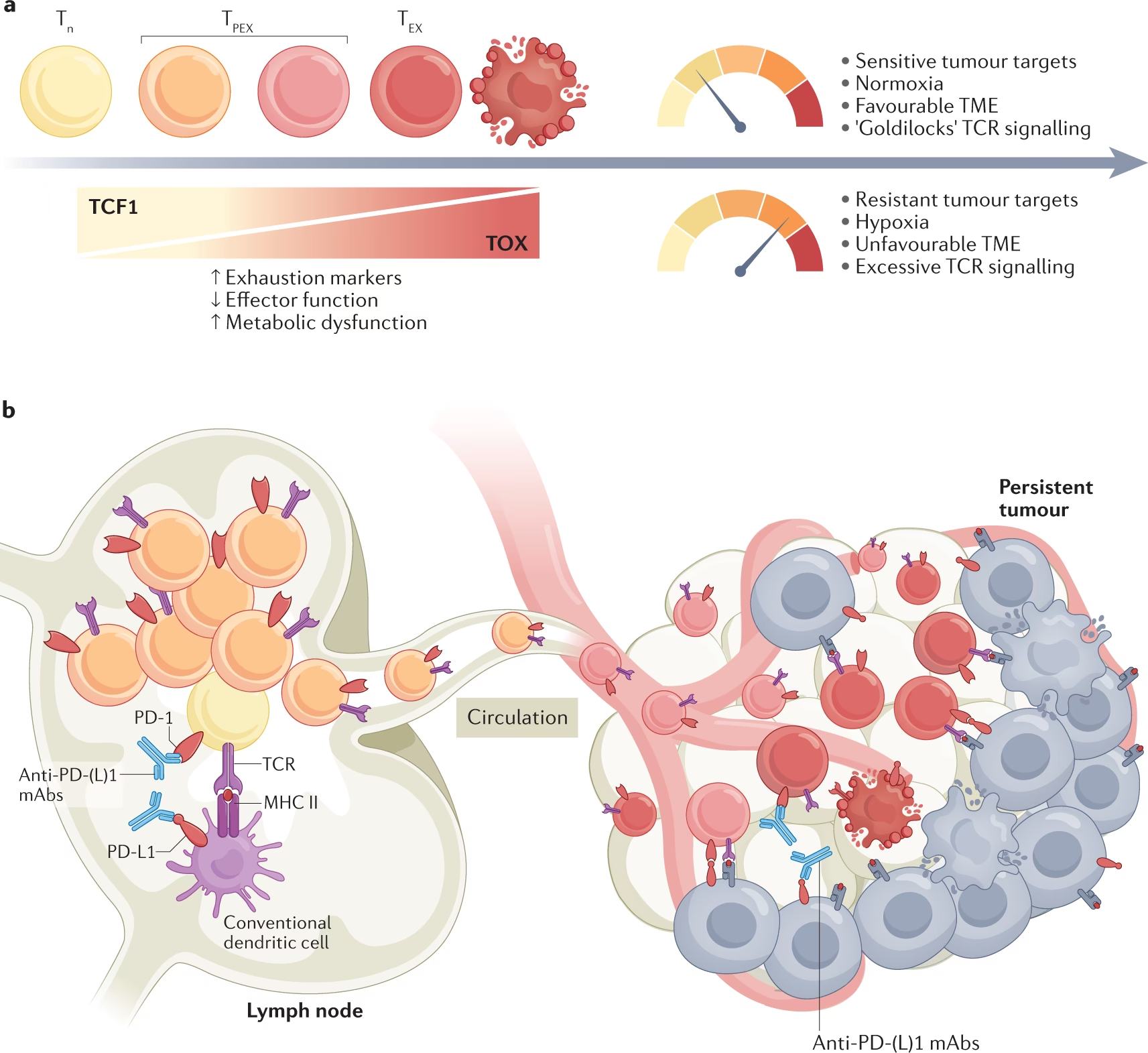
Hvad er T-celleudmattelse helt præcist?
For at en T-celle kan blive fuldt aktiveret og gå til angreb, kræver det en række præcise signaler. Man kan tænke på det som en startprocedure med flere trin:
- Signal 1: Genkendelse. T-cellen skal genkende en specifik markør (et antigen) på overfladen af en kræftcelle. Dette er som at finde det rigtige mål.
- Signal 2: Bekræftelse. Efter genkendelse har T-cellen brug for et bekræftelsessignal. Dette signal kan enten være et "go"-signal (co-stimulerende), der opmuntrer til angreb, eller et "stop"-signal (co-hæmmende), der fungerer som en bremse for at undgå overreaktion og skade på sundt væv.
- Signal 3: Brændstof. Cellen har brug for stimulering fra eksterne signalstoffer (cytokiner som IL-2) for at kunne formere sig og opretholde sit angreb.
Det er balancen i Signal 2, der er altafgørende. I en normal, kortvarig infektion er "stop"-signalerne vigtige for at dæmpe immunresponset, når faren er ovre. Men i tumormikromiljøet bliver T-cellerne konstant bombarderet med kræftantigener. Denne vedvarende stimulation fører til, at "stop"-signalerne tager overhånd. T-cellerne begynder at udtrykke en lang række hæmmende receptorer på deres overflade, som fungerer som konstante bremsepedaler. Resultatet er T-celleudmattelse, en tilstand hvor cellerne er til stede, men ude af stand til at producere de nødvendige våben (cytokiner som IFN-γ og TNF-α) og effektivt dræbe kræftceller. De er i bund og grund blevet pacificeret af tumoren selv.
De Vigtigste "Bremsepedaler": Inhibitoriske Receptorer
Forskningen har identificeret en række af disse hæmmende receptorer, der spiller en central rolle i T-celleudmattelse. At forstå dem er nøglen til at udvikle lægemidler, der kan blokere dem og dermed slippe bremserne for immunforsvaret.
PD-1: Den Primære Regulator
Programmed cell death protein 1 (PD-1) er måske den mest kendte og vigtigste regulator af T-celleudmattelse. Når T-celler i en tumor er udmattede, ses et markant forhøjet niveau af PD-1 på deres overflade. Kræftceller er snedige og udnytter dette ved at udtrykke partner-molekylet til PD-1, kendt som PD-L1. Når PD-1 på T-cellen binder til PD-L1 på kræftcellen, sendes et kraftigt "stop"-signal direkte ind i T-cellen, som lammer dens funktion. Studier på tværs af mange kræftformer, fra modermærkekræft til lungekræft og Hodgkins lymfom, har vist, at blokering af denne PD-1/PD-L1-akse med lægemidler kan genoprette T-cellernes funktion og føre til imponerende tumorreduktion.
CTLA-4: En Anden Kritisk Bremse
Cytotoxic T-lymphocyte-associated protein 4 (CTLA-4) er en anden vigtig hæmmende receptor. Den fungerer lidt anderledes end PD-1. CTLA-4 konkurrerer med et "go"-signal (CD28) om at binde til de samme molekyler på antigenpræsenterende celler. Ved at binde stærkere end CD28, kaprer CTLA-4 effektivt aktiveringsprocessen og dæmper T-cellens respons, herunder dens produktion af det vigtige "brændstof"-cytokin IL-2. Ligesom med PD-1, har udviklingen af lægemidler, der blokerer CTLA-4, været et stort gennembrud i kræftbehandlingen.
Når Kombination er Nøglen
Ofte er de mest udmattede T-celler dem, der udtrykker flere forskellige hæmmende receptorer samtidigt. Det er ikke ualmindeligt at finde T-celler i en tumor, der både har PD-1 og CTLA-4 på overfladen. Disse celler er typisk de mest dysfunktionelle. Dette har ført til en logisk konklusion: Hvis én bremse er aktiveret, kan det hjælpe at fjerne den. Men hvis flere bremser er aktiveret, opnår man en meget stærkere effekt ved at fjerne dem alle. Dobbelt blokade af både PD-1 og CTLA-4 har vist sig at være markant mere effektiv i visse kræftformer, da det genopliver en større del af T-cellepopulationen og fører til et mere robust og varigt anti-tumor respons.
En Voksende Familie af Mål
Ud over PD-1 og CTLA-4 har forskere identificeret en hel række andre hæmmende receptorer, der bidrager til udmattelsen. Disse inkluderer TIM-3, LAG-3, BTLA og TIGIT. Hver af disse receptorer har sin egen unikke mekanisme, men de bidrager alle til det samme overordnede problem. Co-ekspression af f.eks. PD-1 og TIM-3 eller PD-1 og LAG-3 på T-celler signalerer en endnu dybere grad af udmattelse. Dette åbner op for en fremtid med endnu mere sofistikerede kombinationsbehandlinger, hvor man skræddersyr behandlingen til præcis de "bremser", der er mest aktive i en given patients tumor.
Sammenligning af Vigtige Inhibitoriske Receptorer
| Receptor | Primær Funktion | Betydning i Kræft |
|---|---|---|
| PD-1 | Dæmper T-celleaktivitet i perifert væv og tumorer. | Meget udbredt på udmattede T-celler i tumorer. Primært mål for immunterapi. |
| CTLA-4 | Regulerer T-celleaktivering tidligt i processen, primært i lymfeknuder. | Et af de første mål for checkpoint-hæmmere. Blokade fjerner en tidlig bremse. |
| TIM-3 | Markør for alvorlig udmattelse, ofte co-udtrykt med PD-1. | Indikerer en meget dysfunktionel T-celle. Dobbelt blokade med PD-1 er lovende. |
| LAG-3 | Hæmmer T-cellefunktion og cytokinproduktion, ofte sammen med PD-1. | Ligesom TIM-3, er det et mål for kombinationsbehandlinger for at overvinde resistens. |
| TIGIT | Konkurrerer med et co-stimulerende signal (CD226) for at dæmpe T-celler. | Et nyere, men meget lovende mål, især i kombination med PD-1-blokade. |
Fra Nedsat Funktion til Celldød
T-celleudmattelse er en progressiv proces. I de tidlige stadier er T-cellerne blot mindre effektive. De mister evnen til at producere en bred vifte af cytokiner og kan ikke formere sig optimalt. Men hvis den konstante stimulation og de hæmmende signaler fortsætter, kan udmattelsen føre til det ultimative negative udfald: fysisk sletning af T-cellerne gennem programmeret celledød (apoptose). Tumorers udtryk af PD-L1 kan direkte inducere apoptose i de PD-1-positive T-celler, der forsøger at angribe dem. Dette betyder, at tumoren ikke kun pacificerer sine fjender, men aktivt eliminerer dem. Dette understreger vigtigheden af at gribe ind tidligt for at genoplive de udmattede T-celler, før de forsvinder helt.
Desuden påvirker udmattelse T-cellernes evne til at danne langtidshukommelse. Et sundt immunrespons skaber hukommelses-T-celler, der kan genkende og hurtigt eliminere en trussel, hvis den vender tilbage. Udmattede T-celler er dårlige til at danne denne type hukommelse. Dette kan forklare, hvorfor kræft kan vende tilbage efter en ellers vellykket behandling. Ved at vende udmattelsen håber man ikke kun på at fjerne den nuværende tumor, men også på at etablere en varig immunologisk hukommelse, der beskytter mod fremtidig tilbagefald.
Ofte Stillede Spørgsmål
Er T-celleudmattelse det samme som et svagt immunforsvar?
Ikke helt. En person kan have et generelt stærkt og velfungerende immunforsvar, men stadig udvikle T-celleudmattelse specifikt inden i tumormikromiljøet. Det er en lokal og specifik dysfunktion forårsaget af kronisk eksponering for kræftantigener, ikke en generel svækkelse af hele systemet.
Virker immunterapi, der sigter mod T-celleudmattelse, på alle kræfttyper?
Behandlingen, kendt som checkpoint-hæmmer-terapi, har vist bemærkelsesværdig succes i mange kræfttyper som modermærkekræft, lungekræft og nyrekræft. Effektiviteten afhænger dog af, om tumoren og de omkringliggende T-celler udtrykker de relevante molekyler (som PD-1 og PD-L1). Ikke alle tumorer reagerer lige godt, og forskning fokuserer intensivt på at forstå, hvorfor nogle patienter responderer, mens andre ikke gør.
Hvad er de vigtigste lægemidler, der bruges til at modvirke T-celleudmattelse?
De mest kendte er monoklonale antistoffer, der fungerer som "checkpoint-hæmmere". Disse lægemidler er designet til fysisk at blokere interaktionen mellem f.eks. PD-1 og PD-L1, eller mellem CTLA-4 og dets partnere. Ved at gøre dette "frigøres bremserne", og T-cellerne kan genoptage deres angreb på kræftcellerne.
Kan man vende T-celleudmattelse permanent?
Dette er et centralt forskningsspørgsmål. Mens checkpoint-hæmmere klart kan genoplive T-cellernes funktion, tyder nogle studier på, at dybe epigenetiske "ar" kan forblive i cellerne. Målet er at genoprette funktionen længe nok til, at immunsystemet kan få kontrol over og eliminere tumoren, hvilket kan føre til en langvarig og holdbar respons, selvom T-cellerne måske ikke vender fuldstændigt tilbage til deres oprindelige, naive tilstand.
Hvis du vil læse andre artikler, der ligner Genoplivning af T-celler: Nøglen til Kræft, kan du besøge kategorien Sundhed.
