03/12/2018
Bag ethvert banebrydende klinisk forsøg og enhver ny medicinsk behandling står en kompleks struktur af ansvar og tilsyn. Mange tænker måske på læger og forskere som de primære drivkræfter, men i virkeligheden er der en fundamental figur, der bærer det ultimative ansvar: sponsoren. Men er en sponsor virkelig nødvendig for alle kliniske forsøg? Svaret er et utvetydigt ja. Uden en sponsor kan et klinisk forsøg simpelthen ikke igangsættes, styres eller gennemføres lovligt og etisk forsvarligt. Denne artikel vil dykke ned i, hvad en sponsor er, hvilket enormt ansvar rollen indebærer, og hvorfor den er hjørnestenen i al klinisk forskning.
Hvad er en sponsor i klinisk forskning?
I konteksten af klinisk forskning er en sponsor ikke blot en person eller organisation, der giver penge. Definitionen er langt mere specifik og juridisk bindende. En sponsor er den juridiske enhed (en organisation, institution eller virksomhed), der har det endelige ansvar for igangsættelse, ledelse, finansiering og overordnet tilsyn med et klinisk forsøg. Det er sponsoren, der garanterer, at studiet overholder alle gældende love, regler og etiske standarder, såsom Good Clinical Practice (GCP).
Denne juridiske enhed kan være et medicinalfirma, et universitet, et hospital eller endda en velgørenhedsorganisation. Det afgørende er, at sponsoren påtager sig det fulde ansvar for studiets integritet og deltagernes sikkerhed. Selvom sponsoren kan uddelegere specifikke opgaver til tredjeparter, såsom en kontraktforskningsorganisation (CRO), kan det ultimative ansvar aldrig overdrages. Sponsoren forbliver den part, som myndighederne, etiske komiteer og deltagerne holder ansvarlig.
Sponsorens Kerneansvar: Mere end blot finansiering
Sponsorens rolle strækker sig langt ud over at skaffe de nødvendige midler til et studie. Ansvaret er mangesidet og dækker hele studiets livscyklus, fra den indledende idé til den endelige rapportering af resultaterne. Nedenfor er nogle af de mest kritiske ansvarsområder:
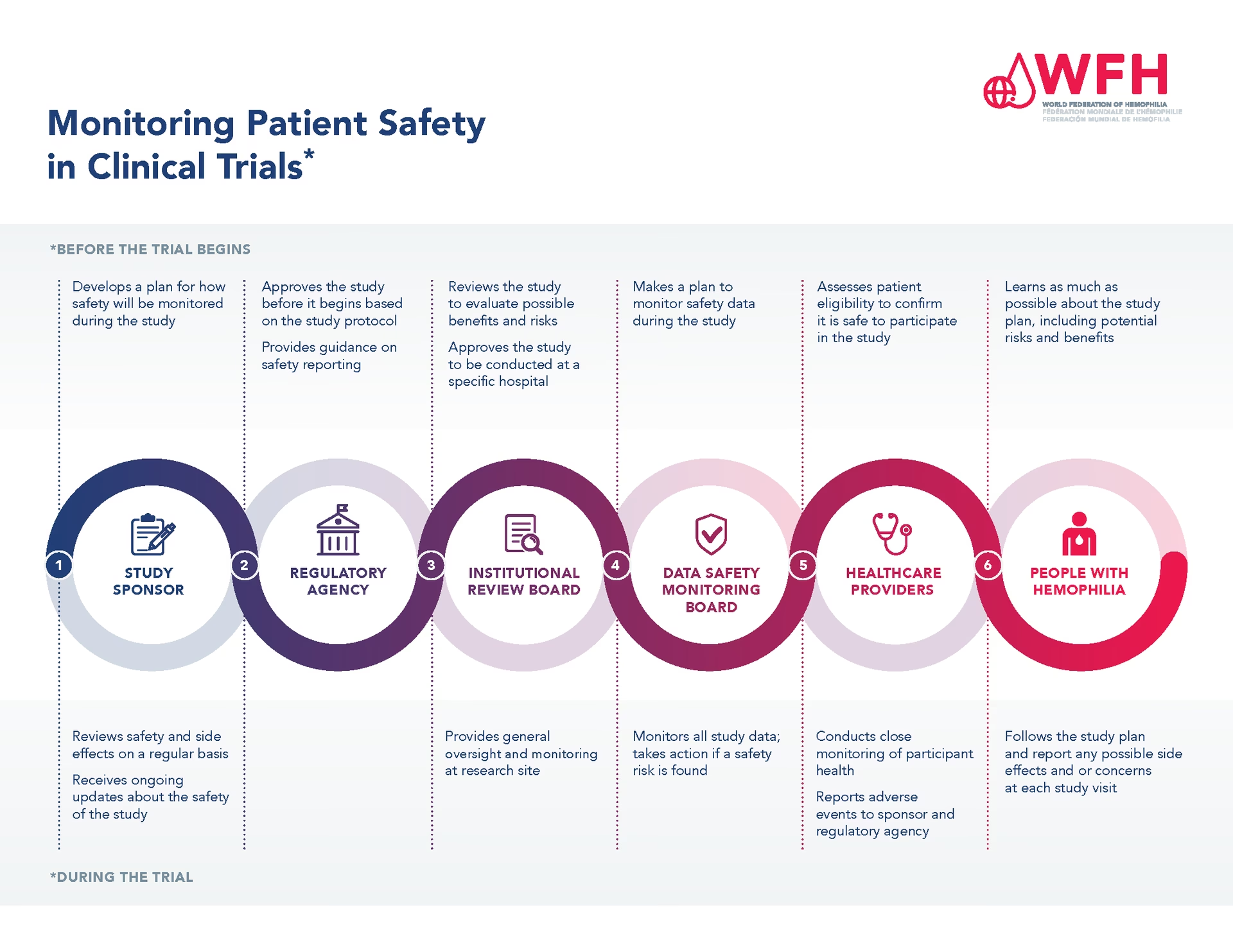
- Igangsættelse og design: Sponsoren er ansvarlig for at sikre, at forsøgsprotokollen er videnskabeligt forsvarlig og etisk acceptabel. De sikrer, at studiet er designet til at besvare de relevante forskningsspørgsmål, samtidig med at deltagernes rettigheder og velvære beskyttes.
- Ledelse og tilsyn: Sponsoren skal føre tilsyn med hele forsøget for at sikre, at det udføres i overensstemmelse med protokollen og gældende regler. Dette indebærer løbende overvågning af datakvalitet og -integritet.
- Finansiering: Selvom det er et åbenlyst ansvar, indebærer det mere end blot at betale regningerne. Sponsoren skal sikre, at der er tilstrækkelige ressourcer til at gennemføre studiet sikkert og effektivt fra start til slut, herunder dækning af uforudsete udgifter.
- Sikkerhedsrapportering: Et af de mest vitale ansvarsområder er overvågning af deltagernes sikkerhed. Sponsoren skal have systemer på plads til at indsamle, vurdere og rapportere alle alvorlige bivirkninger (Adverse Events) til de relevante myndigheder og etiske komiteer.
- Forsikring og erstatning: Sponsoren skal sørge for, at der er passende forsikring eller skadesløsholdelse på plads. Dette er for at dække eventuelle skader, som deltagere måtte lide som følge af deres deltagelse i forsøget. Det er en fundamental beskyttelse for deltagerne.
- Ansvar som dataansvarlig: I henhold til databeskyttelseslove som GDPR er sponsoren typisk den dataansvarlige. Dette betyder, at de har det juridiske ansvar for, hvordan personoplysninger om deltagerne indsamles, behandles, opbevares og beskyttes.
- Patient- og offentlig involvering: En god sponsor sikrer, at patienter og offentligheden er involveret i forskningen på en meningsfuld måde. Dette kan forbedre studiets design, relevans og rekruttering.
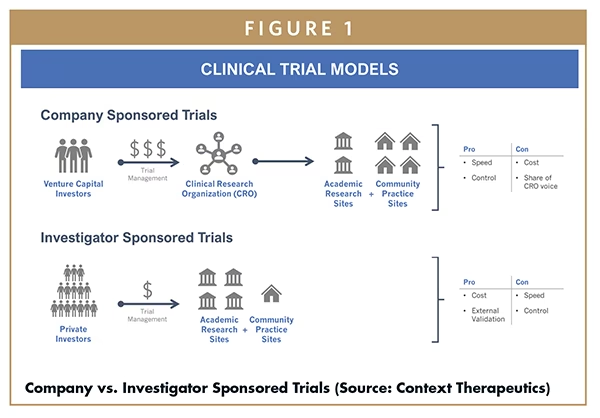
Forskellen mellem sponsor og hovedinvestigator
Det er let at forveksle sponsorens rolle med rollen som hovedinvestigator (Principal Investigator, PI), men de er fundamentalt forskellige. Mens sponsoren har det overordnede juridiske og finansielle ansvar, er hovedinvestigatoren den person, der er ansvarlig for den daglige udførelse af studiet på et specifikt forskningssted (f.eks. et hospital).
Hovedinvestigatoren er typisk en erfaren læge eller forsker, som leder forskerteamet på sitet. Deres ansvar omfatter at rekruttere deltagere, sikre informeret samtykke, administrere behandlingen i henhold til protokollen og indsamle data. Selvom hovedinvestigatoren har et stort ansvar for den praktiske gennemførelse, opererer vedkommende altid under sponsorens overordnede ansvar og tilsyn. I studier med flere sites vil der være en hovedinvestigator på hvert site og en overordnet chefinvestigator (Chief Investigator), der koordinerer på tværs af alle sites, men sponsoren er stadig den øverste ansvarlige enhed for hele studiet.
Hvem kan være sponsor? Kommercielle vs. Ikke-kommercielle enheder
Sponsorer kan groft opdeles i to kategorier: kommercielle og ikke-kommercielle. Begge typer er underlagt de samme strenge regler, men deres motivation og ressourcer kan variere. Nedenstående tabel sammenligner de to typer.
| Karakteristik | Kommerciel Sponsor | Ikke-kommerciel Sponsor |
|---|---|---|
| Eksempler | Medicinalfirmaer, biotekvirksomheder, producenter af medicinsk udstyr. | Universiteter, offentlige hospitaler, forskningsråd, velgørende organisationer. |
| Primært formål | At udvikle et produkt (f.eks. et lægemiddel) med henblik på markedsføring og salg. | At fremme videnskabelig viden, forbedre patientbehandling eller besvare et specifikt forskningsspørgsmål uden et direkte kommercielt mål. |
| Finansiering | Typisk finansieret af virksomhedens egne midler eller investorer. | Finansieret via offentlige bevillinger, donationer eller fonde. Kan modtage støtte fra kommercielle partnere. |
| Studietyper | Ofte store, multinationale kliniske forsøg med lægemidler (CTIMPs). | En bred vifte af studier, herunder observationelle studier, kirurgiske forsøg, diagnostiske studier og investigator-initierede lægemiddelforsøg. |
Nøgleaktører i økosystemet for klinisk forskning
Udover sponsoren og hovedinvestigatoren er der flere andre centrale aktører, der sikrer, at forskningen udføres korrekt og sikkert.
Etiske Komiteer (RECs)
En videnskabsetisk komité er en uafhængig instans, der har til opgave at vurdere alle etiske aspekter af et forskningsprojekt, før det kan begynde. De gennemgår protokollen, informationsmaterialet til deltagerne og samtykkeerklæringen for at sikre, at studiets potentielle fordele opvejer risiciene, og at deltagernes rettigheder er fuldt beskyttede. Komiteens godkendelse er en forudsætning for at starte et studie.
Regulerende Myndigheder
Nationale myndigheder, som f.eks. Lægemiddelstyrelsen i Danmark, er ansvarlige for at regulere kliniske forsøg med lægemidler og medicinsk udstyr. De skal godkende et studie, før det kan starte, og de fører tilsyn med, at sponsoren overholder lovgivningen under hele forløbet.
Data Controller og Data Processor
Som nævnt er sponsoren ofte den dataansvarlige (Data Controller). De bestemmer formålet med og måden, hvorpå personoplysninger behandles. En databehandler (Data Processor) er en separat juridisk enhed, der behandler data på vegne af den dataansvarlige efter dennes instruks. Det er afgørende, at disse roller og ansvarsområder er klart defineret i en databehandleraftale for at sikre overholdelse af databeskyttelsesloven.
Ofte Stillede Spørgsmål (FAQ)
Her er svar på nogle almindelige spørgsmål om sponsorrollen.
Spørgsmål: Er en sponsor altid nødvendig for et klinisk forsøg?
Svar: Ja, absolut. Alle kliniske forsøg, uanset størrelse, risiko eller finansieringskilde, skal have en udpeget sponsor. Det er et lovkrav og en grundlæggende forudsætning for at beskytte deltagerne og sikre forskningens kvalitet.
Spørgsmål: Kan en enkeltperson, f.eks. en forsker, være sponsor?
Svar: Generelt nej. En sponsor skal være en juridisk enhed (en organisation eller virksomhed), der har den nødvendige infrastruktur, finansielle stabilitet og ekspertise til at påtage sig det omfattende ansvar. En individuel forsker kan være hovedinvestigator, men vil typisk være ansat af den organisation (f.eks. et hospital eller universitet), der fungerer som sponsor.
Spørgsmål: Hvad sker der, hvis en sponsor ikke lever op til sit ansvar?
Svar: Konsekvenserne kan være alvorlige. Regulerende myndigheder kan suspendere eller stoppe forsøget. Sponsoren kan blive mødt med juridiske sanktioner og erstatningskrav. Desuden kan det skade organisationens omdømme alvorligt og underminere offentlighedens tillid til forskning.
Spørgsmål: Hvem ejer de data, der genereres i et klinisk forsøg?
Svar: Ejerskabet af data er normalt defineret i aftaler mellem sponsoren, forskningsstederne og eventuelle andre parter. Sponsoren har dog som dataansvarlig det juridiske ansvar for at beskytte dataene i overensstemmelse med GDPR og andre relevante love. De har ansvaret for, at data behandles fortroligt og sikkert.
Konklusionen er klar: sponsoren er den usynlige, men uundværlige rygrad i ethvert klinisk forsøg. Rollen er en garanti for ansvarlighed, sikkerhed og videnskabelig integritet. Uden en dedikeret og kompetent sponsor ville den medicinske forskning, vi stoler på for at udvikle nye og bedre behandlinger, ikke være mulig.
Hvis du vil læse andre artikler, der ligner Skal et klinisk forsøg have en sponsor?, kan du besøge kategorien Sundhed.