12/12/2009
Inden for moderne kræftbehandling er et paradigmeskifte i gang. Væk er dagene, hvor en 'one-size-fits-all'-tilgang var den eneste mulighed. I dag bevæger vi os med hastige skridt ind i en æra af præcisionsmedicin, hvor behandlingen skræddersys til den enkelte patients unikke biologiske profil. Hjørnestenen i denne revolution er brugen af biomarkører. Disse små, målbare indikatorer i vores krop giver lægerne et detaljeret kort over en kræftsvulsts specifikke egenskaber, hvilket åbner døren for mere effektive og mindre skadelige behandlinger. Denne artikel vil udforske, hvad biomarkører er, hvordan de fungerer, og hvilken afgørende rolle de spiller i kampen mod kræft.
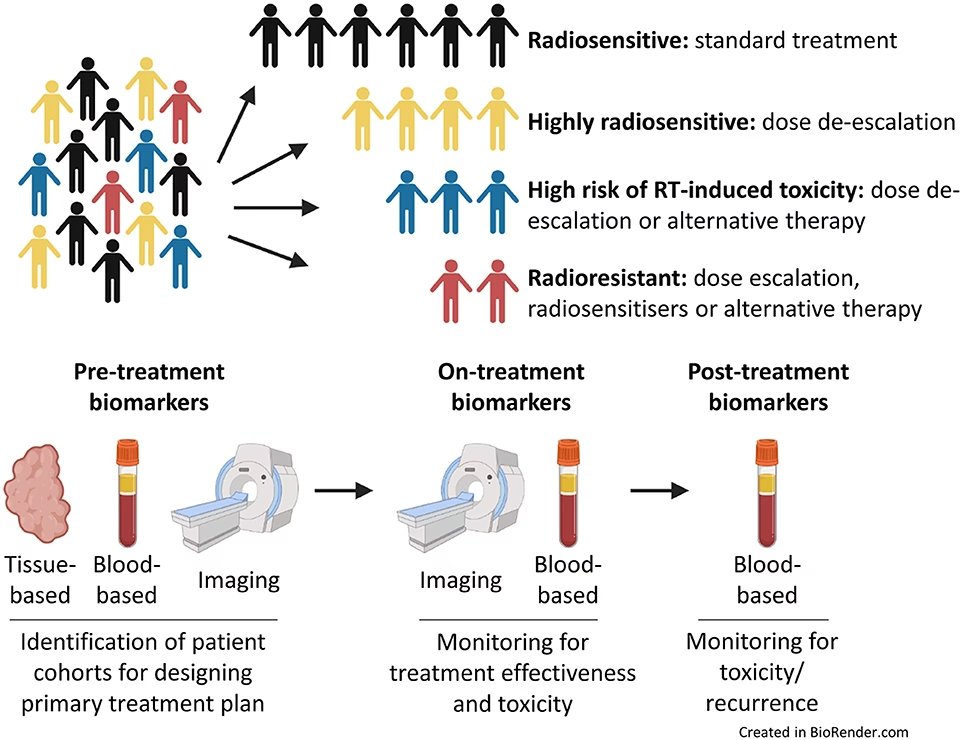
Hvad er en biomarkør?
En biomarkør er defineret som en målbar indikator for en normal eller unormal biologisk proces. I praksis kan det være et molekyle, et gen, et protein eller en anden karakteristik, der kan findes i blod, væv eller andre kropsvæsker. Når en læge tager en blodprøve eller en vævsprøve (biopsi), kan de analysere den for specifikke biomarkører, der kan afsløre tilstedeværelsen eller sværhedsgraden af en sygdom som kræft. En af de mest spændende udviklinger er konceptet 'flydende biopsi', hvor man via en simpel blodprøve kan finde og analysere biomarkører fra kræftceller, såsom cirkulerende tumor-DNA (ctDNA). Dette giver et realtidsbillede af kræften uden behov for et invasivt kirurgisk indgreb.
I onkologi bruges biomarkører til flere formål:
- Diagnose: At identificere kræfttyper og -undertyper med større præcision.
- Prognose: At forudsige sygdommens sandsynlige forløb og patientens overlevelseschancer.
- Behandlingsvejledning: At afgøre, hvilken behandling der vil være mest effektiv for en specifik patient.
- Monitorering: At overvåge, hvordan en patient reagerer på behandlingen, og om kræften vender tilbage.
Forskellige typer af biomarkører i kræftbehandling
Biomarkører kan inddeles i flere kategorier, hver med unikke anvendelser. Forståelsen af disse typer er essentiel for at værdsætte dybden af præcisionsmedicin.
Genetiske biomarkører
Disse er relateret til vores DNA og omfatter mutationer eller andre abnormiteter i gener, der er specifikke for visse kræftformer. De er afgørende for at guide målrettet behandling.
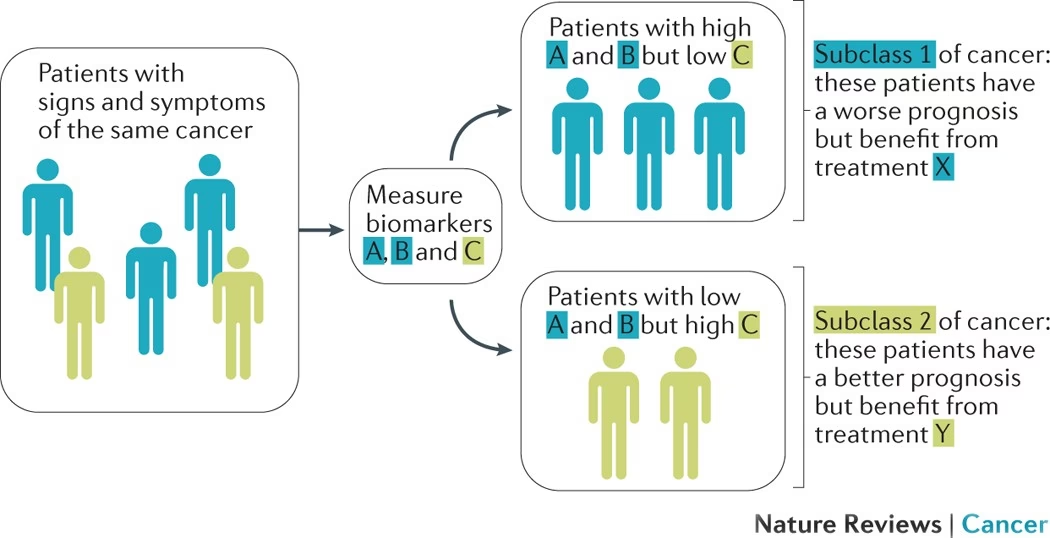
- Onkogener: Disse er gener, der, når de muterer eller bliver overaktive, kan forårsage ukontrolleret cellevækst. Man kan tænke på dem som en speeder, der har sat sig fast. Eksempler inkluderer HER2, BRAF og KRAS. Målrettede lægemidler kan designes til at blokere disse overaktive gener.
- Tumorsuppressorgener: Disse gener fungerer normalt som bremser, der regulerer cellevækst og forhindrer kræft. Når de muterer og deaktiveres, mister cellen sin evne til at kontrollere deling. TP53 og BRCA1/2 er velkendte eksempler.
- DNA-reparationsgener: Disse gener er ansvarlige for at reparere skader på vores DNA. Mutationer i gener som BRCA1 og BRCA2 øger risikoen for kræft, fordi cellerne ikke længere kan reparere fejl effektivt. Dette kan dog også udnyttes terapeutisk med lægemidler som PARP-hæmmere.
Epigenetiske biomarkører
Epigenetik handler om kemiske modifikationer af DNA og proteiner, der ændrer geners aktivitet uden at ændre selve DNA-sekvensen. Unormale epigenetiske mønstre, som f.eks. ændringer i DNA-methylering eller histonmodifikationer, er almindelige i kræftceller og kan bruges som biomarkører for diagnose og prognose.
Protein- og metabolitbiomarkører
Disse biomarkører er proteiner eller små molekyler (metabolitter), der produceres som et resultat af cellernes stofskifte. Deres niveauer kan være ændret i kræftpatienter.
- Proteinbiomarkører: Visse proteiner kan være overudtrykt i kræftceller. For eksempel er PSA (Prostata-Specifikt Antigen) en velkendt markør for prostatakræft, og CA-125 bruges til at overvåge æggestokkræft.
- Metabolitbiomarkører: Kræftcellers stofskifte er anderledes end normale cellers. Ved at måle niveauerne af specifikke metabolitter i blod eller urin kan man opdage og overvåge visse kræftformer.
Billeddiagnostiske biomarkører
Disse er ikke molekylære, men derimod kvantificerbare karakteristika, der kan observeres på medicinske billeder som MR-, PET- eller CT-scanninger. Parametre som tumorstørrelse, form, tæthed og metaboliske aktivitet kan fungere som biomarkører til at vurdere sygdommens omfang og behandlingseffekt.
Biomarkørers afgørende rolle i praksis
Teorien bag biomarkører omsættes dagligt til klinisk praksis, hvor de forbedrer patientresultater markant. Nedenstående tabel viser nogle af de mest anvendte biomarkører og deres betydning.

| Biomarkør | Kræfttype | Klinisk betydning |
|---|---|---|
| HER2 (Human Epidermal growth factor Receptor 2) | Brystkræft, mavekræft | Identificerer patienter, der vil have gavn af HER2-målrettede lægemidler som trastuzumab. HER2-positiv kræft er ofte mere aggressiv. |
| EGFR (Epidermal Growth Factor Receptor) | Ikke-småcellet lungekræft | Mutationer i EGFR-genet gør tumorer følsomme over for EGFR-hæmmere, en type målrettet behandling. |
| BRAF | Modermærkekræft (melanom), tyktarmskræft | En specifik mutation (V600E) indikerer, at patienten kan have stor effekt af BRAF-hæmmere. |
| BRCA1/BRCA2 | Brystkræft, æggestokkræft, prostatakræft | Mutationer indikerer øget arvelig risiko og gør tumorer sårbare over for PARP-hæmmere. |
| PD-L1 | Flere kræfttyper (bl.a. lunge, blære, modermærke) | Forudsiger sandsynligheden for respons på immunterapi (checkpoint-hæmmere). |
Udfordringer og fremtidsperspektiver
Selvom præcisionsmedicin baseret på biomarkører har et enormt potentiale, er der stadig udfordringer, der skal overvindes.
- Tumorheterogenitet: En enkelt tumor er sjældent ensartet. Den kan bestå af forskellige grupper af celler med forskellige mutationer. En biopsi fra ét område afspejler måske ikke hele tumoren, hvilket komplicerer behandlingsvalget.
- Høje omkostninger: Både biomarkørtestning og de målrettede lægemidler kan være meget dyre, hvilket skaber udfordringer for sundhedssystemer og adgang for patienter.
- Resistensudvikling: Kræftceller er adaptive. Over tid kan de udvikle nye mutationer, der gør dem resistente over for en ellers effektiv målrettet behandling.
- Etiske overvejelser: Genetisk testning kan afsløre arvelige risici, hvilket kan have konsekvenser for patienten og deres familie. Spørgsmål om datasikkerhed og potentiel genetisk diskrimination er også relevante.
Fremtiden ligger i at overkomme disse udfordringer. Forskere arbejder på at udvikle mere følsomme og omfattende tests, som f.eks. flydende biopsi, der kan give et mere komplet billede af en tumors udvikling og heterogenitet over tid. Kombinationsterapier, der angriber kræften fra flere vinkler samtidigt, bliver også mere almindelige for at forhindre resistens. Kunstig intelligens (AI) spiller en voksende rolle i at analysere de enorme mængder data fra biomarkørtestning for at finde nye mønstre og forudsige behandlingsrespons endnu mere præcist.
Ofte Stillede Spørgsmål
Hvad er forskellen på en almindelig biopsi og en 'flydende biopsi'?
En almindelig biopsi involverer fjernelse af et lille stykke væv direkte fra tumoren, ofte via et kirurgisk indgreb. En flydende biopsi er en blodprøve, hvor man analyserer for cirkulerende tumorceller eller fragmenter af tumor-DNA (ctDNA), som kræftceller har frigivet til blodbanen. Den er mindre invasiv og kan gentages oftere for at overvåge sygdommen.
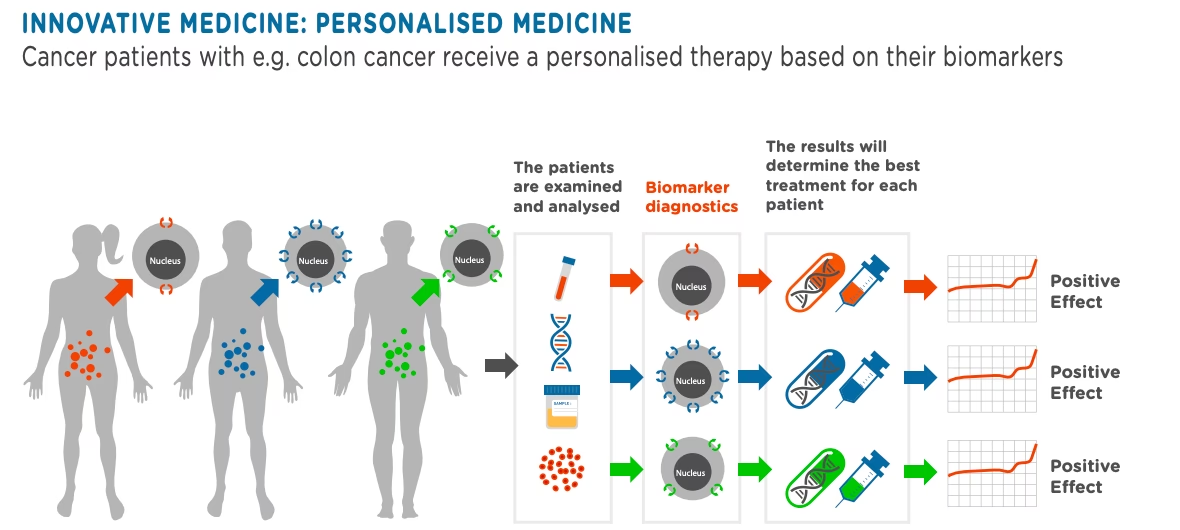
Kan alle kræftpatienter få gavn af biomarkørtest?
Ikke alle kræftformer har endnu kendte, handlingsanvisende biomarkører. Men for et stadigt voksende antal kræfttyper, herunder lunge-, bryst-, tyktarms- og modermærkekræft, er biomarkørtestning blevet standardpraksis og afgørende for at vælge den bedste behandling.
Er målrettet behandling altid bedre end traditionel kemoterapi?
Målrettet behandling er ofte mere effektiv og har færre bivirkninger end traditionel kemoterapi, HVIS patientens tumor har den specifikke biomarkør, som lægemidlet er rettet mod. Hvis tumoren ikke har denne markør, vil behandlingen ikke virke. Kemoterapi spiller stadig en vigtig rolle i mange behandlingsforløb, ofte i kombination med målrettet terapi eller immunterapi.
Dækker det offentlige sundhedsvæsen omkostningerne til biomarkørtest?
I Danmark og mange andre lande dækkes omkostningerne til veletablerede og klinisk nødvendige biomarkørtests, der er afgørende for valg af standardbehandling, af det offentlige sundhedssystem. Adgangen til nyere og mere eksperimentelle tests kan variere.
Hvis du vil læse andre artikler, der ligner Biomarkører: Nøglen til personlig kræftbehandling, kan du besøge kategorien Kræft.
