04/07/2012
I den komplekse verden af lægemiddeludvikling er rejsen fra en lovende kemisk forbindelse til et godkendt lægemiddel lang og fyldt med udfordringer. En af de største forhindringer er ofte et molekyles fysiske egenskaber. En forbindelse kan vise fantastisk aktivitet i et reagensglas, men hvis den ikke kan opløses i kroppens væsker, kan den aldrig nå sit mål og udøve sin virkning. Her kommer et af de mest kraftfulde værktøjer i medicinsk kemi ind i billedet: bioisosterisme. Dette er princippet om at udskifte en del af et molekyle med en anden del, der har lignende fysiske eller kemiske egenskaber. Målet er at finjustere molekylet for at forbedre dets profil, især dets opløselighed, uden at ofre dets terapeutiske effekt.
Hvad er Bioisosterisme Helt Præcist?
Forestil dig, at du bygger med legoklodser. Du har en struktur, der næsten er perfekt, men en enkelt klods har en forkert farve eller passer ikke helt. Du finder en anden klods, der har næsten samme størrelse og form, og som passer perfekt ind og fuldender din model. Bioisosterisme fungerer på en lignende måde på et molekylært niveau. Forskere identificerer en del af et lægemiddelmolekyle – et atom eller en gruppe af atomer – der forårsager problemer, såsom dårlig opløselighed eller uønskede bivirkninger. Derefter erstatter de denne del med en 'bioisoster', en kemisk gruppe, der efterligner den oprindelige dels størrelse, form og elektroniske egenskaber, men som samtidig introducerer en ønsket forbedring, f.eks. øget polaritet, hvilket fører til bedre opløselighed i vand.
To Typer af Bioisosterer: Klassisk og Ikke-Klassisk
Bioisosterer kan groft inddeles i to hovedkategorier, som hver især tilbyder unikke strategier for molekylær modifikation.
- Klassiske Bioisosterer: Disse er atomer eller grupper, der har det samme antal valenselektroner (elektroner i den yderste skal). De er ofte meget ens i størrelse og form. Udskiftningerne er typisk simple og følger forudsigelige regler.
- Ikke-Klassiske Bioisosterer: Disse følger ikke de strenge regler for valenselektroner, men de efterligner de rumlige og elektroniske egenskaber af den oprindelige gruppe. De kan være mere komplekse funktionelle grupper, der kan ændre et molekyles egenskaber på mere dybtgående måder.
For at give et klarere overblik, er her en tabel, der illustrerer de forskellige typer af bioisosterer med eksempler:
| Klassiske Bioisosterer | Ikke-Klassiske Bioisosterer |
|---|---|
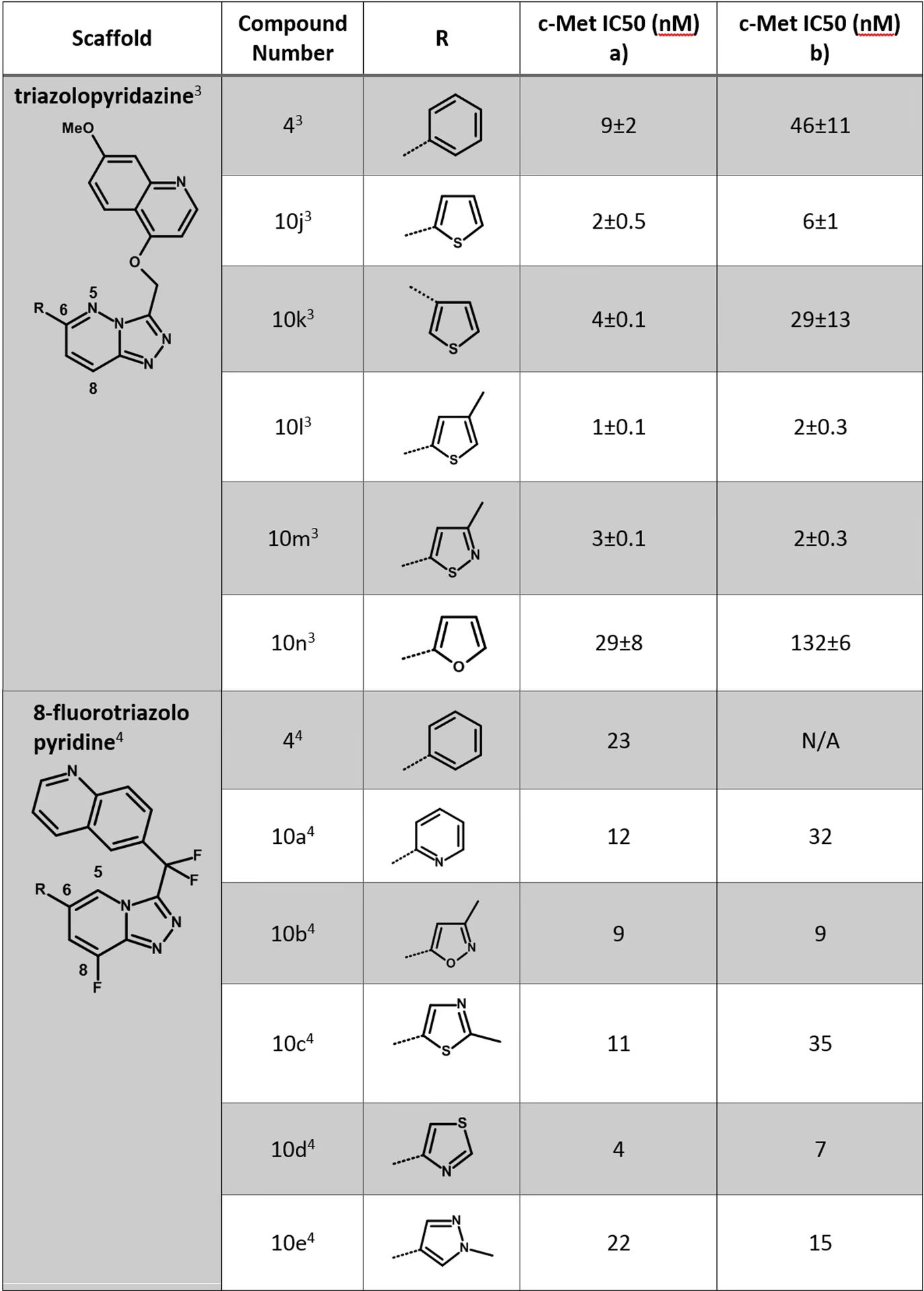
| Monovalente atomer/grupper: -OH, -NH₂, -CH₃, -Cl, -SH | Cykliske vs. Ikke-cykliske grupper: Udskiftning af en benzenring med en thiophenring. |
| Divalente atomer/grupper: -O-, -S-, -CH₂- | Udskiftelige funktionelle grupper: En carboxylsyregruppe (-COOH) kan erstattes med en tetrazolring. |
| Trivalente atomer/grupper: -CH=, -N=, -P= | Eksempler: Benzimidazol, 3-hydroxyisoxazol. |
| Tetrasubstituerede atomer: C, Si | Disse grupper efterligner den overordnede topologi og elektroniske profil uden at dele valensstruktur. |
| Ringækvivalenter: Benzenring (-C₆H₅) vs. Pyridinring (-C₅H₄N) | --- |
Forbedring af Opløselighed: Fra Laboratoriet til Patienten
Et lægemiddels opløselighed er altafgørende. For at kroppen kan optage et lægemiddel, der tages oralt, skal det først opløses i mave-tarm-kanalen. Et stof med lav opløselighed vil passere gennem systemet uden at blive absorberet i tilstrækkelig grad, hvilket gør det ineffektivt, uanset hvor potent det er på et cellulært niveau. Bioisosterisk udskiftning er en af de mest anvendte metoder til at tackle dette problem. Ved at erstatte en upolær, fedtopløselig (lipofil) del af et molekyle, som f.eks. en phenylring, med en mere polær, vandopløselig (hydrofil) gruppe, som en pyridin- eller pyrazolring, kan forskere dramatisk forbedre et molekyles vandopløselighed. Dette forbedrer ikke kun absorptionen, men kan også påvirke andre farmakokinetiske egenskaber positivt, såsom hvordan lægemidlet fordeles i kroppen og udskilles.
Eksempler fra den Virkelige Verden
Medicinsk kemi er fyldt med succeshistorier, hvor bioisosterisme har forvandlet problematiske molekyler til levedygtige lægemiddelkandidater.
- Kræftbehandling: Forskere, der arbejdede med en Src/Abl dual-hæmmer til kræftbehandling, havde et lovende molekyle, der desværre havde dårlige farmakokinetiske egenskaber. Ved at erstatte en fluorophenylring med en mere vandopløselig 4-picolyl-gruppe, lykkedes det dem at forbedre den termodynamiske opløselighed markant, samtidig med at aktiviteten blev bibeholdt.
- Malaria: Et molekyle (CK-2-68) med potentiale til at bekæmpe malariaparasitten Plasmodium falciparum var begrænset af sin høje fedtopløselighed (logP-værdi) og manglende vandopløselighed. Ved at foretage en bioisosterisk udskiftning af en phenyl-sidekæde med en pyridinring, skabte forskerne et nyt molekyle (SL-2-25). Denne ændring forbedrede ikke kun opløseligheden, men reducerede også logP-værdien betydeligt, hvilket resulterede i et mere effektivt lægemiddel.
- Epilepsi: I udviklingen af T-type calciumkanalblokkere til behandling af epilepsi, stod forskerne over for et problem med dårlig vandopløselighed i deres 1,4-benzodiazepin-derivater. En smart bioisosterisk udskiftning, hvor benzenringen i benzodiazepinstrukturen blev erstattet med en pyridinring, førte til et pyridodiazepin-derivat. Resultatet var et molekyle med forbedret opløselighed og potent aktivitet mod anfald.
- Ikke-konventionelle Udskiftninger: Nogle gange kræver det mere kreativ tænkning. I et tilfælde blev en flad fluorophenylring i en gamma-sekretasehæmmer erstattet med en tredimensionel bicyclo[1.1.1]pentan-struktur. Denne 'ikke-konventionelle' udskiftning brød molekylets planhed, hvilket øgede dets tredimensionalitet. Dette simple trick førte til en markant forbedring af både vandopløselighed og hjernens permeabilitet, hvilket er afgørende for lægemidler, der skal virke i centralnervesystemet.
Mere end blot Opløselighed
Selvom forbedring af opløselighed er en primær anvendelse, strækker fordelene ved bioisosterisme sig meget længere. Denne strategi bruges også til at:
- Forbedre potens: Små ændringer kan optimere, hvordan et lægemiddel binder sig til sit målprotein, hvilket øger dets effektivitet.
- Øge selektivitet: Ved at justere et molekyles form kan man gøre det mere specifikt for sit mål, hvilket reducerer binding til andre proteiner og dermed minimerer bivirkninger.
- Forbedre metabolisk stabilitet: Visse dele af et molekyle er sårbare over for nedbrydning af kroppens enzymer. Ved at erstatte disse 'metaboliske hotspots' med mere robuste bioisosterer, kan man forlænge lægemidlets levetid i kroppen.
- Reducere toksicitet: Udskiftning af en potentielt toksisk funktionel gruppe med en mere harmløs bioisoster kan gøre et lægemiddel meget sikrere for patienten.
Bioisosterisme er således en fundamental og alsidig del af det molekylære designarbejde, der ligger til grund for udviklingen af næsten al moderne medicin. Det er et vidnesbyrd om den elegance og præcision, der kræves for at designe molekyler, der ikke kun er effektive, men også sikre og praktiske for patienterne.
Ofte Stillede Spørgsmål (FAQ)
- Er bioisosterisme en ny opfindelse?
- Nej, konceptet er en klassisk tilgang inden for medicinsk kemi og har været anvendt i årtier. Dog har moderne værktøjer som molekylær modellering og avanceret syntetisk kemi gjort det muligt for forskere at anvende princippet med større præcision og kreativitet end nogensinde før.
- Hvorfor er det så vigtigt, at et lægemiddel kan opløses i vand?
- Kroppen består primært af vand. For at et lægemiddel kan transporteres via blodet og nå frem til de celler eller væv, hvor det skal virke, skal det kunne opløses i dette vandige miljø. Dårlig opløselighed betyder dårlig absorption og distribution, hvilket i sidste ende betyder, at lægemidlet ikke virker.
- Er det risikabelt at ændre på et molekyles struktur?
- Ja, enhver ændring i et molekyles struktur medfører en risiko for at ændre dets biologiske aktivitet eller sikkerhedsprofil. Derfor er bioisosterisk udskiftning en omhyggelig proces, der involverer omfattende testning. Hver ny variant af et molekyle skal gennemgå strenge prækliniske og kliniske forsøg for at sikre, at det er både sikkert og effektivt, før det kan blive til et godkendt lægemiddel.
- Bruges bioisosterisme til alle typer medicin?
- Ja, princippet er universelt og anvendes på tværs af næsten alle terapeutiske områder, herunder kræft, infektionssygdomme, hjerte-kar-sygdomme og neurologiske lidelser. Uanset sygdommen er de grundlæggende krav til et lægemiddels fysiske og kemiske egenskaber de samme.
Hvis du vil læse andre artikler, der ligner Bioisosterisme: Nøglen til Bedre Medicin, kan du besøge kategorien Farmaci.

