28/02/2019
Vores hjerne er et utroligt komplekst og følsomt organ, der er afgørende for vores eksistens. For at beskytte den mod skadelige stoffer, toksiner og patogener, har kroppen udviklet en yderst specialiseret og selektiv grænse: blod-hjerne-barrieren (BBB). Denne barriere fungerer som en omhyggelig portvagt, der nøje kontrollerer, hvad der får lov til at passere fra blodbanen ind i hjernens væv. Selvom denne beskyttelsesmekanisme er livsvigtig, udgør den samtidig en af de største forhindringer inden for medicinsk behandling af sygdomme i centralnervesystemet (CNS), såsom Alzheimers, Parkinsons, hjernetumorer og multipel sklerose. At udvikle lægemidler, der effektivt kan krydse denne barriere, er en hellig gral inden for medicinsk kemi og farmakologi.
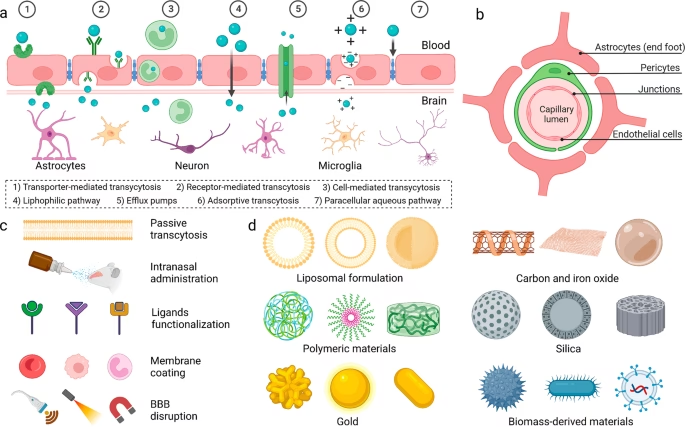
Passiv Diffusion: Den Direkte, Men Svære Vej
Den mest almindelige måde, hvorpå små molekyler kan trænge ind i hjernen, er gennem passiv diffusion. Dette indebærer, at molekylet bevæger sig direkte gennem cellemembranerne i de endotelceller, der udgør blod-hjerne-barrieren. Denne proces kræver ingen energi, men den stiller strenge krav til lægemidlets fysisk-kemiske egenskaber. For at forudsige et molekyles evne til at krydse BBB via passiv diffusion, har forskere udviklet en række retningslinjer, ofte opsummeret i det, der kaldes Lipinskis "Rule of Five".
Nøgleegenskaber for Effektiv Passiv Diffusion
For at et lægemiddel skal have en chance for at diffundere passivt ind i hjernen, skal det generelt opfylde følgende kriterier:
- Lav Molekylvægt: Mindre er absolut bedre. Lægemidler med en molekylvægt under 400-500 Dalton (Da) har en markant større chance for at passere. Faktisk kan permeabiliteten falde op til 100 gange, når molekylvægten stiger fra 200 Da til 450 Da. Det handler i bund og grund om molekylær volumen – små molekyler kan lettere smutte gennem de midlertidige porer, der dannes i cellemembranens fedtsyrekæder.
- Høj Lipofilicitet: Barrieren består primært af fedtstoffer (lipider). Derfor skal et molekyle være "fedtelskende" (lipofilt) for at kunne opløses i og passere gennem membranen. Dette måles ofte som logP-værdien.
- Lavt Polært Overfladeareal (PSA): Molekyler med mange polære grupper (som ilt og nitrogen) har svært ved at krydse den upolære, fedtbaserede barriere. Et lavt PSA er derfor at foretrække.
- Få Brintbindingsdonorer og -acceptorer: Evnen til at danne brintbindinger er relateret til polaritet. Færre brintbindinger betyder, at molekylet er mindre "klæbrigt" over for vand og lettere kan interagere med den lipofile barriere.
- Neutral Elektrisk Ladning: Molekyler med en stærk elektrisk ladning ved kroppens fysiologiske pH-værdi vil blive frastødt af cellemembranen. Neutrale molekyler har den letteste passage. Interessant nok har man observeret, at molekyler med en svag positiv ladning, ofte fra en tertiær amin, kan have forbedret permeabilitet.
- Begrænset Molekylær Fleksibilitet: Antallet af roterbare bindinger i et molekyle er også en vigtig faktor. Et meget fleksibelt molekyle kan folde sig sammen til en større, mere klodset form, som har sværere ved at passere. CNS-lægemidler har typisk færre roterbare bindinger (ofte fem eller færre) sammenlignet med andre lægemiddelklasser.
Udfordringer i Blodbanen: Før Ankomst til Hjernen
Selv hvis et lægemiddel er perfekt designet til at krydse BBB, står det over for udfordringer i selve blodbanen. Et af de største problemer er binding til serumproteiner. Human Serum Albumin (HSA) er det mest udbredte protein i blodet og har en tendens til at binde sig til mange lægemidler. Når et lægemiddelmolekyle er bundet til et kæmpe protein som HSA, bliver det effektivt for stort til at krydse barrieren. Selvom denne binding er reversibel, reducerer den drastisk koncentrationen af frit, tilgængeligt lægemiddel, der kan nå hjernen.
Desuden spiller lægemidlets samlede farmakokinetiske profil (ADME: Absorption, Distribution, Metabolisme, Ekskretion) en afgørende rolle. Nogle gange kan forsøg på at øge lipofiliciteten for at forbedre hjerneoptag give bagslag. Et mere lipofilt lægemiddel kan for eksempel blive distribueret bredere til kroppens fedtvæv i stedet for at koncentrere sig i hjernen. Dette fænomen ses med visse prodrugs, hvor den øgede fedtopløselighed fører til, at stoffet ender i perifere væv, og den samlede terapeutiske effekt i hjernen ikke forbedres.
Aktive Transportmekanismer: Hjernens "VIP-Indgange"
Heldigvis er passiv diffusion ikke den eneste vej ind. Blod-hjerne-barrieren er udstyret med en række specialiserede transportproteiner, der aktivt flytter essentielle næringsstoffer som glukose, aminosyrer og vitaminer ind i hjernen. Medicinske kemikere forsøger at udnytte disse systemer ved at designe lægemidler, der efterligner disse naturlige substrater. Dette kaldes en "trojansk hest"-strategi. Ved at "forklæde" et lægemiddel som et næringsstof kan man få det transporteret aktivt over barrieren.
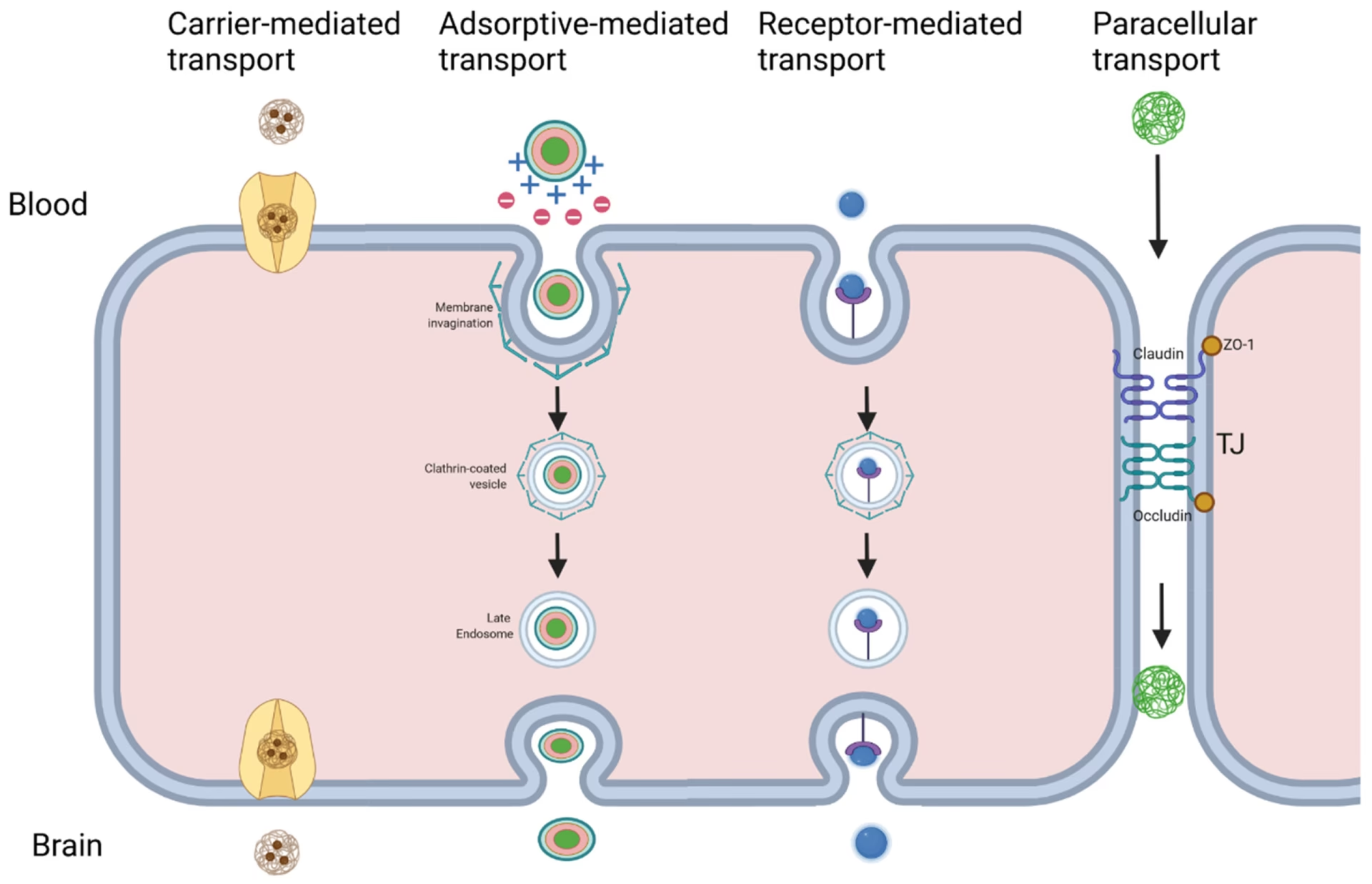
Disse transportører, kendt som Carrier-Mediated Transport (CMT) systemer, er yderst effektive og hurtige. De er kendetegnet ved deres transportkapacitet (Vmax) og deres affinitet for substratet (Km). En ideel strategi er at målrette en transportør med høj kapacitet og lav affinitet for at sikre, at lægemidlet effektivt kan konkurrere med de naturlige substrater.
Udforskning af Specifikke Transportører
Flere transportører er blevet identificeret som lovende mål for lægemiddel-levering:
- Glut1 (Glukosetransportør): Dette er en af de mest udbredte transportører i BBB og er ansvarlig for hjernens konstante forsyning af glukose. Forskere har forsøgt at koble lægemidler til glukosemolekyler. Udfordringen er dog, at selv små ændringer kan ødelægge affiniteten for Glut1, og det er kun små, hydrofile lægemidler, der med succes er blevet transporteret på denne måde.
- LAT1 (Aminosyretransportør): Denne transportør flytter store, neutrale aminosyrer. Det mest berømte eksempel på udnyttelse af LAT1 er L-DOPA, et prodrug til dopamin, der bruges til behandling af Parkinsons sygdom. Dopamin kan ikke selv krydse BBB, men L-DOPA ligner en aminosyre og transporteres effektivt ind i hjernen, hvor det omdannes til dopamin.
- MCT1 (Monocarboxylattransportør): Transporterer stoffer som laktat og pyruvat. Antiepileptikaet valproinsyre menes at bruge MCT1 til at komme ind i hjernen.
- ENT1 (Nukleosidtransportør): Ansvarlig for transport af nukleosider, som er byggesten til DNA og RNA. Visse antivirale midler og kemoterapeutika, der er nukleosidanaloger, kan udnytte denne vej.
Sammenligning af Vigtige BBB Transportører
| Transportør | Naturligt Substrat | Eksempler på Lægemidler/Prodrugs |
|---|---|---|
| Glut1 | D-Glukose | Visse glukose-konjugerede kemoterapeutika |
| LAT1 | Store neutrale aminosyrer (f.eks. Phenylalanin) | L-DOPA, Gabapentin, Melphalan |
| ENT1 | Nukleosider (f.eks. Adenosin) | Gemcitabin, Ribavirin |
| MCT1 | Monocarboxylsyrer (f.eks. Laktat) | Valproinsyre |
Fremtidsperspektiver og Overvejelser i Lægemiddeldesign
At designe lægemidler, der kan trænge ind i hjernen, er en delikat balancegang. Forskere skal ikke kun optimere molekylet til at krydse BBB, men også sikre, at det bevarer sin potens og selektivitet over for sit mål i hjernen. Derudover skal man overveje efflukspumper – en anden type transportører i BBB, der aktivt pumper fremmede stoffer ud af hjernen igen. At overvinde disse effluksmekanismer er en anden stor udfordring.
Fremtiden inden for CNS-lægemiddeludvikling ligger i en dybere forståelse af disse komplekse mekanismer. Ved at kombinere viden om passiv diffusion, udnyttelse af aktive transportører og omgåelse af efflukspumper kan vi håbe på at udvikle mere effektive behandlinger for de mest invaliderende neurologiske lidelser.
Ofte Stillede Spørgsmål (FAQ)
Hvad er blod-hjerne-barrieren (BBB)?
Blod-hjerne-barrieren er et tæt lag af specialiserede endotelceller, der omgiver blodkarrene i hjernen. Den fungerer som en meget selektiv, semipermeabel grænse, der beskytter hjernen mod potentielt skadelige stoffer i blodet, samtidig med at den tillader passage af essentielle næringsstoffer.

Hvorfor er det så svært for medicin at krydse BBB?
Det er svært på grund af barrierens unikke struktur. Cellerne er forbundet med "tight junctions", der forhindrer fri passage mellem cellerne. For at krydse barrieren skal et lægemiddel typisk passere direkte gennem cellerne, hvilket kræver specifikke fysisk-kemiske egenskaber, såsom lav molekylvægt, høj fedtopløselighed og en neutral ladning.
Hvad er Lipinskis "Rule of Five"?
Det er et sæt retningslinjer, der bruges i lægemiddeludvikling til at vurdere, om et kemisk stof sandsynligvis vil være et oralt aktivt lægemiddel hos mennesker. For BBB-penetration er reglerne endnu strengere, men de grundlæggende principper omhandler molekylvægt, lipofilicitet (logP), og antallet af brintbindingsdonorer og -acceptorer.
Kan man "snyde" blod-hjerne-barrieren?
Ja, det er den strategi, forskere forfølger. Ved at designe lægemidler (eller prodrugs), der ligner de naturlige molekyler, som hjernen har brug for (f.eks. aminosyrer eller glukose), kan man udnytte hjernens egne aktive transportsystemer til at fragte lægemidlet over barrieren. Dette er kendt som en "trojansk hest"-tilgang.
Hvis du vil læse andre artikler, der ligner Krydsning af blod-hjerne-barrieren: En guide, kan du besøge kategorien Medicin.
