12/03/2010
I hver eneste celle i vores krop findes et komplekst netværk af mikroskopiske porte og kanaler, der utrætteligt arbejder for at opretholde liv. Blandt de mest afgørende af disse er de spændingsafhængige calciumkanaler. Disse specialiserede proteiner fungerer som cellens dørvogtere, der nøje regulerer strømmen af calciumioner. Denne strøm er startsignalet for utallige biologiske processer, fra sammentrækningen af en muskel og frigivelsen af et hormon til overførslen af en nerveimpuls. Ny banebrydende forskning har kastet lys over en specifik type af disse kanaler, CaV2.3, og giver os en hidtil uset indsigt i, hvordan vores nervesystem fungerer, og hvad der går galt ved alvorlige sygdomme.
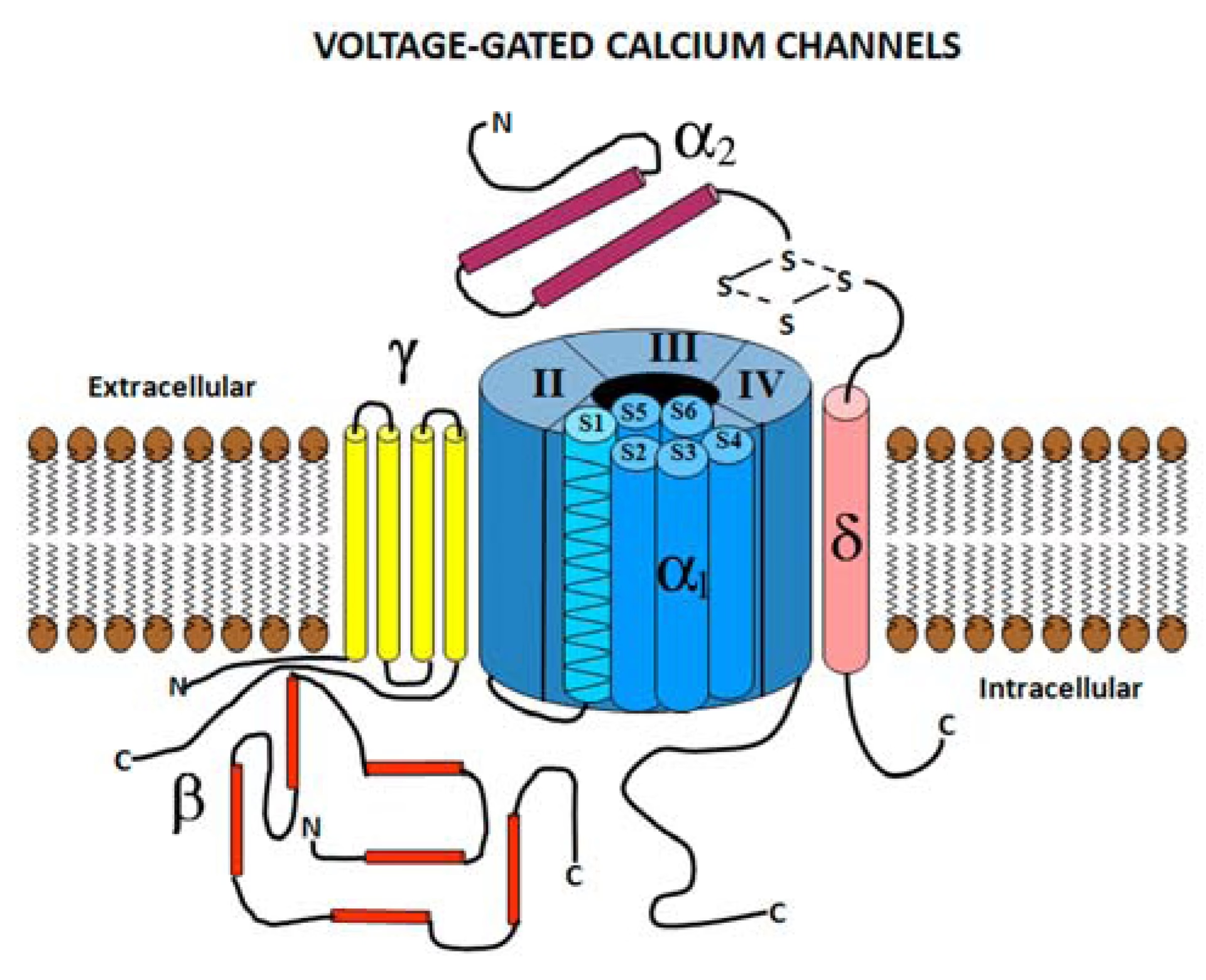
Hvad er Spændingsafhængige Calciumkanaler?
For at forstå vigtigheden af denne nye forskning, må vi først forstå, hvad disse kanaler er. Forestil dig en dæmning med en sluseport. Sluseporten åbner kun, når vandstanden (den elektriske spænding) på den ene side når et bestemt niveau. Når den åbner, strømmer vandet (calciumioner) igennem med stor kraft og sætter en række processer i gang nedenfor dæmningen. Det er præcis sådan, en spændingsafhængig calciumkanal virker i cellemembranen.
Disse kanaler er afgørende for kommunikationen mellem nerveceller. Når et elektrisk signal bevæger sig ned ad en nervecelle, får det calciumkanalerne i nerveenden til at åbne. Den pludselige indstrømning af calcium er det direkte signal, der får nervecellen til at frigive neurotransmittere – de kemiske budbringere, der sender signalet videre til den næste celle. Uden denne præcise mekanisme ville vores nervesystem simpelthen ikke kunne fungere.
Der findes flere familier af calciumkanaler, som hver især har specialiserede roller:
- CaV1-kanaler (L-type): Findes primært i muskler, herunder hjertemusklen, og er afgørende for muskelkontraktion. De er målet for mange velkendte blodtryks- og hjertemediciner.
- CaV2-kanaler (N-, P/Q- og R-type): Disse er stjernerne i nervesystemet og er altafgørende for frigivelsen af neurotransmittere. Den nye forskning fokuserer på CaV2.3, en R-type kanal.
- CaV3-kanaler (T-type): Spiller en vigtig rolle i at generere rytmiske elektriske signaler i celler, f.eks. i hjertets pacemakerceller og i visse områder af hjernen.
Et Dybdegående Kig på CaV2.3-kanalens Arkitektur
Ved hjælp af en avanceret teknik kaldet kryo-elektronmikroskopi (cryo-EM) er det lykkedes forskere at skabe et detaljeret 3D-billede af CaV2.3-kanalen. Dette er et enormt gennembrud, da det svarer til at få den komplette byggetegning til en yderst kompliceret maskine. Denne detaljerede struktur afslører præcis, hvordan kanalen er sammensat af forskellige underenheder, hvor poren, som calciumionerne strømmer igennem, er placeret, og hvordan de spændingsfølende dele er arrangeret.

Denne viden er uvurderlig. Den giver os mulighed for at forstå, hvorfor denne specifikke kanal opfører sig, som den gør, og hvorfor den adskiller sig fra andre calciumkanaler. Det er denne unikke opførsel, der gør den til en central spiller i hjernens funktioner.
Gåden om Lægemiddelresistens er Løst
En af de store udfordringer inden for medicin har været, at CaV2.3-kanalen er notorisk resistent over for mange eksisterende lægemidler, der ellers effektivt blokerer andre typer af calciumkanaler. Den nye 3D-struktur giver svaret på hvorfor. Ved at sammenligne 'låsen' (bindingsstedet for lægemidlet) på CaV2.3 med andre kanaler, kan forskerne se, at små, men afgørende, forskelle i aminosyrerne skaber en anden form. Lægemidlet, 'nøglen', passer simpelthen ikke i CaV2.3-kanalens lås. Denne indsigt i farmakoresistens er afgørende, for den betyder, at forskere nu kan begynde at designe nye lægemidler, der er skræddersyet til at passe præcist til CaV2.3-kanalens unikke struktur. Dette åbner op for udviklingen af mere specifikke behandlinger med færre bivirkninger.
Når Portene Fejler: Forbindelsen til Sygdom
Når byggetegningen til CaV2.3-kanalen indeholder fejl – altså genetiske mutationer – kan det have katastrofale konsekvenser. Forskning har allerede vist, at mutationer i genet, der koder for CaV2.3, er forbundet med alvorlige neurologiske lidelser, herunder visse former for udviklingsforstyrrelser og epilepsi. Med den nye 3D-struktur kan forskerne nu for første gang visualisere præcis, hvor i kanalen disse sygdomsfremkaldende mutationer sidder. Mange af dem er placeret nær den indre port, hvilket kan forklare, hvorfor de får kanalen til at opføre sig unormalt og blive overaktiv, hvilket kan føre til de ukontrollerede elektriske udladninger i hjernen, der ses ved epileptiske anfald.
En Unik 'Sikkerhedsmekanisme' Afsløret
En af de mest fascinerende opdagelser er relateret til, hvordan kanalen slukker sig selv. Dette kaldes inaktivering og er en vital sikkerhedsmekanisme, der forhindrer for meget calcium i at strømme ind i cellen, hvilket kan være giftigt. Forskningen afslører, at CaV2.3-kanalen har en unik dobbelt-mekanisme til at regulere denne proces. Ud over en kendt 'prop' (kaldet W-helix), der kan blokere kanalen indefra, har CaV2.3 en ekstra del, en såkaldt 'pre-W-helix'.

Denne 'pre-W-helix' fungerer som en regulator, der finjusterer, hvor effektivt proppen virker. Den kan enten konkurrere med proppen eller stabilisere den, afhængigt af cellens elektriske tilstand. Denne komplekse, finjusterede kontrolmekanisme er unik for CaV2.3 og kan forklare kanalens specifikke rolle i nervesystemet. Det er også et potentielt nyt mål for lægemidler; i stedet for at blokere kanalen helt, kan man måske udvikle medicin, der kun påvirker denne regulerende mekanisme.
Sammenligning af Calciumkanal-Familier
| Kanaltype | Almindeligt Navn | Primær Funktion | Eksempel på Lægemiddelmål |
|---|---|---|---|
| CaV1 | L-type | Muskelkontraktion, genekspression | Blodtryksmedicin (f.eks. Dihydropyridiner) |
| CaV2 | N-, P/Q-, R-type | Nervesignalering (synapser) | Visse smertestillende og antiepileptika |
| CaV3 | T-type | Rytmisk aktivitet (hjerte, hjerne) | Mål for fremtidige lægemidler |
Fremtidsperspektiver: Fra Grundforskning til Patientbehandling
Denne type grundforskning kan virke fjern fra hverdagens lægebesøg, men den er fundamentet for fremtidens medicin. Ved at forstå den præcise molekylære arkitektur af CaV2.3-kanalen, kan forskere nu udvikle præcisionsmedicin. Det er lægemidler, der er designet til at ramme én specifik type kanal eller endda en kanal med en specifik mutation. Dette kan føre til mere effektive behandlinger for en række neurologiske sygdomme med færre bivirkninger, da man undgår at påvirke andre vigtige kanaler i kroppen.
Forskningen i calciumkanaler er et perfekt eksempel på, hvordan en dybere forståelse af kroppens mindste byggeklodser kan have en revolutionerende indvirkning på vores evne til at bekæmpe sygdomme og forbedre menneskers livskvalitet.
Ofte Stillede Spørgsmål
Hvad er en ionkanal?
En ionkanal er et protein, der sidder i en celles membran og danner en pore eller kanal. Denne kanal kan åbne og lukke for at lade specifikke ioner (elektrisk ladede atomer som calcium, natrium eller kalium) passere ind eller ud af cellen. Denne strøm af ioner skaber de elektriske signaler, som celler, især nerveceller, bruger til at kommunikere.

Hvorfor er calcium så vigtigt for nerveceller?
I nerveceller fungerer calcium som en afgørende 'second messenger'. Når et elektrisk signal når enden af en nervecelle, åbner calciumkanalerne. Den efterfølgende indstrømning af calcium er det direkte signal, der udløser frigivelsen af neurotransmittere. Uden calcium ville nervecellerne ikke kunne sende signaler til hinanden, og hjernen og nervesystemet ville ikke fungere.
Kan jeg spise mere calcium for at hjælpe mine calciumkanaler?
Selvom calcium fra kosten er essentielt for knoglesundhed og generel kropsfunktion, vil det ikke løse problemer forårsaget af defekte calciumkanaler. Sygdomme som epilepsi, der er knyttet til kanalmutationer, skyldes ikke mangel på calcium i kroppen, men derimod en fejl i selve 'porten', der kontrollerer strømmen. Kroppen opretholder en meget streng balance af calcium i og uden for cellerne, en proces kendt som homeostase, og det er denne balance, der forstyrres af en defekt kanal.
Hvor lang tid går der, før denne forskning fører til nye lægemidler?
Udvikling af lægemidler er en lang og kompleks proces, der ofte tager et årti eller mere. Denne type grundforskning er det afgørende første skridt, da den identificerer et mål og giver den nødvendige viden til at designe potentielle lægemidler. Selvom der ikke er en ny pille på apoteket i morgen, har denne forskning lagt fundamentet for en helt ny generation af behandlinger for neurologiske lidelser.
Hvis du vil læse andre artikler, der ligner Calciumkanalernes Hemmelighed: Nøglen til Nervesystemet, kan du besøge kategorien Sundhed.
