19/12/2003
Antibiotika har i årtier været en hjørnesten i moderne medicin, der har reddet utallige liv og gjort komplekse kirurgiske indgreb sikre. Men denne æra er truet. Fremkomsten af antibiotikaresistens, hvor bakterier udvikler forsvar mod vores mest effektive lægemidler, udgør en af de største sundhedskriser i det 21. århundrede. Mens udviklingen af nye antibiotika er gået i stå, spreder resistente bakterier sig globalt. I denne kamp mod superbakterier er forskere begyndt at hente inspiration fra kræftbehandling for at udvikle et nyt, præcisionsstyret våben: Antistof-Antibiotika-Konjugater (AAC'er).
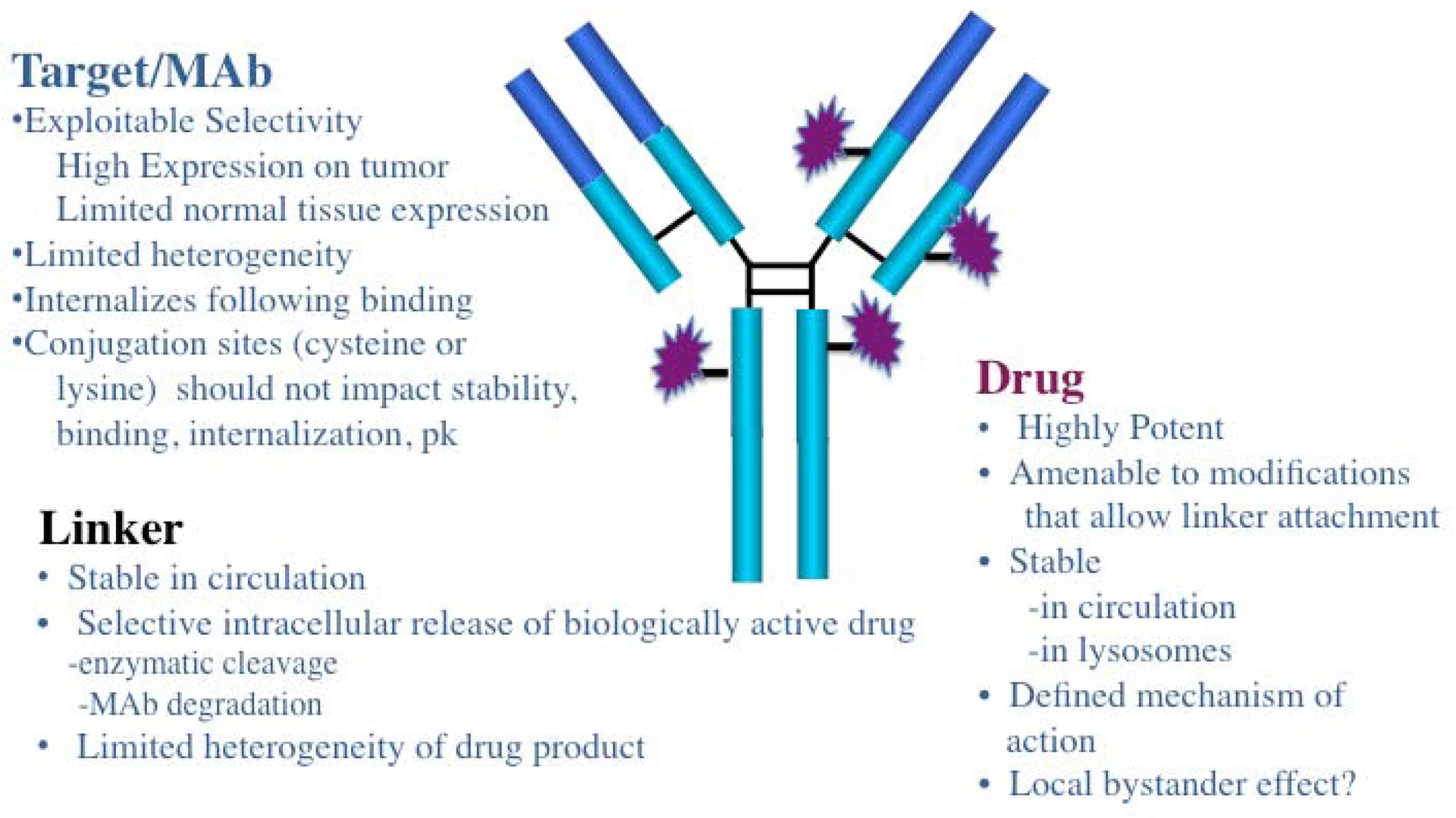
Ideen er både elegant og kraftfuld: Tænk på det som en 'smart bombe', der er designet til at levere en potent dosis antibiotika direkte til de invaderende bakterier, uden at skade kroppens egne celler eller den gavnlige tarmflora. Ved at kombinere antistoffers utrolige specificitet med antibiotikas dræbende effekt, åbner AAC'er op for en ny frontlinje i behandlingen af infektionssygdomme, især dem forårsaget af multiresistente patogener.
Hvad er et Antistof-Antibiotika-Konjugat (AAC)?
Et AAC er et komplekst, bioingeniør-designet molekyle, der består af tre afgørende komponenter, som arbejder i perfekt synergi. Hver del har en unik og uundværlig funktion for den samlede effekt.
1. Antistoffet: Målsøgningssystemet
Kernen i et AAC er et monoklonalt antistof (mAb). Antistoffer er proteiner, som kroppens immunsystem naturligt producerer for at identificere og neutralisere fremmede trusler som bakterier og vira. I et AAC fungerer antistoffet som et yderst præcist målsøgningssystem. Det er designet til specifikt at genkende og binde sig til et unikt molekyle, et såkaldt antigen, der kun findes på overfladen af den specifikke bakterie, man ønsker at bekæmpe. Det ideelle antigen er rigeligt til stede på bakterien i alle infektionsstadier, men fraværende på menneskelige celler for at undgå utilsigtede skader. Ofte anvendes IgG1-isotypen af antistoffer, da den har en lang halveringstid i blodet og effektivt kan aktivere andre dele af immunsystemet.
2. Antibiotikummet: Den potente last
Den anden komponent er selve antibiotikummet, ofte kaldet 'payload' eller last. Dette er den aktive, bakteriedræbende del af konjugatet. En af de store fordele ved AAC-teknologien er, at den gør det muligt at anvende ekstremt potente antibiotika, som måske tidligere er blevet kasseret på grund af for høj toksicitet, når de blev givet systemisk. Fordi antibiotikummet leveres målrettet direkte til bakterien, kan man bruge meget lavere samlede doser, hvilket minimerer bivirkninger. Antibiotikummet skal være stabilt, kunne kobles kemisk til antistoffet og bevare sin dræbende effekt i det sure miljø inde i en værtscelle, hvor bakterier ofte gemmer sig.

3. Linkeren: Den intelligente kobling
Den sidste, men lige så vigtige, del er linkeren. Dette er den kemiske bro, der forbinder antistoffet med antibiotikummet. Linkeren har en dobbeltrolle, der er afgørende for succesen. For det første skal den være ekstremt stabil i blodbanen. Hvis antibiotikummet frigives for tidligt, mister AAC'et sin præcision og kan forårsage skade på raske væv. For det andet skal linkeren være designet til at blive brudt (eller 'kløvet') under de specifikke forhold, der findes på destinationen – typisk inde i den værtscelle, der har optaget bakterien. Der findes forskellige typer linkere, herunder:
- Syrefølsomme linkere: Brydes i det sure miljø i cellens lysosomer.
- Enzymfølsomme linkere: Designet til at blive kløvet af specifikke enzymer, såsom cathepsiner, der findes i høje koncentrationer inde i fagocytter (immunceller, der 'spiser' bakterier).
- Ikke-kløvbare linkere: Her frigives antibiotikummet først, når hele antistoffet nedbrydes inde i cellen.
Samspillet mellem disse tre dele skaber et yderst sofistikeret lægemiddel, der lover at revolutionere behandlingen af svære infektioner.
Hvordan virker AAC'er? En trin-for-trin mekanisme
Den måde, et AAC bekæmper en infektion på, er en flertrinsproces, der udnytter både avanceret bioteknologi og kroppens egne immunmekanismer.
- Målsøgning og binding: AAC'et cirkulerer i blodet i en inaktiv tilstand. Når det møder den målbakterie, det er designet til at genkende, binder antistof-delen sig fast til bakteriens overfladeantigener. Denne proces kaldes opsonisering og 'mærker' bakterien for immunsystemet.
- Optagelse i værtsceller: Bakterier, især genstridige patogener som Staphylococcus aureus, kan gemme sig inde i kroppens egne celler (f.eks. immunceller som makrofager) for at undgå antibiotika og immunforsvaret. En AAC-mærket bakterie bliver hurtigt genkendt og optaget af disse celler gennem en proces kaldet fagocytose.
- Intracellulær transport: Inde i værtscellen bliver bakterien indesluttet i en lille blære kaldet et fagosom. Dette fagosom smelter efterfølgende sammen med et lysosom, der er fyldt med nedbrydende enzymer og har et meget surt miljø.
- Frigivelse af antibiotikum: I det barske miljø i fagolysosomet aktiveres linkeren. Enzymer som cathepsin klipper den over, og det potente antibiotikum frigives fra antistoffet.
- Bakteriedrab: Det nu frie og aktive antibiotikum er fanget inde i værtscellen i en høj koncentration, lige præcis der hvor de intracellulære bakterier gemmer sig. Dette fører til en effektiv eliminering af de skjulte bakterier, som almindelige antibiotika ofte har svært ved at nå.
Sammenligning: Konventionelle Antibiotika vs. AAC'er
For at forstå potentialet fuldt ud er det nyttigt at sammenligne AAC'er med traditionelle antibiotikabehandlinger.
| Egenskab | Konventionelle Antibiotika | Antistof-Antibiotika-Konjugater (AAC'er) |
|---|---|---|
| Specificitet | Bredspektret, påvirker mange forskellige bakterier. | Høj-specifik, rammer kun en bestemt type bakterie. |
| Effekt på Mikrobiota | Skader ofte den gavnlige tarmflora, hvilket kan føre til dysbiose og infektioner som C. difficile. | Minimal påvirkning af kroppens gavnlige bakterier. |
| Effekt mod Intracellulære Bakterier | Ofte begrænset, da mange antibiotika har svært ved at trænge ind i værtsceller. | Meget effektiv, da mekanismen er designet til at frigive antibiotika inde i cellerne. |
| Bivirkninger | Kan være betydelige på grund af systemisk eksponering og 'off-target' effekter. | Potentielt færre bivirkninger på grund af målrettet levering. |
| Udvikling af Resistens | Højt selektionstryk, da mange bakterier udsættes for lægemidlet. | Lavere selektionstryk, da kun målbakterien eksponeres. |
| Produktionsomkostninger | Relativt lave for etablerede antibiotika. | Meget høje på grund af den komplekse bioteknologiske proces. |
Casestudie: DSTA4637A mod MRSA
Et af de mest lovende eksempler på et AAC i udvikling er DSTA4637A, som er designet til at bekæmpe methicillin-resistent Staphylococcus aureus (MRSA). MRSA er en berygtet superbakterie, der forårsager alvorlige og livstruende infektioner på hospitaler og i samfundet.

- Antistof: DSTA4637A bruger et humant monoklonalt antistof, der specifikt genkender et molekyle kaldet vægteichoinsyre (WTA) på overfladen af S. aureus.
- Antibiotikum: Lasten er et yderst potent rifamycin-derivat, der er effektivt mod MRSA i meget lave koncentrationer.
- Linker: En enzymfølsom valin-citrullin linker, der specifikt kløves af cathepsiner inde i fagolysosomet.
Studier har vist imponerende resultater. I dyremodeller var en enkelt dosis af DSTA4637A markant mere effektiv til at fjerne MRSA-bakterier fra organer som hjerte, nyrer og knogler end standardbehandlingen med vancomycin, der blev givet to gange dagligt. Et fase 1-studie i raske frivillige har desuden vist, at lægemidlet er sikkert og veltolereret, hvilket baner vejen for videre klinisk udvikling. Dette casestudie illustrerer perfekt, hvordan AAC-teknologien kan overvinde de udfordringer, der er forbundet med at behandle antibiotikaresistens og infektioner med intracellulære bakterier.
Udfordringer og Fremtidsperspektiver
Selvom potentialet er enormt, står AAC-teknologien over for flere udfordringer. Den mest markante er de høje produktionsomkostninger. Fremstillingen af et AAC er en kompleks, flertrins-proces, der involverer produktion af både et antistof og et specialdesignet antibiotika-linker-molekyle, som derefter skal kobles sammen under nøje kontrollerede forhold. Dette gør behandlingen dyr sammenlignet med traditionelle antibiotika.
En anden udfordring er behovet for hurtig og præcis diagnostik. Fordi AAC'er er så specifikke, er det afgørende at vide præcis, hvilken bakterie der forårsager infektionen, før behandlingen kan startes. Dette kan være en barriere i akutte situationer, hvor man ofte starter med bredspektret antibiotika.
Fremtiden ser dog lys ud. Forskere arbejder på at udvide teknologien til at bekæmpe andre farlige patogener som Pseudomonas aeruginosa og endda ikke-bakterielle infektioner som parasitter (f.eks. sovesyge) og vira. Derudover undersøges muligheden for at bruge andre 'payloads' end traditionelle antibiotika, såsom antimikrobielle peptider. Hvis omkostningerne kan reduceres, og diagnostikken forbedres, kan antistof-antibiotika-konjugater meget vel blive et af vores vigtigste redskaber i den fortsatte kamp mod infektionssygdomme.
Ofte Stillede Spørgsmål
- Er AAC'er en erstatning for almindelige antibiotika?
- Ikke nødvendigvis en fuld erstatning, men snarere et specialiseret og kraftfuldt supplement. De vil sandsynligvis blive brugt til at behandle alvorlige, svært tilgængelige eller multiresistente infektioner, hvor traditionelle antibiotika kommer til kort. For simple, ukomplicerede infektioner vil almindelige antibiotika fortsat være førstevalg.
- Hvorfor er de så dyre at producere?
- Produktionen er en avanceret bioteknologisk proces. Den involverer separat fremstilling af tre komplekse dele: et monoklonalt antistof (typisk i cellekulturer), et kemisk syntetiseret antibiotikum-linker-molekyle, og en efterfølgende præcis konjugeringsproces for at forbinde dem. Hvert trin kræver streng kvalitetskontrol og specialiseret udstyr, hvilket driver omkostningerne op.
- Hvornår kan vi forvente at se disse behandlinger på markedet?
- Det er svært at sætte en præcis tidslinje. Flere AAC'er, som DSTA4637A, er i øjeblikket i kliniske forsøg på mennesker. Lægemiddeludvikling er en lang proces, der tager mange år, men de lovende tidlige resultater giver håb om, at de første AAC'er mod bakterielle infektioner kan blive godkendt inden for det næste årti.
Hvis du vil læse andre artikler, der ligner Antistof-konjugater: Nyt håb mod infektioner, kan du besøge kategorien Medicin.
