24/07/2022
Allergiske sygdomme er komplekse lidelser, hvis oprindelse og udvikling involverer en indviklet sammenspil mellem genetiske og miljømæssige faktorer. Selvom vores medfødte og adaptive immunsystem er afgørende for at regulere vores tilpasning til det ydre mikromiljø, betragtes allergiske sygdomme som en betydelig årsag til immun dysfunktion. Denne dysfunktion opstår fra interaktioner mellem flere gener og det ydre miljø i vores celler. Forskning inden for genetik og epigenetik har markant fremmet vores forståelse af disse sygdomme og har lagt fundamentet for at udforske den genetiske baggrund for allergier. I denne artikel vil vi udforske de mange facetter af allergiens patogenese, fra genetisk arv til cellulære signalveje og mikrobiotaens rolle.
Genetiske og Epigenetiske Faktorer
Forskningen inden for genetik og epigenetik har revolutioneret vores forståelse af allergiske sygdomme. Anvendelsen af genom-brede associationsstudier (GWAS), analyse af enkeltnukleotidpolymorfier (SNP) og epigenom-brede associationsstudier (EWAS) har skabt et solidt grundlag for at udforske den genetiske basis for disse lidelser. Epigenetik, som omfatter DNA-methylering, post-translationelle histonmodifikationer og ikke-kodende RNA'er, kan forklare, hvordan miljøet påvirker udviklingen af allergiske sygdomme og belyse mekanismerne bag immunsystemets plasticitet.
Arvelighedsstudier: Tvillinger afslører genetisk indflydelse
Det er ofte svært at adskille den uafhængige rolle af genetik og miljø i allergiske sygdomme. Tvillingerstudier er et værdifuldt værktøj til dette, da de kan hjælpe med at isolere genetiske faktorer. Studier af tvillinger har vist, at fødevareallergi (FA) har en høj arvelighed. For eksempel er konkordansraten for jordnøddeallergi hos enæggede tvillinger 82%, hvilket er langt højere end de 20% observeret hos tveæggede tvillinger. Børn, hvis forældre eller søskende har jordnøddeallergi, har syv gange større sandsynlighed for selv at udvikle sygdommen. Generelt anslås arveligheden for fødevareallergi at være så høj som 81%, mens den for allergisk rhinitis (AR) anslås til ca. 91%.
SNPs og GWAS-analyser i allergiske sygdomme
Enkeltnukleotidpolymorfier (SNPs) er de mest almindelige former for genetisk variation i det menneskelige genom. Disse variationer kan findes i forskellige regioner af genomet og betragtes som grundlaget for DNA-sekvensvariation. GWAS-studier har identificeret adskillige genetiske varianter associeret med allergiske sygdomme.
- Atopisk Dermatitis (AD): Mindst 34 loci og 46 gener er blevet identificeret som risikofaktorer for AD i forskellige befolkninger. Den vigtigste genetiske risikofaktor er tab-af-funktion mutationer i FLG-genet, der koder for filaggrin, et protein afgørende for hudbarrieren.
- Astma: Gener som IL1RL1, HLA-DQA1, IL33 og GSDMA er blevet associeret med astma. Specifikt er 17q12-q21-locus, der indeholder gener som ORMDL3 og GSDMB, stærkt forbundet med barndomsastma.
- Allergisk Rhinitis (AR): Store GWAS-studier har afsløret 20 nye loci associeret med AR-risiko, herunder gener involveret i både det medfødte og adaptive immunsystem, såsom IL7R og CXCR5.
Mitokondriel Arv i Allergiske Sygdomme
Mitokondrier arves primært fra moderen, og mitokondriel arv er tæt forbundet med forekomsten af astma. Varianter i mitokondrielt DNA (mtDNA) er signifikant associeret med allergiske lidelser. For eksempel kan dysfunktion af specifikke mitokondrielle gener være forbundet med astma hos kvinder, mens mutationer i andre gener kan føre til astma hos mænd gennem ændringer i reaktive iltarter (ROS).
Epigenetikkens Rolle: Når Miljøet Ændrer Genekspression
Epigenetik refererer til arvelige ændringer, der påvirker genekspression uden at ændre selve DNA-sekvensen. Disse mekanismer er afgørende for at forstå, hvordan miljøet interagerer med vores gener for at forårsage sygdom.
DNA-methylering
DNA-methylering er en proces, hvor en methylgruppe tilføjes til DNA, hvilket typisk fører til undertrykkelse af gentranskription. Ændringer i DNA-methylering er blevet observeret i mange allergiske sygdomme. For eksempel er promotoren for TSLP-genet, et nøglemolekyle i allergisk inflammation, hypomethyleret i beskadiget hud hos patienter med atopisk dermatitis. I astma er hypermethylering af kromosom 17q12-q21, en velkendt astma-risikoregion, blevet forbundet med sygdommens patogenese. Disse ændringer kan fungere som biomarkører og potentielle terapeutiske mål.
Histonmodifikationer
DNA i vores celler er pakket omkring proteiner kaldet histoner. Kemiske modifikationer af disse histoner, såsom acetylering og methylering, kan ændre, hvor tæt DNA'et er pakket, og dermed påvirke genekspression. I astmapatienter er der observeret øgede niveauer af visse histonmodifikationer i epitelceller, hvilket fører til ændret ekspression af gener relateret til inflammation. En ubalance mellem enzymer, der tilføjer (HATs) og fjerner (HDACs) acetylgrupper, menes at være en afgørende faktor i astma.
Centrale Signalveje i Allergiske Sygdomme
Intercellulær kommunikation sker via komplekse signalveje. Dysregulering af disse veje spiller en central rolle i udviklingen af allergiske sygdomme. Forståelse af disse signalveje er afgørende for udviklingen af målrettede terapier.

JAK/STAT-signalvejen
Janus kinase/signaltransducer og aktivator af transkription (JAK/STAT) vejen er en hurtig rute fra cellemembranen til kernen, der regulerer mange gener involveret i inflammation. Cytokiner, der er centrale for allergiske reaktioner, såsom IL-4, IL-5 og IL-13, signalerer gennem JAK/STAT-vejen. Aktivering af denne vej er afgørende for differentieringen af T-hjælper 2 (Th2) celler, som er de primære drivkræfter bag allergisk inflammation. Hæmmere af JAK-kinaser er derfor blevet en lovende ny behandlingsform for sygdomme som atopisk dermatitis.
NF-κB/MAPK-signalvejen
NF-κB (nukleær faktor kappa B) er en proteinkompleks, der kontrollerer transkriptionen af DNA og er involveret i immunresponser over for infektion og inflammation. I astma kontrollerer NF-κB/MAPK-vejen inflammation ved at regulere produktionen af pro-inflammatoriske cytokiner som TNF-α og IL-6. Aktivering af NF-κB er blevet observeret i inflammatoriske celler fra astmapatienter og i dyremodeller for allergi, hvilket understreger dens centrale rolle.
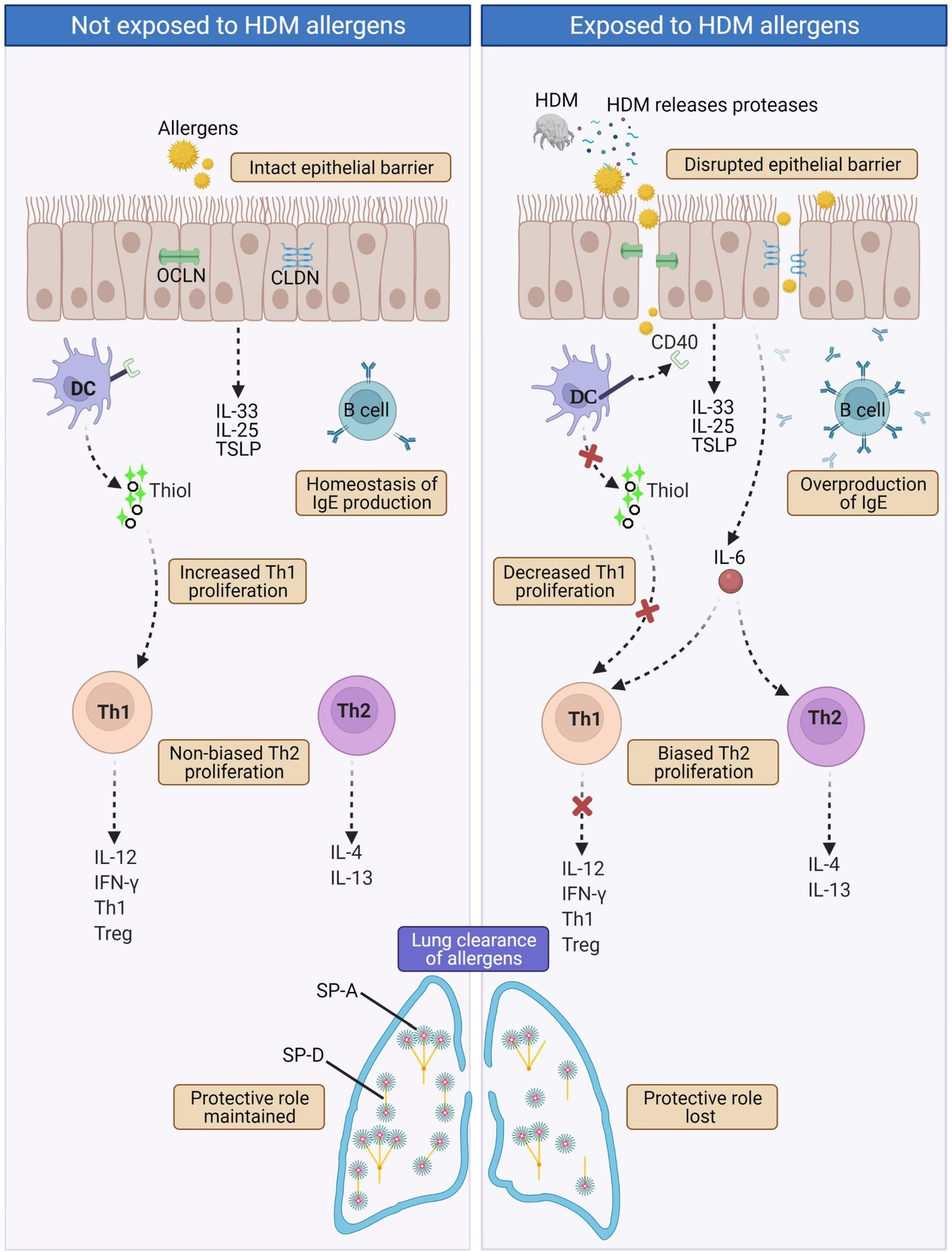
TOLL-lignende receptor (TLR) signalvej
TLR'er er en klasse af proteiner, der spiller en nøglerolle i det medfødte immunsystem. De er receptorer, der genkender molekylære mønstre associeret med patogener. Styrken af TLR-signalering kan afgøre, om en immunrespons bliver allergisk (Th2-domineret) eller beskyttende (Th1-domineret). Lave niveauer af TLR-stimulering kan fremme allergi, mens stærk stimulering kan beskytte mod det. Dette er en del af grundlaget for "hygiejnehypotesen", som postulerer, at reduceret eksponering for mikrober i den tidlige barndom kan øge risikoen for allergiske sygdomme.
Mikrobiotaens Indflydelse
Den samling af mikroorganismer, der lever i og på vores krop, kendt som mikrobiota, har en dybtgående indflydelse på vores immunsystem. En ubalance i mikrobiotaen, eller dysbiose, er i stigende grad blevet forbundet med udviklingen af allergiske sygdomme.

Hygiejnehypotesen og Dysbiose
Den oprindelige hygiejnehypotese foreslog, at færre infektioner i den tidlige barndom førte til en øget forekomst af allergiske sygdomme. Denne hypotese er blevet udvidet til at omfatte vigtigheden af eksponering for en mangfoldig mikrobiota. Faktorer som kejsersnit, brug af antibiotika og en vestlig diæt kan reducere mikrobiel diversitet tidligt i livet, hvilket kan forringe udviklingen af immun tolerance og øge risikoen for allergi. Studier har vist, at spædbørn med lavere diversitet i tarmmikrobiotaen har en højere risiko for at udvikle astma og atopisk dermatitis.
Mikrobiotaens Rolle for Immunsystemet
Tarmmikrobiotaen træner immunsystemet til at skelne mellem harmløse og skadelige antigener. Visse bakterier kan fremme udviklingen af regulatoriske T-celler (Tregs), som er afgørende for at undertrykke uønskede immunresponser, herunder allergiske reaktioner. Metabolitter produceret af tarmbakterier, såsom kortkædede fedtsyrer (SCFA'er), har anti-inflammatoriske egenskaber og kan påvirke immunceller i hele kroppen, herunder i lungerne, via den såkaldte "tarm-lunge-akse".
De Cellulære Mekanismer og Allergiske Reaktioner
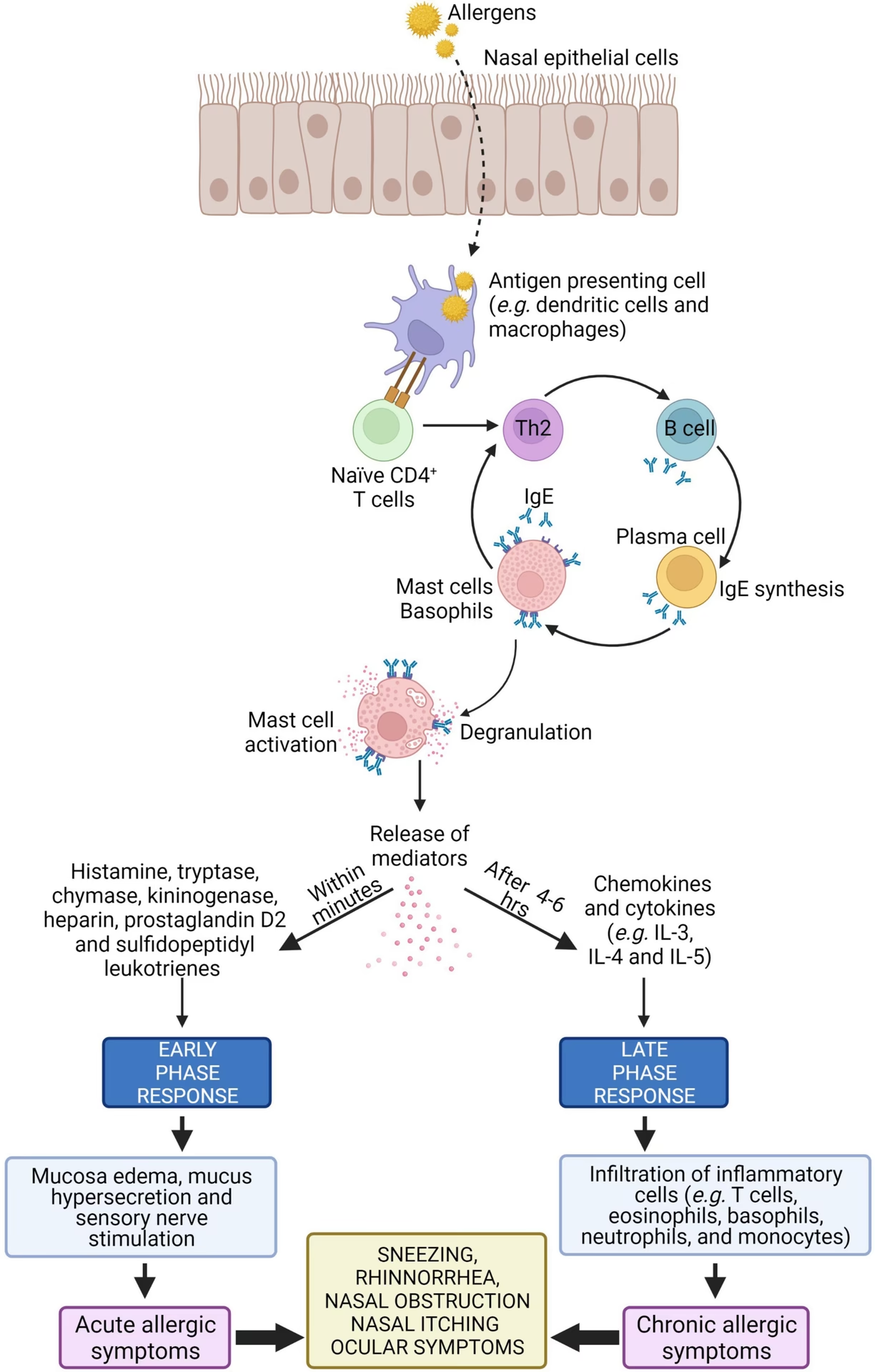
Den allergiske inflammation er resultatet af et komplekst samspil mellem flere inflammatoriske celler, herunder mastceller, basofiler, lymfocytter og eosinofiler. Disse celler producerer en kaskade af mediatorer, der forårsager symptomerne på allergi.
Typer af Overfølsomhedsreaktioner
Allergi er en form for overfølsomhed. Disse reaktioner kan klassificeres i fire hovedtyper baseret på den involverede immunmekanisme.

| Overfølsomhedstype | Immunreaktant | Antigentype | Effektormekanisme | Eksempel |
|---|---|---|---|---|
| Type 1: Allergi | IgE | Opløseligt antigen | Mastceller | Anafylaksi, høfeber |
| Type 2: Lægemiddelallergi | IgG | Lægemiddel bundet til celleoverflade | Komplement/Fagocytose | Penicillinallergi |
| Type 3: Serumssyge | IgG | Opløseligt antigen | Immunkomplekser | Arthus-reaktion i huden |
| Type 4: Forsinket type | T-celler | Opløseligt eller celle-associeret antigen | Inflammation, celledød | Kontakt dermatitis, kronisk astma |
Den Akutte og Kroniske Allergiske Reaktion
Allergiske reaktioner har typisk to faser:
- Den akutte fase (urticaria/kvadel): Denne fase opstår hurtigt efter eksponering for et allergen (typisk inden for en time). Den skyldes degranulering af mastceller, som frigiver histamin og andre mediatorer. Histamin forårsager lokal inflammation, rødme og hævelse. Denne reaktion er hurtig, fordi allergenet binder til IgE-antistoffer, der allerede sidder på overfladen af mastcellerne.
- Den kroniske fase (flare/opblussen): Denne fase udvikler sig typisk 6-12 timer efter den indledende eksponering. Det er en cellulær respons, der involverer rekruttering af T-celler, eosinofiler og flere mastceller til eksponeringsstedet. Disse celler frigiver enzymer, toksiske proteiner og flere cytokiner, hvilket fører til vedvarende inflammation og vævsskade.
Ofte Stillede Spørgsmål
Hvad er en allergen?
Et allergen er et normalt harmløst stof, der kan udløse en allergisk reaktion hos en disponeret person. Almindelige allergener er små, opløselige og stabile proteiner fra kilder som pollen, husstøvmider, kæledyr og fødevarer. Der er ingen enkelt strukturel egenskab, der definerer et protein som værende allergifremkaldende.
Hvorfor udvikler nogle mennesker allergi, mens andre ikke gør?
Dette skyldes et komplekst samspil mellem genetisk disposition og miljømæssige faktorer. En persons gener kan gøre dem mere tilbøjelige til at udvikle en Th2-domineret immunrespons, som er karakteristisk for allergi. Miljøfaktorer i det tidlige liv, såsom eksponering for mikrober og kost, spiller en afgørende rolle i at forme immunsystemet og bestemme, om denne genetiske disposition kommer til udtryk.
Hvad er forskellen på en akut og en kronisk allergisk reaktion?
Den akutte reaktion er øjeblikkelig og medieret af forudformede stoffer som histamin fra mastceller, hvilket forårsager symptomer som kløe, hævelse og rødme. Den kroniske reaktion er forsinket og skyldes rekruttering af inflammatoriske celler som T-celler og eosinofiler, hvilket fører til vedvarende inflammation og potentielt vævsskade.
Kan man vokse fra en allergi?
Ja, det er muligt, især med visse fødevareallergier som mælke- og ægallergi hos børn. Dette sker, fordi immunsystemet kan udvikle tolerance over tid. For andre allergier, som f.eks. jordnøddeallergi eller pollenallergi, er det mindre almindeligt at vokse fra dem, men symptomerne kan ændre sig over et livsforløb.
Hvis du vil læse andre artikler, der ligner Allergiens Oprindelse: Gener, Miljø og Immunsystem, kan du besøge kategorien Allergi.
