13/02/2024
Sikkerheden og kvaliteten af medicin på det danske marked er af allerhøjeste prioritet. En central aktør i at opretholde denne standard er Lægemiddelstyrelsen. Når der opstår en mistanke om, at et lægemiddel har en kvalitetsfejl, der potentielt kan skade patienter, er det afgørende, at de relevante parter handler hurtigt og korrekt. Dette indebærer en øjeblikkelig kontakt til myndighederne for at vurdere situationen og om nødvendigt igangsætte en tilbagekaldelse fra markedet. At vide præcis, hvordan og hvornår man skal kontakte Lægemiddelstyrelsen, er essentiel viden for medicinalvirksomheder, apoteker og grossister.
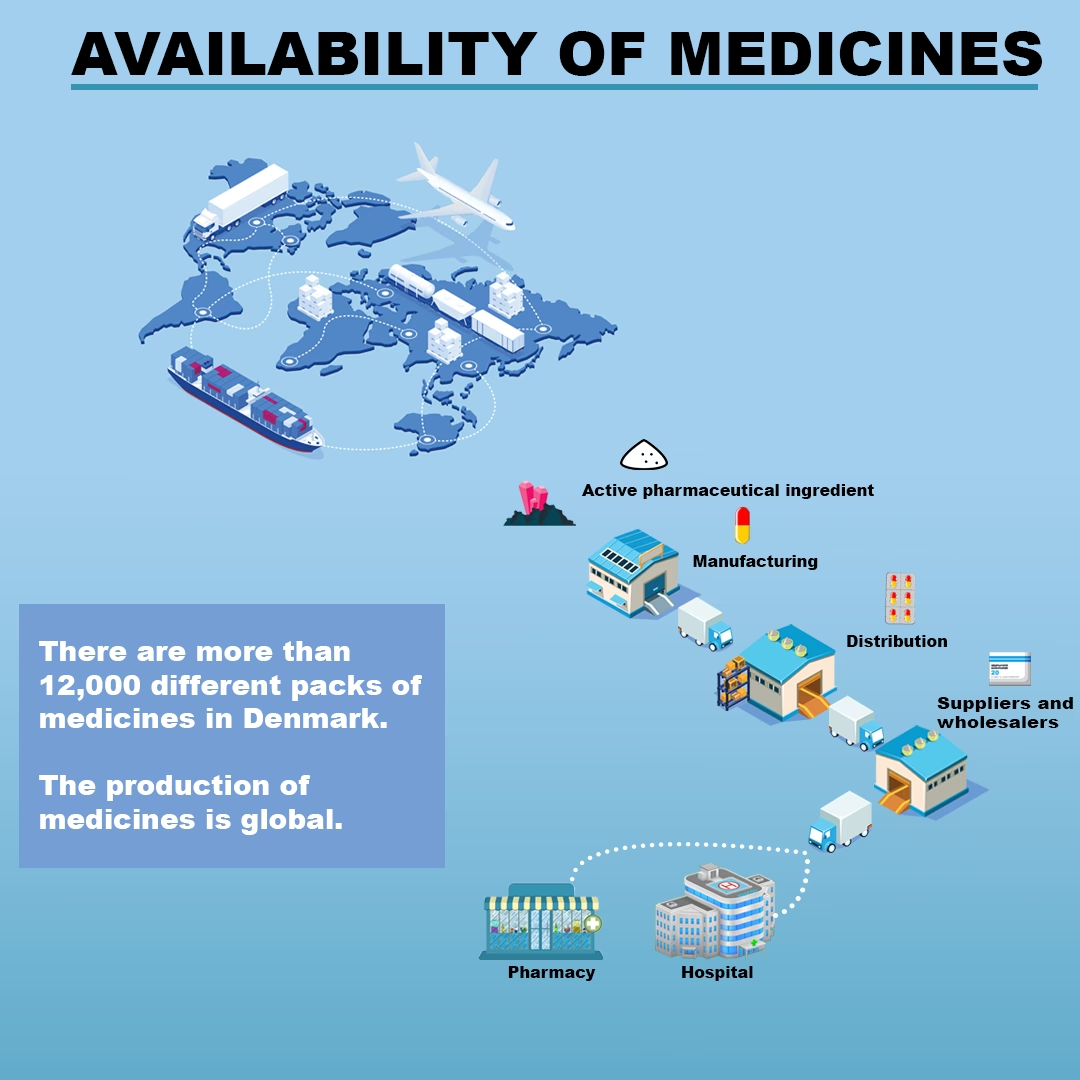
Denne artikel fungerer som en omfattende guide til den korrekte procedure for at indberette en potentiel kvalitetsfejl, der kan føre til en tilbagekaldelse af et lægemiddel. Vi vil dække, hvem der har ansvaret, hvilke situationer der kræver kontakt, den specifikke kontaktinformation og hvad man kan forvente, at der sker efterfølgende.
Forståelse af Kvalitetsfejl og Tilbagekaldelse
Før vi dykker ned i kontaktproceduren, er det vigtigt at definere, hvad en kvalitetsfejl er i denne sammenhæng. En kvalitetsfejl er en afvigelse fra produktets specifikationer eller fremstillingsproces, som kan påvirke dets sikkerhed, kvalitet eller virkning. Det er ikke det samme som en bivirkning, som er en uønsket reaktion på et korrekt fremstillet lægemiddel.
Eksempler på kvalitetsfejl kan omfatte:
- Forurening med fremmedlegemer eller mikroorganismer.
- Forkert styrke eller dosis i tabletten/væsken.
- Fejl på emballagen, der kompromitterer produktets holdbarhed (f.eks. en utæt forsegling).
- Trykfejl på pakningen, der angiver forkert information.
- Problemer med produktets fysiske egenskaber (f.eks. uventet farveændring eller opløsningstid).
Når en virksomhed, der er indehaver af markedsføringstilladelsen, bliver opmærksom på en sådan fejl, har de pligt til at informere Lægemiddelstyrelsen øjeblikkeligt.
Den Korrekte Kontaktprocedure til Lægemiddelstyrelsen
Hurtig og effektiv kommunikation er nøglen til at håndtere en potentiel tilbagekaldelse og minimere enhver risiko for patienterne. Processen er designet til at sikre, at Lægemiddelstyrelsen modtager al nødvendig information for at kunne foretage en hurtig risikovurdering.
Trin 1: Øjeblikkelig Telefonisk Kontakt
Ved alvorlige kvalitetsfejl, der kan medføre en tilbagekaldelse, skal Lægemiddelstyrelsen altid kontaktes telefonisk som det allerførste skridt. Dette sikrer den hurtigst mulige sagsbehandling.
Hovedtelefonnummer: +45 4488 9595
Når du ringer, skal du bede om at tale med den relevante afdeling for lægemiddelkontrol eller inspektion. Vær forberedt på at give følgende grundlæggende oplysninger:
- Dit navn, din virksomhed og din rolle.
- Navnet på det pågældende lægemiddel.
- Batch- eller lotnummer(e) der er berørt.
- En kort, præcis beskrivelse af den formodede kvalitetsfejl.
- En foreløbig vurdering af den potentielle risiko for patienter.
Kontakt Uden for Normal Arbejdstid
Patientsikkerhed følger ikke kontortider. Hvis en kritisk kvalitetsfejl opdages uden for Lægemiddelstyrelsens normale åbningstid (hverdage 8:30 - 16:00, fredag til 15:30), er der en vagtordning. Ved at ringe til hovednummeret (+45 4488 9595) vil en telefonsvarer oplyse om nummeret til den vagthavende medarbejder, som kan håndtere akutte sager relateret til tilbagekaldelser.
Trin 2: Skriftlig Opfølgning
Efter den indledende telefoniske kontakt skal der altid følges op med en skriftlig redegørelse. Denne sendes typisk via e-mail til den adresse, Lægemiddelstyrelsen oplyser under telefonsamtalen. Den skriftlige rapport bør indeholde en mere detaljeret beskrivelse af problemet, herunder:
- Alle detaljer om produktet (navn, styrke, form, batchnumre).
- En dybdegående beskrivelse af kvalitetsfejlen.
- Resultater af eventuelle indledende undersøgelser.
- Information om distributionen af de berørte batch(es) – hvor meget er der på markedet, og hvor er det distribueret?
- Virksomhedens egen risikovurdering og forslag til handling (f.eks. klassificering af tilbagekaldelsen).
- Et forslag til kommunikation til grossister, apoteker og eventuelt læger.
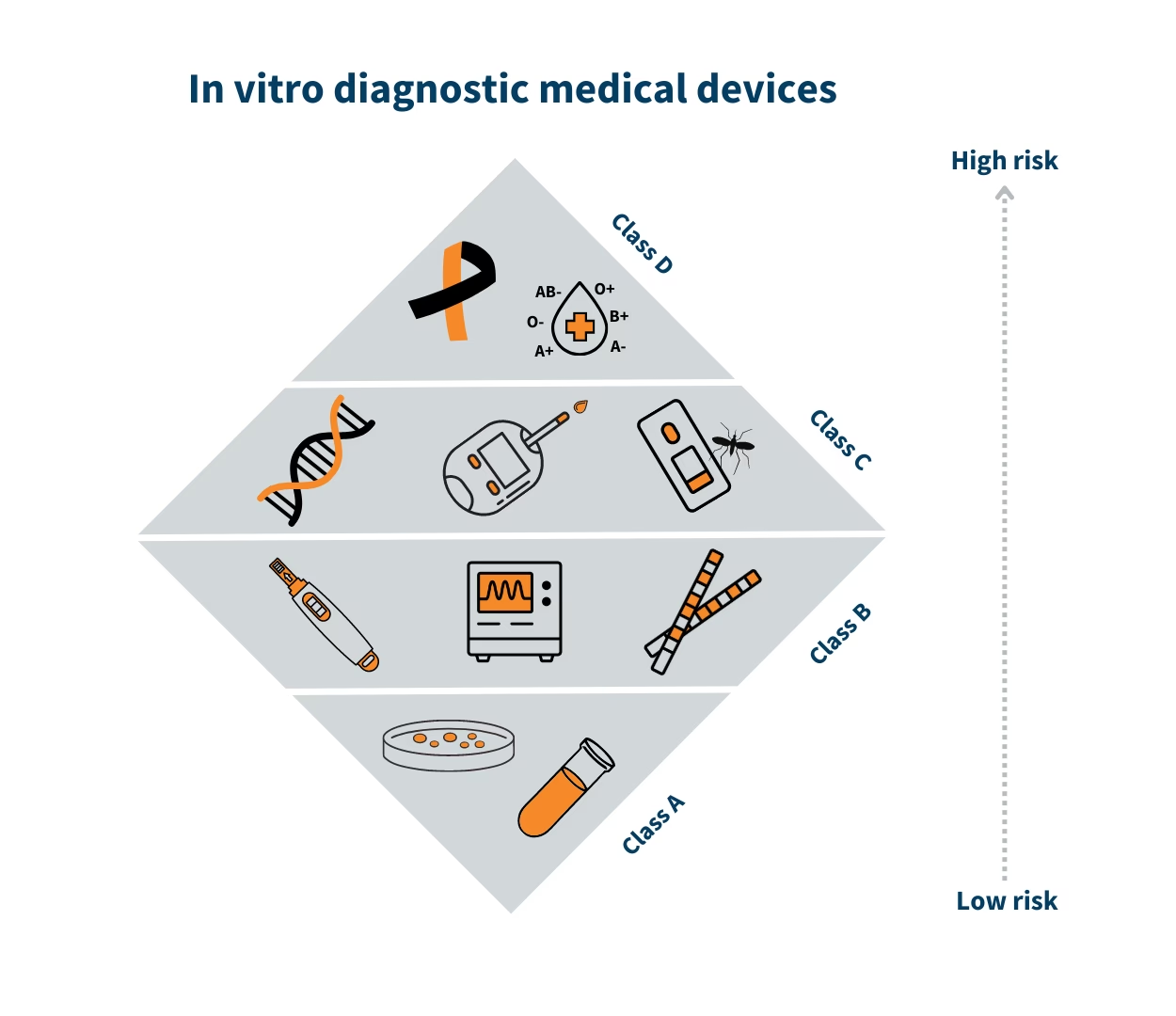
Klassificering af Tilbagekaldelser
Lægemiddelstyrelsen vil i samarbejde med virksomheden klassificere alvorligheden af fejlen. Dette afgør, hvor hurtigt og hvor bredt tilbagekaldelsen skal effektueres. Klassificeringen følger typisk internationale standarder.
| Klasse | Risikoniveau | Beskrivelse | Handling |
|---|---|---|---|
| Klasse I | Høj risiko | En kvalitetsfejl, der kan forårsage alvorlige helbredsproblemer eller være livstruende. | Tilbagekaldelse ned til patientniveau. Kræver ofte offentlig kommunikation. |
| Klasse II | Mellem risiko | En kvalitetsfejl, der kan forårsage midlertidige eller medicinsk reversible helbredsproblemer. Sandsynligheden for alvorlig skade er lav. | Tilbagekaldelse ned til apoteks- og hospitalsniveau. |
| Klasse III | Lav risiko | En kvalitetsfejl, der sandsynligvis ikke vil forårsage helbredsmæssige konsekvenser, f.eks. en mindre trykfejl på etiketten, der ikke påvirker sikkerheden. | Tilbagekaldelse fra grossistniveau eller stop for yderligere distribution. |
Hvad Sker der Efter Rapporteringen?
Når Lægemiddelstyrelsen er informeret, starter en tæt dialog med virksomheden. Styrelsen vurderer virksomhedens undersøgelser og risikovurdering og tager den endelige beslutning om omfanget af tilbagekaldelsen. De sikrer, at kommunikationen til de relevante parter (grossister, apoteker, hospitaler) er klar og effektiv. Formålet er at fjerne det potentielt skadelige produkt fra markedet så hurtigt og sikkert som muligt for at beskytte folkesundheden.
Ofte Stillede Spørgsmål (FAQ)
Hvad er forskellen på at indberette en bivirkning og en kvalitetsfejl?
En bivirkning er en reaktion på et lægemiddel, der er produceret korrekt, mens en kvalitetsfejl er en fejl ved selve produktet. Bivirkninger indberettes via et separat system, typisk af patienter eller sundhedspersonale. Kvalitetsfejl, der kan føre til tilbagekaldelse, indberettes som beskrevet i denne artikel, primært af medicinalvirksomheder.
Kan jeg som privatperson indberette en mistanke om en kvalitetsfejl?
Ja. Hvis du som patient har mistanke om, at der er noget galt med din medicin (f.eks. misfarvede piller, mærkelig lugt, brudt forsegling), bør du kontakte dit apotek eller din læge. De vil vurdere situationen og om nødvendigt tage kontakt til producenten og/eller Lægemiddelstyrelsen.
Hvad er Lægemiddelstyrelsens hovedtelefonnummer igen?
Det primære kontaktnummer for sager vedrørende potentiel tilbagekaldelse af lægemidler er +45 4488 9595.
Skal jeg vente med at ringe, til jeg har alle detaljer?
Nej. Ved en potentiel alvorlig fejl er det bedre at ringe med det samme med den information, du har, og derefter følge op skriftligt, når flere detaljer er kendt. Tidlig varsling er afgørende for patientsikkerheden.
Hvis du vil læse andre artikler, der ligner Kontakt Lægemiddelstyrelsen ved tilbagekaldelse, kan du besøge kategorien Sundhed.