16/09/2018
Når du tager din medicin, forventer du, at den virker præcis som den skal, hver eneste gang. Men hvad sikrer egentlig, at pillen i dag har nøjagtig samme kvalitet og effekt som den, du tog i sidste uge? Svaret ligger i en moderne og videnskabelig tilgang til lægemiddeludvikling og -produktion kendt som Quality by Design (QbD). Konceptet blev oprindeligt udviklet af kvalitetspioneren Dr. Joseph M. Juran, som mente, at kvalitet skal designes ind i et produkt fra starten, frem for at blive testet ind til sidst. I den farmaceutiske verden betyder det, at man ikke længere blot tester slutproduktet for at se, om det lever op til kravene. I stedet bygger man kvaliteten ind i hver eneste fase af processen, fra den indledende idé til den færdige tablet.
Denne proaktive tilgang er en revolution i forhold til den traditionelle metode, hvor man ofte opdagede problemer sent i processen, hvilket førte til kasserede partier, forsinkelser og i værste fald tilbagekaldelser af medicin fra markedet. Med QbD er målet at forstå produktet og processen så dybtgående, at man kan forudsige og kontrollere kvaliteten på forhånd. Det er en systematisk metode, der sikrer, at patienter modtager lægemidler, der er både sikre og pålideligt leverer den lovede terapeutiske fordel.
Hvad er Quality by Design (QbD) helt præcist?
Quality by Design er en systematisk, videnskabs- og risikobaseret tilgang til farmaceutisk udvikling. Den begynder med foruddefinerede mål og lægger vægt på en dyb forståelse af produktet og fremstillingsprocessen. Kernen i QbD er at identificere de faktorer, der er kritiske for lægemidlets endelige kvalitet, og derefter designe en proces, der konsekvent kan levere denne kvalitet.
Forestil dig, at du skal bygge et hus. Den traditionelle metode ville være at bygge huset og bagefter tjekke, om væggene er lige, og om taget er tæt. Med en QbD-tilgang ville du på forhånd analysere materialerne, forstå hvordan de reagerer på vejrforhold, og designe byggeprocessen, så du er sikker på, at væggene bliver lige, og taget bliver tæt – hver gang. I lægemiddelproduktion handler det om at forstå, hvordan lægemiddelstoffet (den aktive ingrediens) og hjælpestofferne (fyldstoffer, bindemidler osv.) interagerer, og hvordan hver enkelt produktionsetape (f.eks. blanding, granulering, tørring og presning) påvirker det endelige produkts egenskaber som opløsningstid, holdbarhed og effekt.
De primære mål med farmaceutisk QbD
Implementeringen af QbD i medicinalindustrien har flere klare mål, som alle i sidste ende gavner patienten:
- At sikre klinisk ydeevne: Det vigtigste mål er at designe et produkt, der konsekvent leverer den ønskede terapeutiske effekt. Ved at koble produktets kvalitetsattributter direkte til dets kliniske performance, kan man udvikle robuste formuleringer, der virker som forventet.
- At reducere produktvariation: Variation i produktionen kan føre til defekte produkter, afvisninger og tilbagekaldelser. QbD sigter mod at designe robuste processer, der kan modstå små variationer i råmaterialer og driftsbetingelser, hvilket resulterer i et mere ensartet og pålideligt produkt.
- At øge effektiviteten: Ved at forstå processen dybtgående kan producenter hurtigere identificere og løse produktionsproblemer. Dette flytter ressourcer fra reaktiv fejlfinding til proaktiv kvalitetssikring, hvilket sparer tid og penge og i sidste ende kan føre til hurtigere adgang til ny medicin.
Kerneelementerne i Quality by Design
QbD-processen er bygget op omkring en række definerede elementer, der tilsammen skaber et komplet billede af produktet og processen. Disse elementer sikrer en struktureret og videnskabelig tilgang.
- Kvalitetsmålprofil for produktet (QTPP - Quality Target Product Profile): Dette er startpunktet. QTPP er en detaljeret beskrivelse af, hvordan det ideelle lægemiddel skal se ud og fungere fra patientens perspektiv. Det inkluderer information om doseringsform (tablet, kapsel), dosisstyrke, administrationsvej, og hvordan lægemidlet skal frigives i kroppen for at opnå den ønskede effekt.
- Identifikation af Kritiske Kvalitetsattributter (CQAs - Critical Quality Attributes): Baseret på QTPP identificeres de fysiske, kemiske og biologiske egenskaber ved det færdige produkt, som er afgørende for dets kvalitet. For en tablet kan CQAs være hårdhed, vægt, opløsningstid og indhold af aktive stof. En attribut er "kritisk", hvis en afvigelse kan skade patienten eller mindske effekten.
- Design og forståelse af produkt og proces: Her dykker man ned i videnskaben. Man undersøger råmaterialerne – både det aktive lægemiddelstof og hjælpestofferne – for at identificere deres kritiske materialeattributter (CMAs). Samtidig analyseres fremstillingsprocessen for at finde de kritiske procesparametre (CPPs), f.eks. blandingshastighed eller pressetryk. Målet er at forstå præcis, hvordan CMAs og CPPs påvirker de endelige CQAs.
- Udvikling af en kontrolstrategi: Med den opnåede viden udvikles en plan for at overvåge og styre produktionen. Denne strategi sikrer, at processen forbliver inden for de definerede rammer, så det færdige produkt altid opfylder kvalitetskravene. Dette kan inkludere avanceret overvågning i realtid (Process Analytical Technology - PAT) i stedet for kun at teste det færdige produkt.
- Kontinuerlig forbedring: QbD er ikke en engangsøvelse. Processen og produktet overvåges løbende gennem hele produktets levetid for at finde muligheder for forbedringer og for at sikre, at kvaliteten opretholdes.
Sammenligning: Traditionel tilgang vs. QbD
For at illustrere forskellen kan vi se på, hvordan man ville gribe en produktionsudfordring an med de to metoder.
| Aspekt | Traditionel Kvalitetstilgang (Quality by Testing) | Moderne Tilgang (Quality by Design) |
|---|---|---|
| Fokus | Empirisk, fokuseret på reproducerbarhed. Man tester slutproduktet for at bekræfte kvalitet. | Systematisk, videnskabelig og proaktiv. Kvalitet designes ind i processen. |
| Procesforståelse | Ofte begrænset. Man ved, at processen virker, men ikke altid hvorfor. | Dybdegående. Man forstår sammenhængen mellem råmaterialer, procesparametre og produktkvalitet. |
| Råmaterialekontrol | Strenge specifikationer for råmaterialer for at minimere variation. | Forstår, hvordan variation i råmaterialer påvirker processen, og kan justere processen for at kompensere. |
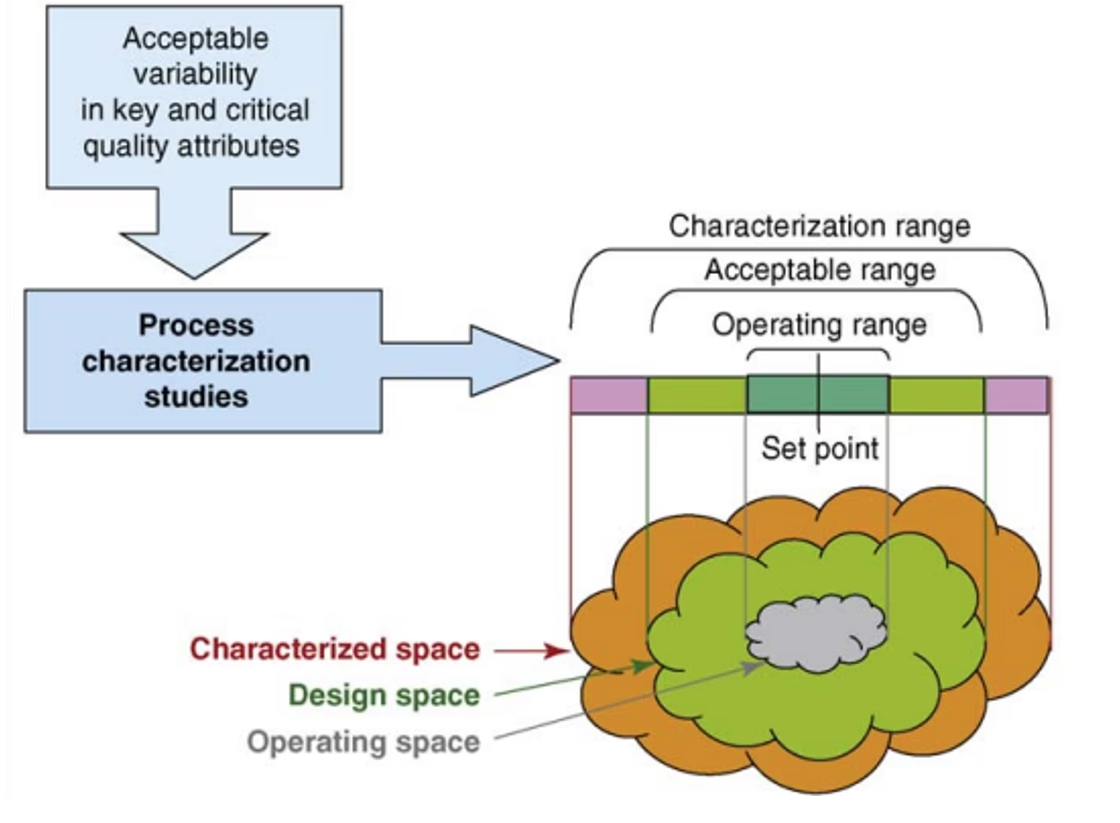
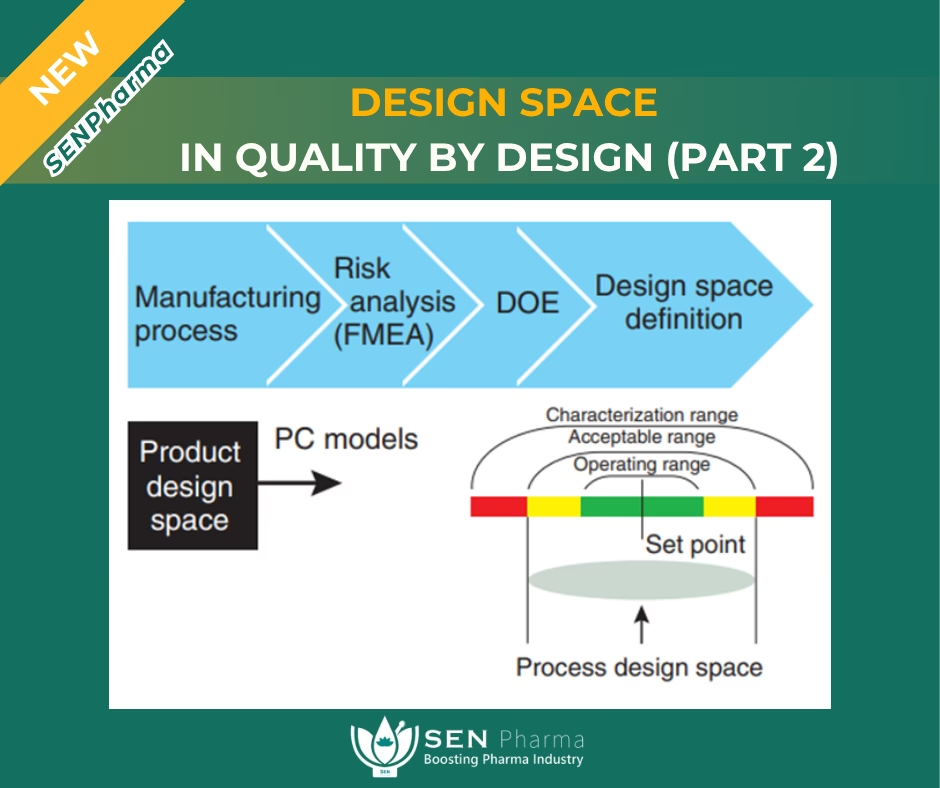
| Kontrolstrategi | Primært baseret på in-process tests og omfattende testning af det færdige produkt. | Risikobaseret kontrol, der kan inkludere realtidsovervågning (PAT) og fleksible procesparametre inden for et valideret "Design Space". |
| Håndtering af ændringer | Enhver ændring kræver ofte en ny validering og regulatorisk godkendelse. | Ændringer inden for det godkendte Design Space kan implementeres uden yderligere godkendelse, hvilket fremmer kontinuerlig forbedring. |
Hvad betyder QbD for dig som patient?
Selvom QbD er et teknisk koncept for medicinalindustrien, har det direkte og positive konsekvenser for patienterne. Når producenter anvender QbD-principperne, resulterer det i:
- Øget sikkerhed og pålidelighed: En dybere forståelse af produktet og processen minimerer risikoen for produktionsfejl. Dette fører til færre defekte produkter og en markant lavere risiko for tilbagekaldelser af medicin.
- Mere konsistent effekt: Ved at kontrollere de kritiske kvalitetsattributter sikrer man, at hver eneste dosis medicin har den samme høje kvalitet og virker præcis som forventet. Dette er især vigtigt for lægemidler med et snævert terapeutisk indeks, hvor små variationer i dosis kan have store konsekvenser.
- Potentielt færre medicinmangler: Robuste og effektive produktionsprocesser er mindre sårbare over for forstyrrelser. Dette kan bidrage til en mere stabil forsyning af vigtige lægemidler og reducere risikoen for mangelsituationer på apotekerne.
- Innovation og hurtigere adgang til ny medicin: En mere effektiv udviklingsproces kan forkorte tiden, det tager at bringe nye, innovative lægemidler på markedet, så patienter hurtigere kan få adgang til nye behandlinger.
Ofte Stillede Spørgsmål (FAQ)
Er Quality by Design et helt nyt koncept?
Nej, ideen om at designe kvalitet ind i et produkt har eksisteret i mange andre industrier i årtier, f.eks. i bil- og elektronikindustrien. Anvendelsen og formaliseringen inden for den farmaceutiske industri er dog mere moderne og er blevet stærkt opmuntret af lægemiddelmyndigheder som det amerikanske FDA og det europæiske EMA siden begyndelsen af 2000-tallet.
Gør QbD medicin dyrere at fremstille?
I starten kan implementeringen af QbD kræve større investeringer i forskning, udstyr og ekspertise. Men på lang sigt er målet det modsatte. Ved at reducere antallet af fejlslagne produktionsserier, minimere spild og skabe en mere effektiv proces, kan de samlede produktionsomkostninger falde. Denne effektivitet kan potentielt bidrage til at holde medicinpriserne stabile.
Hvordan ved jeg, om min medicin er produceret ved hjælp af QbD?
Som patient kan du ikke direkte se det på medicinpakken. QbD er dog i dag en integreret del af de regulatoriske krav for udvikling af nye lægemidler. Når et nyt lægemiddel bliver godkendt af myndighederne, er det baseret på en omfattende dokumentation, hvor QbD-principperne spiller en central rolle i at demonstrere produktets kvalitet og sikkerhed. Du kan derfor have tillid til, at moderne medicin er underlagt disse strenge kvalitetsstandarder.
Gælder QbD for alle typer medicin?
Ja, principperne i QbD er universelle og kan anvendes på alle typer lægemidler og doseringsformer – lige fra simple tabletter og kapsler til mere komplekse produkter som cremer, inhalatorer, injektionsvæsker og bioteknologiske lægemidler.
Afslutningsvis repræsenterer Quality by Design et paradigmeskifte i den farmaceutiske verden. Det er vejen fra en reaktiv til en proaktiv tilgang, hvor dyb videnskabelig forståelse danner grundlaget for at skabe sikre, effektive og pålidelige lægemidler. For dig som patient er det en usynlig, men afgørende garanti for, at den medicin, du stoler på, er af den højest mulige kvalitet – hver eneste gang.
Hvis du vil læse andre artikler, der ligner Kvalitet i Design: Sikring af din Medicin, kan du besøge kategorien Sundhed.