19/08/2021
Inden for moderne medicin og sundhedsvidenskab er der få koncepter, der har haft en så transformerende effekt som biomarkører. De er blevet uundværlige værktøjer, der spænder over hele sundhedsspektret – fra tidlig sygdomsdetektion og diagnose til overvågning af behandling og udvikling af nye lægemidler. Biomarkører fungerer som kroppens egne budbringere, der giver os kritiske indblik i normale biologiske processer, patogene processer og kroppens reaktion på behandlinger. Forståelsen af disse målbare indikatorer er kernen i den bevægelse, vi kalder personlig medicin, hvor behandlinger skræddersys til den enkelte patients unikke biologiske profil.
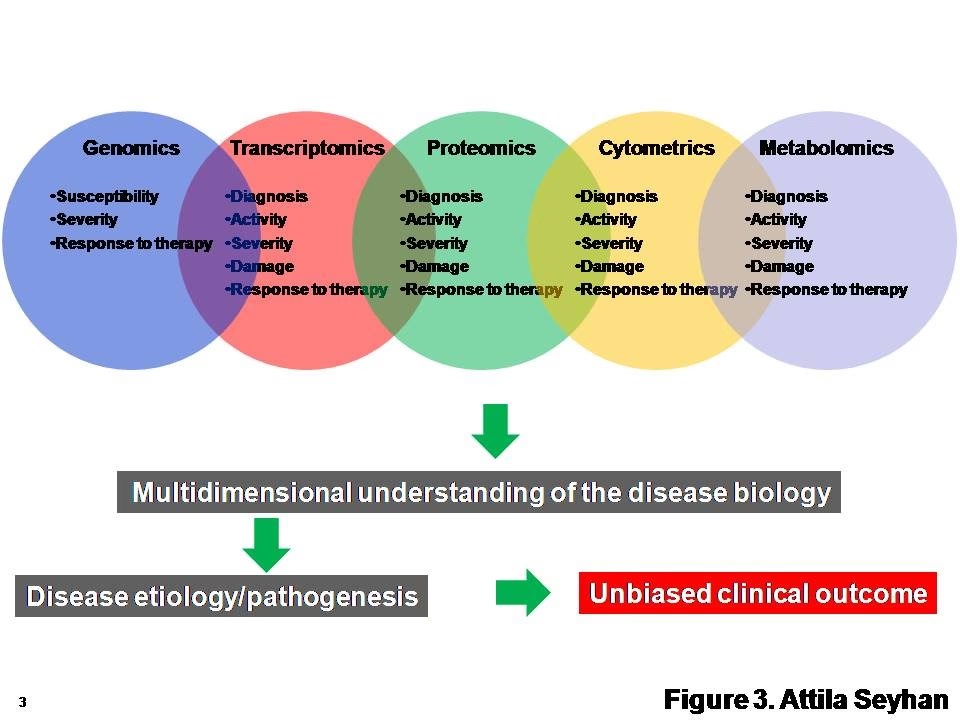
I de sidste tre årtier har vi været vidne til en dramatisk udvikling. Fra simple målinger som blodsukker og kolesterol er vi gået til avancerede molekylære og digitale markører, der kan forudsige sygdomsforløb med hidtil uset præcision. Denne udvikling er drevet af gennembrud inden for genomik, proteomik og kunstig intelligens, som tilsammen har åbnet døren for en dybere forståelse af menneskelig biologi. Denne artikel vil dykke ned i, hvad biomarkører er, de forskellige typer, der findes, og hvordan de former fremtiden for diagnostik og behandling.
Hvad er en biomarkør helt præcist?
Den grundlæggende definition af en biomarkør er bedragerisk simpel. Ifølge en fælles ressource fra den amerikanske fødevare- og lægemiddelmyndighed (FDA) og National Institutes of Health (NIH) er en biomarkør: "En defineret karakteristik, der måles som en indikator for normale biologiske processer, patogene processer eller reaktioner på en eksponering eller intervention."
Denne brede definition dækker et stort område. En biomarkør kan stamme fra molekylære, histologiske, radiografiske eller fysiologiske karakteristika. Det kan være alt fra tilstedeværelsen af et bestemt protein i blodet, en genetisk mutation, blodtryksmålinger til data fra et smartwatch. Det er afgørende at skelne mellem biomarkører og det, der kaldes kliniske resultatvurderinger (Clinical Outcome Assessments - COAs). COAs måler direkte, hvordan en patient har det, fungerer eller overlever – for eksempel smerteniveau, mobilitet eller levetid. Biomarkører er derimod indirekte målinger, der kan bruges til at forudsige disse kliniske resultater. Kun når en biomarkør er grundigt valideret, kan den fungere som det primære grundlag for godkendelse af et lægemiddel.
De Forskellige Typer af Biomarkører
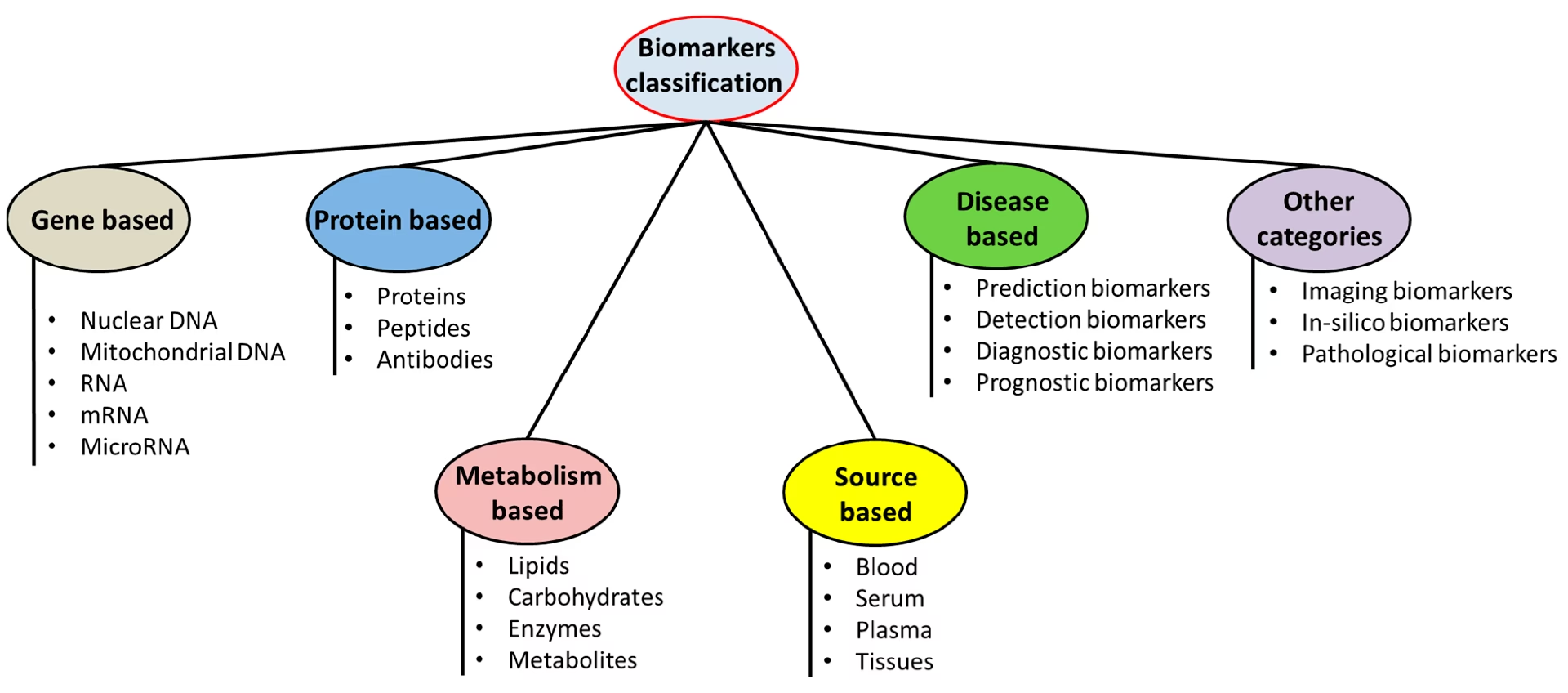
Biomarkører kan klassificeres i flere undertyper baseret på deres specifikke anvendelse. Det er vigtigt at bemærke, at en enkelt biomarkør kan opfylde kriterierne for flere kategorier, men hver anvendelse kræver separat validering og dokumentation. Nedenfor gennemgås de mest almindelige typer.
Diagnostiske Biomarkører
En diagnostisk biomarkør bruges til at opdage eller bekræfte tilstedeværelsen af en sygdom eller tilstand. Den kan også identificere en specifik undertype af en sygdom. Et klassisk eksempel er måling af troponin i blodet for at diagnosticere et akut myokardieinfarkt (hjerteanfald). I takt med at vi bevæger os ind i æraen for præcisionsmedicin, udvikler denne type biomarkør sig markant, især inden for onkologi, hvor kræft i stigende grad klassificeres baseret på molekylære profiler frem for kun organets placering.
Monitoreringsbiomarkører
Disse biomarkører måles serielt (gentagne gange over tid) for at vurdere status for en sygdom, en medicinsk tilstand eller for at opdage effekten af et lægemiddel. Eksempler inkluderer måling af blodtryk for at overvåge effekten af antihypertensiv behandling, LDL-kolesterolniveauer under behandling med statiner, eller HbA1c for at overvåge blodsukkerkontrol hos diabetespatienter. De er afgørende i kliniske forsøg for at sikre deltagernes sikkerhed, for eksempel ved at måle leverenzymer for at opdage potentiel lægemiddeltoksicitet.

Farmakodynamiske/Responsbiomarkører
En farmakodynamisk biomarkør viser en ændring som reaktion på eksponering for et lægemiddel. Denne type er ekstremt nyttig i både klinisk praksis og tidlig lægemiddeludvikling. Hvis en patient behandles for forhøjet blodtryk, og blodtrykket ikke falder, er det en klar indikation af, at behandlingen ikke virker. I tidlige faser af lægemiddeludvikling kan disse biomarkører give bevis for, at et lægemiddelkandidat rammer sit biologiske mål, hvilket er afgørende for beslutningen om at fortsætte udviklingen.
Prædiktive Biomarkører
En prædiktiv biomarkør forudsiger, om en person eller en gruppe er mere tilbøjelig til at opleve en gunstig eller ugunstig effekt af en bestemt behandling. Et af de mest kendte eksempler er HER2-receptoren i brystkræft. Patienter med HER2-positiv brystkræft har en markant bedre respons på behandlingen med Herceptin (trastuzumab). Et andet eksempel er PD-L1-ekspression, som kan forudsige respons på immunterapi. Disse biomarkører er fundamentale for at kunne udvælge de patienter, der vil have størst gavn af en given behandling.
Prognostiske Biomarkører
En prognostisk biomarkør bruges til at identificere sandsynligheden for en klinisk hændelse, sygdomsrecidiv eller progression hos patienter, der allerede har en sygdom. I modsætning til prædiktive biomarkører er de ikke relateret til effekten af en specifik behandling, men snarere til sygdommens naturlige forløb. I kliniske forsøg bruges de ofte til at udvælge højrisikopopulationer for at øge antallet af hændelser og dermed den statistiske styrke i forsøget.
Sikkerhedsbiomarkører
En sikkerhedsbiomarkør måles før eller efter eksponering for en medicinsk intervention for at indikere sandsynligheden, tilstedeværelsen eller omfanget af toksicitet som en bivirkning. For eksempel overvåges QT-intervallet på et elektrokardiogram (EKG), når visse antiarytmiske lægemidler gives, da en forlængelse kan forudsige risikoen for en livstruende arytmi.
Modtageligheds-/Risikobiomarkører
Disse biomarkører indikerer potentialet for at udvikle en sygdom hos en person, der endnu ikke har klinisk synlig sygdom. De er fundamentale for epidemiologiske studier. Et velkendt eksempel er tilstedeværelsen af BRCA1- eller BRCA2-genmutationer, som markant øger risikoen for at udvikle bryst- og æggestokkræft.
Oversigtstabel over Biomarkørtyper
| Biomarkørtype | Formål | Eksempel |
|---|---|---|
| Diagnostisk | Opdage eller bekræfte en sygdom. | Troponin for hjerteanfald. |
| Monitorering | Følge en sygdoms status eller behandlingseffekt. | HbA1c for diabetes. |
| Farmakodynamisk | Måle en biologisk respons på et lægemiddel. | Blodtryksfald efter antihypertensiv medicin. |
| Prædiktiv | Forudsige respons på en specifik behandling. | HER2-status for behandling med Herceptin. |
| Prognostisk | Forudsige sygdomsforløb uafhængigt af behandling. | Visse genekspressionsprofiler i kræft. |
| Sikkerhed | Indikere potentiel toksicitet eller bivirkninger. | Leverenzymer under lægemiddelbehandling. |
| Modtagelighed/Risiko | Identificere risiko for at udvikle en sygdom. | BRCA1/2-genmutationer for kræft. |
Fremtiden for Biomarkørvidenskab
Feltet for biomarkører er i konstant og hurtig udvikling. Nye teknologier skubber grænserne for, hvad vi kan måle og forstå. Nogle af de mest spændende fremtidsudsigter inkluderer:
- Flydende Biopsi: Dette repræsenterer et af de mest lovende fremskridt, især inden for onkologi. En flydende biopsi er en simpel blodprøve, hvor man kan analysere cirkulerende tumor-DNA (ctDNA), exosomer og andre molekylære markører, der frigives fra en tumor. Dette giver mulighed for ikke-invasiv, tidlig kræftopdagelse, overvågning af behandlingsrespons og sporing af tumorudvikling i realtid.
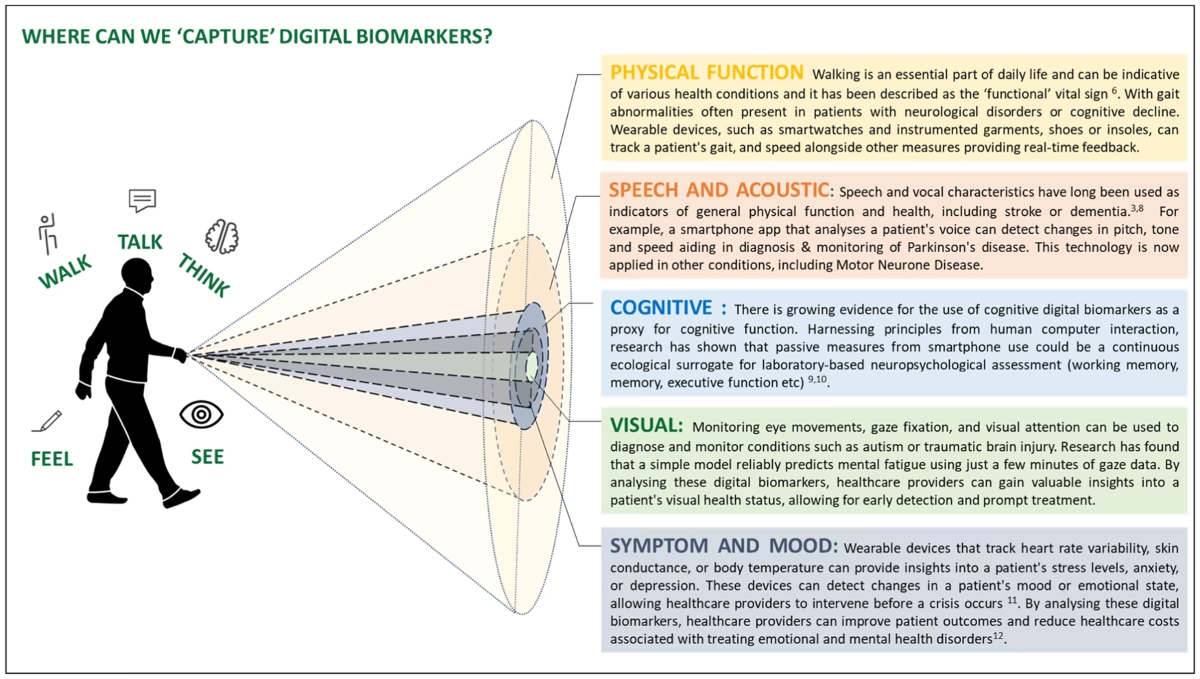
- Digitale Biomarkører: Med udbredelsen af wearables som smartwatches og fitness-trackere samt smartphones er digitale biomarkører kommet i fokus. Disse enheder kan kontinuerligt indsamle fysiologiske og adfærdsmæssige data, såsom hjerterytmevariabilitet, søvnmønstre, bevægelsesanalyse og endda talemønstre. Disse data kan bruges til at overvåge kroniske sygdomme som hjerte-kar-sygdomme og diabetes eller til tidlig opsporing af neurodegenerative sygdomme som Parkinsons.
- Kunstig Intelligens (AI): AI og machine learning-algoritmer revolutionerer opdagelsen af biomarkører. Ved at analysere enorme datasæt fra genomik, proteomik og billeddiagnostik kan AI identificere komplekse mønstre og nye biomarkører, som ville være umulige at opdage med konventionelle metoder.
- Mikrobiombaserede Biomarkører: Forskning i det menneskelige mikrobiom – samlingen af mikroorganismer i vores krop – afslører tætte forbindelser mellem tarmfloraens sammensætning og en lang række sygdomme, herunder inflammatoriske tarmsygdomme, fedme, kræft og endda psykiske lidelser. Mikrobiomets profil kan derfor fungere som en ny type biomarkør.
Ofte Stillede Spørgsmål
Hvad er forskellen på en biomarkør og et klinisk resultat?
En biomarkør er en indirekte måling af en biologisk tilstand (f.eks. kolesteroltal), mens et klinisk resultat er en direkte måling af, hvordan patienten har det, fungerer eller overlever (f.eks. et hjerteanfald eller overlevelsesrate). En velvalideret biomarkør kan dog bruges til at forudsige et klinisk resultat.
Kan én biomarkør bruges til flere formål?
Ja, absolut. For eksempel er LDL-kolesterol både en modtageligheds-/risikobiomarkør (høje niveauer øger risikoen for hjerte-kar-sygdom) og en monitoreringsbiomarkør (dens niveau følges under behandling med kolesterolsænkende medicin).
Hvorfor er validering af biomarkører så vigtig?
Validering sikrer, at en biomarkør er pålidelig, præcis og relevant for sin specifikke anvendelse (context of use). Uden grundig validering kan en biomarkør føre til forkerte diagnoser, ineffektive behandlingsvalg og spildte ressourcer i lægemiddeludvikling.
Hvad er en "companion diagnostic"?
En companion diagnostic er en diagnostisk test (ofte baseret på en biomarkør), der er tæt knyttet til et specifikt lægemiddel. Testen er nødvendig for at identificere de patienter, der sandsynligvis vil have gavn af lægemidlet. Et eksempel er testen for HER2-status, som er afgørende for at beslutte, om en brystkræftpatient skal behandles med Herceptin.
Hvis du vil læse andre artikler, der ligner Biomarkører: Kroppens Skjulte Signaler Forklaret, kan du besøge kategorien Sundhed.