30/11/2020
Når du tager din medicin, forventer du, at den virker på samme måde hver eneste gang. Du stoler på, at hver pille, kapsel eller injektion indeholder den korrekte mængde aktivt stof og er fri for urenheder. Denne konsistens og sikkerhed er ikke en tilfældighed. Den er resultatet af omhyggelige produktionsprocesser. I de senere år har en videnskabelig og risikobaseret tilgang kaldet Quality by Design (QbD) revolutioneret, hvordan medicinalvirksomheder sikrer kvalitet i deres produkter. Det er en filosofi, der flytter fokus fra blot at teste det færdige produkt til at forstå og kontrollere hele fremstillingsprocessen fra start til slut.
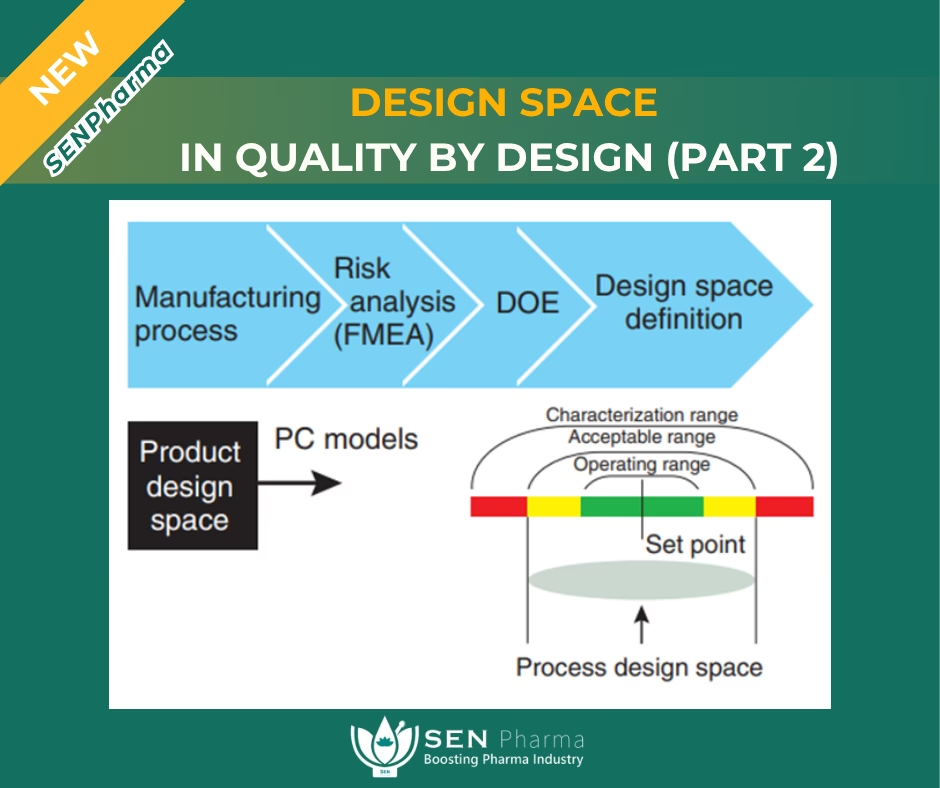
QbD er i sin essens en systematisk tilgang til udvikling, der begynder med foruddefinerede mål og lægger vægt på produkt- og procesforståelse samt proceskontrol, baseret på solid videnskab og kvalitetsrisikostyring. I stedet for at vente til slutningen af produktionslinjen og håbe på, at et parti medicin består en kvalitetstest, designer man med QbD kvaliteten ind i selve processen. Dette sikrer en langt højere grad af forudsigelighed og robusthed, hvilket i sidste ende kommer patienterne til gode i form af sikrere og mere effektive lægemidler.
Hvad betyder Quality by Design (QbD) i praksis?
For at forstå QbD kan man forestille sig, at man skal bage den perfekte kage. Den traditionelle metode ville være at følge en opskrift, bage kagen og derefter smage på den for at se, om den er god. Hvis den mislykkes, kasserer man den og prøver igen. Med en QbD-tilgang ville man i stedet starte med at definere, hvad den 'perfekte kage' er (smag, tekstur, højde). Derefter ville man systematisk undersøge, hvordan hver ingrediens (mel, sukker, æg) og hver procesvariabel (ovntemperatur, bagetid) påvirker det endelige resultat. Man ville finde ud af, at en ovntemperatur mellem 175 og 185 grader og en bagetid på 30-35 minutter altid giver en perfekt kage. Dette 'vindue' af acceptable betingelser kaldes et 'Design Space'. Så længe man arbejder inden for dette vindue, ved man med stor sikkerhed, at kagen bliver vellykket, uden at man behøver at smage på hver eneste.
I lægemiddelproduktion fungerer princippet på samme måde. QbD handler om at opbygge en dyb procesforståelse. Det indebærer at identificere de kritiske kvalitetsattributter (Critical Quality Attributes - CQAs) for et lægemiddel – de fysiske, kemiske eller biologiske egenskaber, der skal være inden for et bestemt interval for at sikre den ønskede produktkvalitet. Herefter identificeres de kritiske procesparametre (Critical Process Parameters - CPPs), som er de procesvariable, der kan påvirke disse CQAs. Ved at forstå forholdet mellem CPPs og CQAs kan man definere et såkaldt Design Space.
Kernekomponenterne i QbD-tilgangen
QbD-processen er struktureret og bygger på flere nøgleelementer, der arbejder sammen for at sikre det endelige produkts kvalitet:
- Quality Target Product Profile (QTPP): Dette er det første skridt. Her defineres målet for lægemidlet. Hvad skal det kunne? Hvilken sygdom skal det behandle? Hvordan skal det administreres (f.eks. pille, injektion)? Hvad er de vigtigste sikkerheds- og effektivitetskrav? QTPP fungerer som en guide for hele udviklingsprocessen.
- Critical Quality Attributes (CQAs): Baseret på QTPP identificeres de specifikke egenskaber ved produktet, som er afgørende for dets kvalitet. For en pille kan det være ting som opløsningstid, hårdhed, og renhed af det aktive stof. Disse skal måles og kontrolleres nøje.
- Critical Process Parameters (CPPs): Dette er de variable i produktionsprocessen, som har en direkte indflydelse på CQAs. Det kan være temperatur, tryk, blandingshastighed eller tørretid. En lille ændring i en CPP kan potentielt have stor betydning for det færdige produkts kvalitet.
- Design Space: Som nævnt er dette det 'operationelle vindue' for CPPs. Det er en multidimensionel kombination af procesparametre, der er blevet demonstreret til at levere et produkt af den ønskede kvalitet. Det defineres videnskabeligt gennem eksperimenter og dataanalyse. Så længe produktionen foregår inden for dette Design Space, er der en meget høj grad af sikkerhed for, at produktet vil opfylde sine specifikationer. Det er her, statistiske begreber som '95% konfidens for, at 99% af populationen opfylder specifikationerne' kommer i spil. Det giver en robust ramme for produktionen.
- Kontrolstrategi: Til sidst udvikles en samlet kontrolstrategi. Denne strategi omfatter overvågning af CPPs i realtid (ofte ved hjælp af avanceret teknologi kaldet Process Analytical Technology - PAT), kontrol af råmaterialer og procedurer for at sikre, at processen konstant holdes inden for det definerede Design Space.
Sammenligning: QbD vs. Traditionel Kvalitetskontrol
For at illustrere fordelene ved QbD er det nyttigt at sammenligne det med den mere traditionelle tilgang, som ofte kaldes Quality by Testing (QbT).
| Aspekt | Traditionel Tilgang (Quality by Testing) | Moderne Tilgang (Quality by Design) |
|---|---|---|
| Fokus | Testning af det færdige produkt. | Forståelse og kontrol af hele processen. |
| Tilgang | Reaktiv - man reagerer på fejl, når de opstår. | Proaktiv - man designer processen for at undgå fejl. |
| Procesviden | Ofte begrænset. Man ved, at opskriften virker, men ikke altid hvorfor. | Dybdegående og videnskabeligt baseret. |
| Fleksibilitet | Meget lav. Enhver ændring kræver ofte ny godkendelse. | Højere. Fleksibilitet til at justere inden for det godkendte Design Space. |
| Kvalitetssikring | Kvalitet sikres primært gennem inspektion og test. | Kvalitet er bygget ind i produktet og processen fra starten. |
| Resultat | Variabel produktkvalitet er en risiko. | Høj grad af konsistens og forudsigelighed. |
Fordele for Patienten
Selvom QbD kan virke som et teknisk koncept for industrien, har det direkte og betydelige fordele for dig som patient. Den øgede fokus på patientsikkerhed og produktkonsistens fører til flere positive resultater:
- Mere Pålidelig Medicin: Med QbD er der mindre variation fra et produktionsparti til et andet. Det betyder, at den medicin, du tager i dag, har præcis samme effekt og kvalitet som den, du tager om et halvt år.
- Færre Tilbagekaldelser og Mangelsituationer: En robust og velkontrolleret proces fører til færre produktionsfejl. Dette reducerer risikoen for, at et parti medicin må trækkes tilbage fra markedet, og mindsker sandsynligheden for mangelsituationer på apotekerne.
- Hurtigere Adgang til Forbedringer: Fordi QbD giver en dybere procesforståelse, kan producenter lettere og mere sikkert implementere forbedringer i deres produktion. Dette kan føre til mere effektive og billigere lægemidler over tid.
- Øget Sikkerhed: Ved proaktivt at identificere og kontrollere de faktorer, der kan påvirke produktkvaliteten, minimeres risikoen for urenheder eller forkert dosering, hvilket øger den generelle sikkerhed ved lægemidlet.
Ofte Stillede Spørgsmål (FAQ)
Er medicin fremstillet med QbD mere sikker?
Ja, generelt set er medicin fremstillet efter QbD-principperne designet til at have en højere og mere konsistent grad af sikkerhed. Tilgangen minimerer risikoen for produktionsfejl ved at bygge kvalitetskontrol ind i hvert eneste trin af processen, i stedet for kun at stole på en afsluttende test.
Hvorfor bruger ikke alle medicinalvirksomheder QbD?
Implementering af QbD kræver en betydelig investering i tid, teknologi og ekspertise i starten af udviklingsprocessen. Det er en mere kompleks og datadrevet tilgang end den traditionelle metode. Selvom de langsigtede fordele er store, kan den indledende investering være en barriere for nogle virksomheder. Dog opfordrer myndigheder som det Europæiske Lægemiddelagentur (EMA) og den amerikanske FDA kraftigt til brugen af QbD, og det bliver mere og mere standard i industrien.
Hvordan kan jeg vide, om min medicin er fremstillet ved hjælp af QbD?
Det er ikke noget, der normalt fremgår af indlægssedlen eller emballagen. Det er en del af den tekniske dokumentation, som medicinalvirksomheden indsender til sundhedsmyndighederne for at få deres produkt godkendt. Man kan dog være forvisset om, at alle lægemidler på markedet har gennemgået en streng godkendelsesproces for at sikre deres kvalitet, sikkerhed og effekt, og at moderne lægemidler i stigende grad drager fordel af QbD-principperne.
Hvis du vil læse andre artikler, der ligner Quality by Design: Kvalitet i din Medicin, kan du besøge kategorien Sundhed.
