30/12/2021
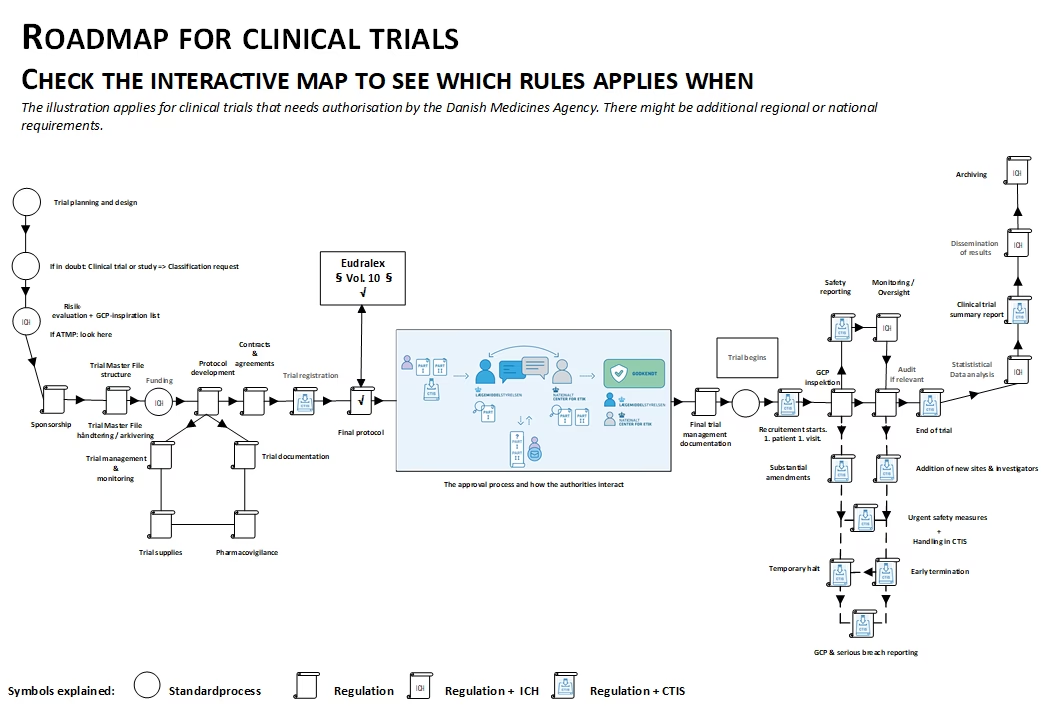
Gennemførelse af kliniske forsøg er en fundamental del af medicinsk udvikling, der sikrer, at nye lægemidler og medicinsk udstyr er både sikre og effektive. I de seneste år er landskabet for ansøgning om kliniske forsøg i Europa blevet markant forandret. Med introduktionen af EU's forordning om kliniske forsøg (CTR) er processen blevet centraliseret og harmoniseret på tværs af medlemslandene. Danmark har fuldt ud implementeret disse nye regler, hvilket betyder, at alle ansøgninger nu skal navigeres gennem et nyt fælles europæisk system. Denne artikel fungerer som en dybdegående guide til sponsorer og forskere, der ønsker at ansøge om at udføre kliniske forsøg i Danmark, med særligt fokus på de nye procedurer, krav og den unikke nationalt koordinerede proces for kombinerede studier.
Den Nye Æra: EU's Forordning om Kliniske Forsøg (CTR)
Den primære drivkraft bag ændringerne er EU-forordning nr. 536/2014, bedre kendt som Clinical Trials Regulation (CTR). Formålet med CTR er at skabe en mere effektiv og harmoniseret ramme for kliniske forsøg i hele EU. Dette gøres ved at forenkle processerne og øge gennemsigtigheden. En af de mest markante ændringer er introduktionen af Clinical Trials Information System (CTIS). Dette er en centraliseret EU-portal og database, der fungerer som det eneste indgangspunkt for indsendelse og vurdering af alle ansøgninger om kliniske forsøg med lægemidler i EU/EØS.
Overgangen til det nye system har været gradvis, men siden 31. januar 2023 har det været obligatorisk for alle nye ansøgninger om kliniske forsøg at blive indsendt via CTIS. For forsøg, der allerede var i gang og godkendt under det tidligere direktiv, er der en overgangsperiode. Alle sådanne igangværende forsøg skal være overført til CTIS og administrativt godkendt under CTR senest den 31. januar 2025. Det er sponsorens ansvar at sikre, at denne overførsel sker i tide.
Hvem Behandler Din Ansøgning i Danmark?
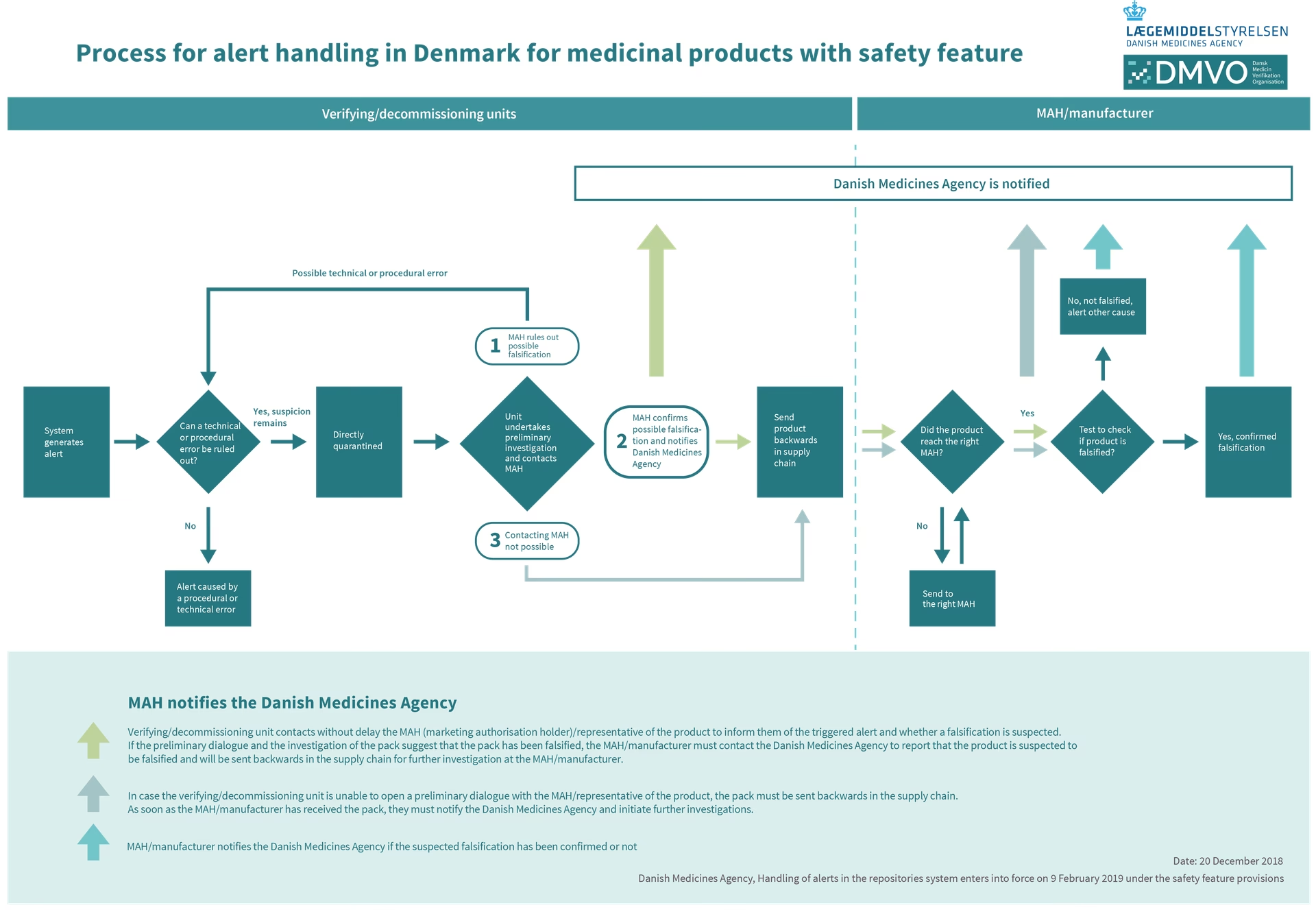
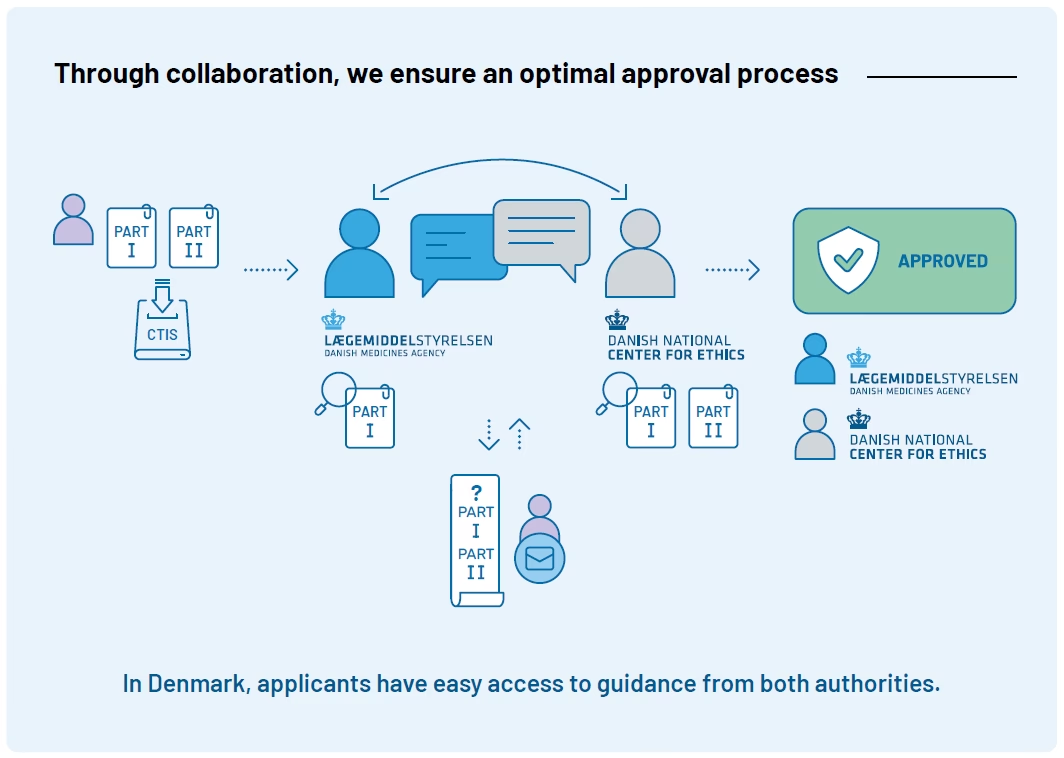
I Danmark varetages behandlingen af ansøgninger om kliniske forsøg af et tæt samarbejde mellem to centrale myndigheder: Lægemiddelstyrelsen (DKMA) og De Videnskabsetiske Medicinske Komiteer (VMK). Når en ansøgning indsendes via CTIS, behandler disse to organer den samtidigt og koordinerer en samlet dansk afgørelse. Lægemiddelstyrelsen fokuserer på lægemidlets sikkerhed og kvalitet, mens VMK vurderer de etiske aspekter af forsøget, herunder beskyttelsen af forsøgsdeltagerne.
Al interaktion mellem ansøger og myndighederne skal foregå gennem CTIS-portalen. Selvom kommunikationen med VMK i CTIS kan foregå på engelsk, er det et ufravigeligt krav, at alt forsøgsmateriale, der er rettet mod forsøgsdeltagerne, såsom samtykkeerklæringer og patientinformation, skal være udarbejdet på dansk.
Sådan Indsender Du en Ansøgning via CTIS
Det er sponsorens eget ansvar at sætte sig ind i brugen af CTIS. Det Europæiske Lægemiddelagentur (EMA), som udvikler og vedligeholder systemet, har heldigvis stillet en række ressourcer til rådighed. Det anbefales kraftigt at benytte sig af:
- EMA's Sponsorhåndbog: En detaljeret vejledning i brugen af systemet.
- EMA's Træningsprogram: Et omfattende program designet til at oplære brugere i alle aspekter af CTIS.
- EU-Kommissionens Q&A: En samling af svar på hyppigt stillede spørgsmål om CTR og dens krav.
Derudover kan man på de danske GCP-enheders hjemmeside finde løbende opdateret information og vejledning specifikt rettet mod danske forhold. De har blandt andet udarbejdet en oversigt over ansøgningsprocessen under CTR og en CTIS-guide på engelsk.

Brug af Skabeloner og Tjeklister
For at sikre, at ansøgningen indeholder alle nødvendige oplysninger, henviser CTR's bilag 1 til en detaljeret oversigt over kravene til indhold. Selvom det ikke er et krav, anbefales det at bruge de skabeloner, der er listet i EUDRALEX volumen 10, kapitel 1. Hvis man vælger ikke at bruge disse, skal man sikre, at alle de påkrævede oplysninger fremgår tydeligt i de relevante dokumenter. For at få en fornemmelse af, hvad myndighederne lægger vægt på i deres vurdering, kan det være nyttigt at se på de rapporter for Del I og Del II, som offentliggøres for afsluttede forsøg på den offentlige del af CTIS-hjemmesiden.
Særlige Udfordringer: Kombinerede Studier (CTR & IVDR)
Kompleksiteten stiger, når et klinisk forsøg med et lægemiddel kombineres med en afprøvning af medicinsk udstyr til in vitro-diagnostik (IVD). Disse kaldes "kombinerede studier". Her skal sponsoren ikke kun overholde CTR, men også forordningen om medicinsk udstyr til in vitro-diagnostik (IVDR). Dette har skabt udfordringer, da det kræver separate godkendelser for både lægemiddelforsøget og afprøvningen af IVD-udstyret, før studiet kan påbegyndes. Godkendelsesprocesserne under IVDR og MDR (forordningen om medicinsk udstyr) er endnu ikke koordineret på EU-niveau, hvilket skaber et behov for nationale løsninger.
Danmarks Løsning: Den Nationalt Koordinerede Ansøgningsproces
For at imødekomme udfordringerne ved kombinerede studier har Danmark introduceret en nationalt koordineret ansøgningsproces. Formålet er at forbedre kvaliteten og strømline godkendelsesproceduren, så sponsorer kan modtage samtidige afgørelser for både lægemiddelforsøget under CTR og afprøvningen under IVDR. Processen sikrer, at ansøgningerne vurderes parallelt af de samme myndigheder og den samme etiske komité, og at den kliniske vurdering hos Lægemiddelstyrelsen er koordineret.
Denne proces er tilgængelig for både mononationale og multinationale kombinerede studier, hvor Danmark er involveret. Det gælder uanset, om Danmark fungerer som Reference Member State (RMS), der leder vurderingen, eller som Member State Concerned (MSC), der deltager i vurderingen. Danmark har desuden erklæret sig villig til at påtage sig rollen som RMS for disse komplekse kombinerede studier.
Trin-for-Trin: Den Koordinerede Proces
For at benytte den koordinerede proces skal sponsorer følge en specifik procedure:
- Parallel Indsendelse: IVDR-ansøgningen skal indsendes til Lægemiddelstyrelsen og VMK op til 5 dage før, men senest samtidig med, at CTR-ansøgningen indsendes i CTIS. Følgebrevet for begge ansøgninger skal tydeligt angive, at der er tale om et 'kombineret studie' og henvise til hinandens sagsnumre (EU CT-nummer og EUDAMED CIV-ID).
- Parallel Validering: Valideringen af begge ansøgninger sker parallelt og følger tidsfristerne i CTIS. Det er afgørende, at sponsor svarer på eventuelle anmodninger om supplerende oplysninger (RFI) for begge ansøgninger samtidigt. Hvis fristerne ikke overholdes, kan den koordinerede proces ikke gennemføres.
- Parallel Vurdering: Selve vurderingen af de faglige og etiske aspekter sker også parallelt. Igen er det altafgørende, at sponsor overholder de RFI-svarfrister, som er fastsat i CTIS, for begge ansøgninger.
- Afgørelse: Sponsor vil modtage en afgørelse for IVDR-ansøgningen kort før afgørelsen for CTR-ansøgningen, typisk senest på dag 45 i processen. Afgørelsen for CTR-ansøgningen følger de gældende tidsfrister i CTIS.
Sammenligning af Ansøgningsspor
| Trin | CTR Ansøgning (Lægemiddel) | IVDR Ansøgning (Diagnostisk Udstyr) |
|---|---|---|
| Indsendelse | Via den centrale EU-portal CTIS. | Via e-mail til Lægemiddelstyrelsen og VMK. Skal ske senest samtidig med CTR-ansøgningen. |
| Validering & Vurdering | Foregår i CTIS med faste tidsfrister. | Foregår parallelt, men følger tidsfristerne for RFI-svar fra CTIS-processen. |
| Kommunikation | Al kommunikation og RFI-svar sker via CTIS. | Kommunikation og RFI-svar sker via e-mail. |
| Afgørelse | Afgørelse meddeles i CTIS efter endt vurdering. | Afgørelse modtages kort før afgørelsen på CTR-ansøgningen. |
Ofte Stillede Spørgsmål (FAQ)
Skal alt ansøgningsmateriale være på dansk?
Nej, selve kommunikationen med myndighederne i CTIS kan foregå på engelsk. Dog er det et absolut krav, at alt materiale, der er rettet mod forsøgsdeltagerne, såsom patientinformation og samtykkeerklæringer, skal være på dansk.
Hvad sker der, hvis jeg misser en RFI-frist i den koordinerede proces?
Hvis svar på RFI for IVDR- og CTR-ansøgningerne ikke indsendes samtidigt og inden for den frist, der er angivet i CTIS, kan den koordinerede proces ikke fuldføres. De to ansøgninger vil derefter blive behandlet som separate sager, hvilket kan forsinke den samlede godkendelse.
Kan jeg stadig ansøge efter de gamle regler fra direktivet?
Nej. Siden den 31. januar 2023 skal alle nye ansøgninger om kliniske forsøg med lægemidler indsendes under CTR via CTIS-portalen. Der er ingen vej udenom.
Hvad er forskellen på RMS og MSC?
I et multinationalt forsøg er Reference Member State (RMS) det medlemsland, der leder vurderingen af ansøgningens Del I (de generelle videnskabelige dele). Member State Concerned (MSC) er de øvrige medlemslande, hvor forsøget skal udføres, og som deltager i vurderingen. Den danske koordinerede proces for kombinerede studier kan anvendes, uanset om Danmark er RMS eller MSC.
Hvor finder jeg de nødvendige skabeloner til min ansøgning?
Det anbefales at bruge skabelonerne fra EUDRALEX volumen 10. For følgebrev og svar på RFI findes der desuden skabeloner udarbejdet af Clinical Trials Coordination Group (CTCG), som kan findes på deres hjemmeside.
Afslutningsvis har overgangen til CTR og CTIS skabt en mere standardiseret, men også mere kompleks ansøgningsproces. Ved at sætte sig grundigt ind i de nye systemer og udnytte de ressourcer og nationale initiativer, som Danmark tilbyder, kan sponsorer sikre en smidig og effektiv vej til godkendelse af deres kliniske forsøg.
Hvis du vil læse andre artikler, der ligner Guide til ansøgning om kliniske forsøg i Danmark, kan du besøge kategorien Sundhed.