29/07/2020
Et lægemiddel er et stof eller en kombination af stoffer, der anvendes til at behandle eller forebygge sygdomme hos mennesker. I en verden, hvor vores sundhed er altafgørende, spiller disse produkter en central rolle. Men hvordan kan vi være sikre på, at den pille, vi tager, eller det medicinske udstyr, der bruges på hospitalet, er sikkert og effektivt? Svaret ligger i et komplekst, men robust juridisk rammeværk, der er etableret af Den Europæiske Union (EU) for at beskytte folkesundheden. Denne ramme sikrer ikke kun produkternes sikkerhed, men adresserer også afgørende emner som forsyningssikkerhed, etisk forskning og kampen mod voksende sundhedstrusler.
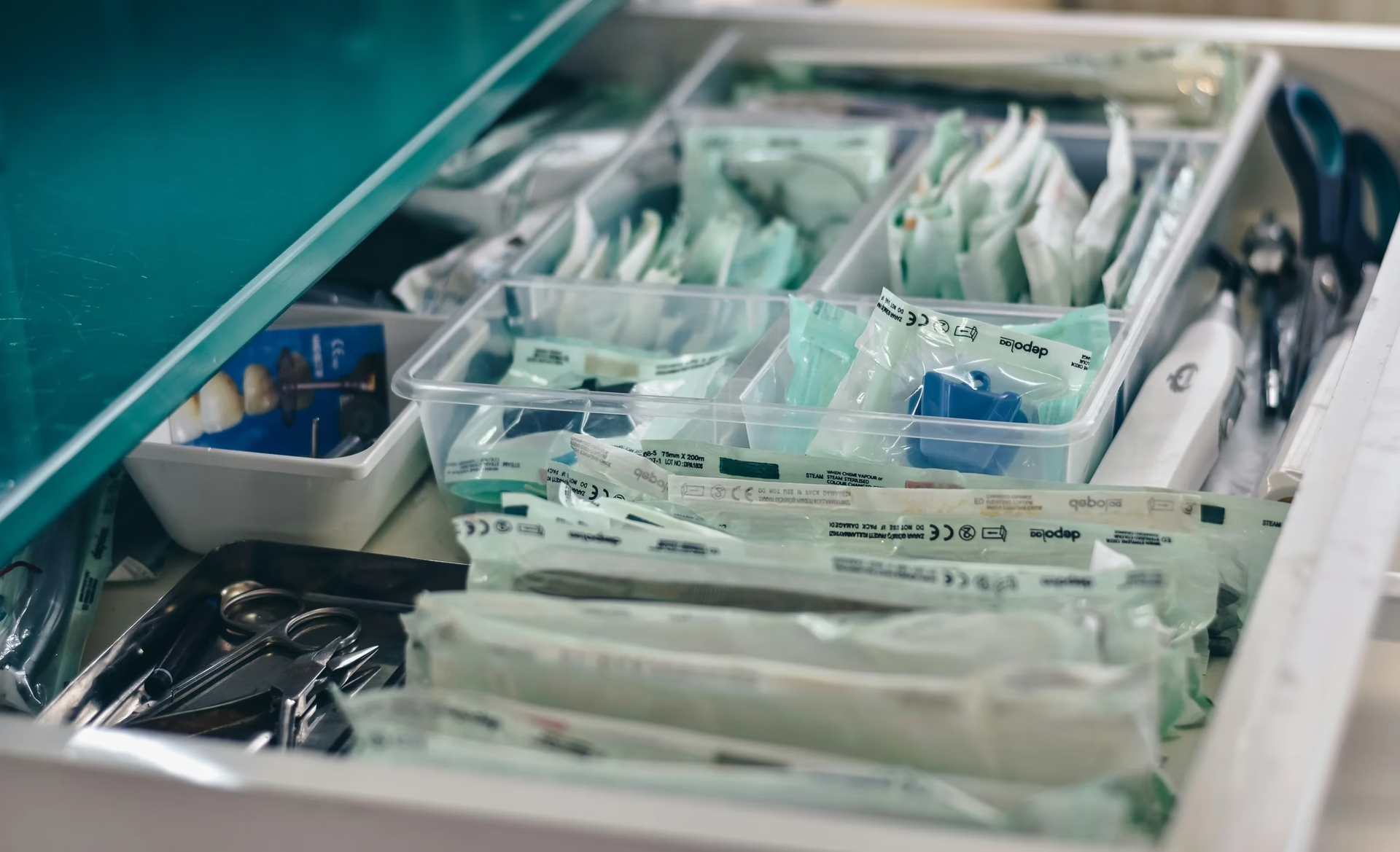
Den Juridiske Ramme: Hvordan EU Beskytter Din Sundhed
EU's kompetence inden for sundhedsområdet er designet til at supplere medlemslandenes eget ansvar for sundhedspolitik. Gennem centrale traktatartikler kan EU vedtage bindende lovgivning for lægemiddel- og medicinsk udstyr, hvilket skaber et harmoniseret indre marked, hvor patientsikkerheden er i højsædet. Kernen i dette system er Det Europæiske Lægemiddelagentur (EMA), som har spillet en afgørende rolle siden 1995.
EMA står for den centraliserede evaluering af de fleste nye lægemidler. Dette betyder, at et lægemiddel kun skal godkendes én gang for at kunne markedsføres i hele EU. Processen er grundig og baseret på videnskabelig vurdering af produktets kvalitet, sikkerhed og virkning. Når et lægemiddel er godkendt og kommer på markedet, stopper overvågningen ikke. Gennem et system kaldet lægemiddelovervågning (pharmacovigilance) indsamler og analyserer EMA løbende data om eventuelle bivirkninger. Dette system sikrer, at uventede risici hurtigt kan identificeres og håndteres, hvilket beskytter patienter i deres daglige brug af medicin.
I april 2023 fremlagde Kommissionen en omfattende 'lægemiddelpakke', der sigter mod at revidere og modernisere den eksisterende lovgivning. Målet er at gøre reglerne mere fremtidssikrede, sikre forsyningen af medicin og fremme innovation, så patienter i hele EU får hurtigere adgang til nye og bedre behandlinger.
Fra Laboratorium til Apotek: Rejsen for et Nyt Lægemiddel
Før et nyt lægemiddel kan nå patienterne, skal det gennemgå en lang og omhyggelig proces med test og evaluering. En af de mest afgørende faser på denne rejse er de kliniske forsøg.
Kliniske forsøg er systematiske undersøgelser af lægemidler på mennesker med det formål at afdække deres virkning og sikkerhed. Disse forsøg er strengt regulerede for at beskytte deltagernes rettigheder, sikkerhed og værdighed. Intet forsøg kan starte uden en forudgående videnskabelig og etisk gennemgang og godkendelse. EU-lovgivningen, især Forordning (EU) nr. 536/2014, har harmoniseret reglerne for kliniske forsøg i hele Unionen. En central del af denne forordning er oprettelsen af EU's informationssystem for kliniske forsøg (CTIS). Denne portal centraliserer ansøgninger og resultater, hvilket skaber en hidtil uset gennemsigtighed og gør det lettere for forskere at samarbejde og for offentligheden at få adgang til information om forskningen.
Særlige Lægemidler til Særlige Behov
Ikke alle lægemidler er ens, og nogle patientgrupper kræver særlig opmærksomhed og specifik lovgivning.
- Lægemidler til børn (Pædiatriske Lægemidler): Børn er ikke små voksne. Deres kroppe omsætter medicin anderledes, og derfor er det afgørende, at lægemidler er testet specifikt til dem. EU-regler sikrer, at medicinalfirmaer undersøger deres produkter på børn på en etisk forsvarlig måde for at fastslå den korrekte dosis og formulering. EMA's Pædiatriske Udvalg vurderer disse studier for at garantere, at medicin til børn er både sikker og effektiv.
- Orphan Drugs (Lægemidler til sjældne sygdomme): En sjælden sygdom defineres i EU som en, der rammer højst 5 ud af 10.000 mennesker. Da patientgrundlaget er lille, er det ofte ikke økonomisk attraktivt for virksomheder at udvikle medicin til disse sygdomme. For at imødekomme dette problem har EU indført en særlig procedure for 'orphan drugs'. Virksomheder, der udvikler disse lægemidler, får en række incitamenter, såsom markedsbeskyttelse og videnskabelig rådgivning, for at fremme forskning og udvikling på dette vitale område.
- Avancerede Terapier (ATMP'er): Dette er en relativt ny kategori af lægemidler baseret på banebrydende fremskridt inden for celle- og molekylærbioteknologi. De omfatter genterapier, celleterapier og vævsteknologi. Disse komplekse behandlinger har et enormt potentiale, men kræver også specialiseret lovgivning for at sikre deres kvalitet og sikkerhed. EMA har et særskilt udvalg til at vurdere disse innovative produkter.
Medicinsk Udstyr: Mere End Bare Piller
Når vi tænker på behandling, er det let kun at fokusere på medicin. Men medicinsk udstyr spiller en lige så vigtig rolle i vores sundhedssystem. Det dækker over et enormt spektrum af produkter – fra simple plastre og sprøjter til avancerede pacemakere, MRI-scannere og diagnostiske tests.
For at øge patientsikkerhed og sikre, at udstyret på markedet er af høj kvalitet, har EU for nylig implementeret to nye, skærpede forordninger: Forordningen om medicinsk udstyr (MDR) og Forordningen om medicinsk udstyr til in vitro-diagnostik (IVDR). Disse forordninger stiller strengere krav til producenterne, herunder:
- Strengere kontrol før markedsføring: Udstyr, især det i højrisikokategorier, skal gennemgå en mere grundig overensstemmelsesvurdering.
- Øget overvågning efter markedsføring: Producenter skal aktivt overvåge deres produkters ydeevne og sikkerhed, når de er i brug.
- Bedre sporbarhed: Et unikt identifikationssystem for udstyr (UDI) gør det muligt at spore hvert enkelt produkt fra producent til patient.
- Europæisk database (EUDAMED): En central database, der vil øge gennemsigtigheden omkring alt medicinsk udstyr på det europæiske marked.
Denne tabel giver et forenklet overblik over risikoklasserne for medicinsk udstyr:
| Risikoklasse | Eksempler | Kontrolniveau |
|---|---|---|
| Klasse I (Lav risiko) | Plastre, bandager, kørestole | Producenten kan som regel selv certificere. |
| Klasse IIa (Mellemrisiko) | Høreapparater, kirurgiske klemmer | Kræver gennemgang af et bemyndiget organ. |
| Klasse IIb (Mellem/høj risiko) | Infusionspumper, respiratorer | Strengere gennemgang af et bemyndiget organ. |
| Klasse III (Højeste risiko) | Pacemakere, hjerteklapper, hofteimplantater | Den mest stringente kontrol og klinisk dokumentation. |
Nutidens Udfordringer i Lægemiddelverdenen
Selvom rammerne er stærke, står sundhedssektoren over for konstante udfordringer, som kræver fælles europæisk handling.
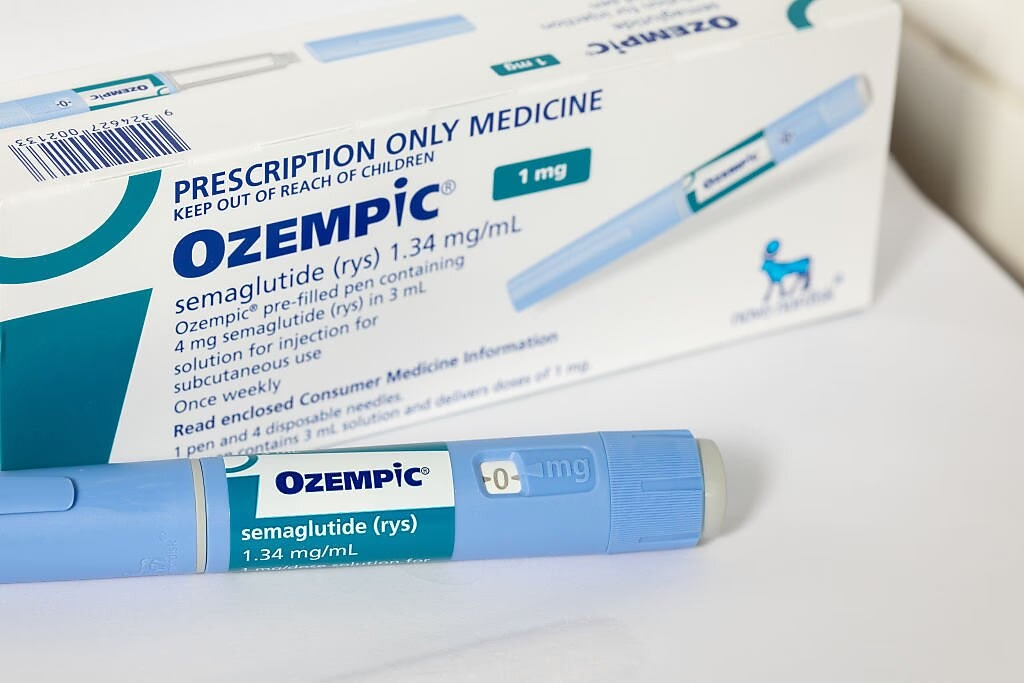
Kampen mod Antibiotikaresistens (AMR)
Antibiotikaresistens er en af de største trusler mod global folkesundhed. Når bakterier udvikler resistens mod antibiotika, bliver almindelige infektioner potentielt dødelige, og mange medicinske procedurer som kirurgi og kemoterapi bliver langt mere risikable. EU bekæmper AMR gennem en 'One Health'-tilgang, der anerkender sammenhængen mellem menneskers, dyrs og miljøets sundhed. Indsatsen fokuserer på at reducere unødvendigt forbrug af antibiotika, fremme udviklingen af nye antimikrobielle midler og styrke overvågningen.
Adgang til Medicin og Forsyningssikkerhed
Selv det bedste lægemiddel er nytteløst, hvis det ikke er tilgængeligt for de patienter, der har brug for det. Mangel på medicin er blevet et stigende problem i Europa, forværret af globale kriser. For at imødekomme dette arbejder EU på flere fronter. EMA har fået en styrket rolle i at overvåge og håndtere mangelsituationer. Desuden er 'Critical Medicines Alliance' blevet oprettet for at samle interessenter og finde løsninger, der kan styrke forsyningskæderne og sikre, at kritiske lægemidler altid er tilgængelige for europæiske borgere.
Ofte Stillede Spørgsmål (FAQ)
Hvad er forskellen på et lægemiddel og medicinsk udstyr?
Et lægemiddel opnår sin primære virkning gennem farmakologiske, immunologiske eller metaboliske midler (dvs. det interagerer kemisk med kroppen). Medicinsk udstyr opnår sit formål gennem fysiske midler (f.eks. en skinne, der støtter et brækket ben, eller en skalpel, der skærer).
Hvem godkender medicin i Danmark og EU?
I EU sker godkendelsen ofte centralt via Det Europæiske Lægemiddelagentur (EMA), hvilket giver markedsføringstilladelse i alle medlemslande. Nationalt er det Lægemiddelstyrelsen i Danmark, der håndterer visse typer godkendelser og fører tilsyn med markedet.
Hvorfor tager det så lang tid at udvikle ny medicin?
Udviklingen af et nyt lægemiddel er en langvarig proces, der kan tage 10-15 år. Det indebærer omfattende forskning, prækliniske tests og flere faser af kliniske forsøg på mennesker for at sikre, at lægemidlet er både sikkert og effektivt, før det kan godkendes.
Hvad gør EU ved mangel på medicin?
EU har styrket EMA's mandat til at forebygge og håndtere medicinmangel. Der er oprettet platforme til overvågning af forsyningen og koordinering mellem medlemslandene. Initiativer som Critical Medicines Alliance arbejder på langsigtede løsninger for at gøre Europas forsyningskæder mere robuste.
EU's omfattende regelsæt for lægemidler og medicinsk udstyr er et dynamisk system, der konstant udvikles for at imødekomme nye videnskabelige fremskridt og samfundsmæssige udfordringer. Fra den første idé i laboratoriet til den endelige behandling af en patient er hver eneste fase omhyggeligt reguleret med ét overordnet formål: at beskytte og forbedre folkesundheden for alle borgere i Unionen.
Hvis du vil læse andre artikler, der ligner Lægemidler i EU: Din Guide til Sikkerhed, kan du besøge kategorien Sundhed.

