15/09/1999
Farmaceutisk fremstilling gennemgår en transformation. Den traditionelle metode, hvor man tester kvaliteten til sidst i produktionsprocessen, bliver erstattet af en mere intelligent og proaktiv tilgang: Quality by Design (QbD). Denne metode har revolutioneret, hvordan medicinalvirksomheder udvikler og producerer lægemidler. I en verden, hvor myndigheder som FDA og EMA i stigende grad lægger vægt på en videnskabsbaseret tilgang, er implementeringen af robuste QbD-principper blevet afgørende for at opretholde konkurrenceevnen og, vigtigst af alt, sikre patienternes sikkerhed. Dette paradigmeskift fra reaktiv kvalitetstestning til proaktiv kvalitetsopbygning repræsenterer et af de mest betydningsfulde fremskridt inden for farmaceutisk praksis, hvilket giver virksomhederne mulighed for at opnå større procesforståelse, forbedret produktkonsistens og øget regulatorisk fleksibilitet.
Hvad er Quality by Design (QbD)?
Quality by Design er en systematisk, videnskabsbaseret tilgang, der integrerer kvalitetsovervejelser gennem hele lægemidlets livscyklus – fra det indledende koncept til den kommercielle fremstilling. I stedet for at stole på testning af slutproduktet for at sikre kvalitet, bygger QbD kvaliteten direkte ind i produkter og processer gennem en forbedret videnskabelig forståelse. Hele filosofien bag QbD centrerer sig om tre kerneprincipper:
- Proaktiv kvalitetsstyring frem for reaktiv kvalitetskontrol.
- Videnskabelig forståelse af sammenhænge mellem produkt og proces.
- Risikobaseret beslutningstagning gennem hele udviklingen og fremstillingen.
Denne tilgang gør det muligt for producenter at forstå, hvordan formuleringskomponenter og procesparametre påvirker det endelige produkts kvalitet, hvilket skaber et robust fundament for konsekvent lægemiddelproduktion.
Fra Kvalitet ved Testning til Kvalitet ved Design
Historisk set har farmaceutisk fremstilling været stærkt afhængig af 'Kvalitet ved Testning' (Quality by Testing, QbT). Denne traditionelle metode medførte adskillige betydelige udfordringer. Den tilbød begrænset procesforståelse og minimal videnskabelig viden om centrale procesvariable. Dette førte til en reaktiv kvalitetsstyring, hvor man var stærkt afhængig af slutprodukttestning, omfattende omarbejdning af partier, der ikke levede op til specifikationerne, og datatunge regulatoriske indsendelser. Overgangen til Quality by Design adresserer disse begrænsninger direkte.
Sammenligning: QbT vs. QbD
| Funktion | Kvalitet ved Testning (QbT) - Traditionel Tilgang | Quality by Design (QbD) - Moderne Tilgang |
|---|---|---|
| Procesforståelse | Begrænset, empirisk baseret. | Dybdegående, videnskabeligt baseret. Forstår sammenhængen mellem parametre og kvalitetsattributter. |
| Kvalitetsstyring | Reaktiv. Kvalitet sikres primært ved testning af slutproduktet. | Proaktiv. Kvalitet bygges ind i designet af produktet og processen. |
| Regulatorisk Fleksibilitet | Meget lav. Ændringer efter godkendelse kræver ofte ny regulatorisk indsendelse. | Høj. Ændringer inden for det godkendte Design Space kan implementeres uden ny godkendelse. |
| Fokus | At reproducere en fastlåst proces. | At opnå et defineret produktkvalitetsmål gennem fleksibel, men kontrolleret proces. |
| Kontinuerlig Forbedring | Begrænset og vanskelig at implementere. | Integreret del af livscyklussen, opmuntres inden for designrummet. |
De Fem Væsentlige Elementer i QbD Implementering
For at implementere QbD succesfuldt, arbejder man med fem centrale elementer, der bygger på hinanden for at skabe en holistisk forståelse af produktet og processen.
1. Kvalitetsmålproduktprofil (QTPP)
QTPP (Quality Target Product Profile) er udgangspunktet. Det definerer de ønskede kvalitetskarakteristika for produktet, med hensyntagen til sikkerhed, effektivitet og patientens behov. Det fungerer som fundamentet for alle efterfølgende QbD-aktiviteter. Komponenter i en QTPP inkluderer:
- Doseringsform og administrationsvej (f.eks. tablet, injektion).
- Dosisstyrke og krav til biotilgængelighed.
- Specifikationer for stabilitet og holdbarhed.
- Kompatibilitet med beholder/lukkesystem.
2. Kritiske Kvalitetsattributter (CQA'er)
CQA'er (Critical Quality Attributes) er målbare fysiske, kemiske, biologiske eller mikrobiologiske egenskaber ved produktet, der skal kontrolleres inden for passende grænser for at sikre den ønskede produktydelse. Eksempler på CQA'er er:
- Analyse og indholdsuniformitet for det aktive farmaceutiske stof (API).
- Opløsningsprofil, som påvirker biotilgængeligheden.
- Fysiske egenskaber som tablethårdhed, sprødhed og desintegrationstid.
- Urenhedsniveauer, der sikrer sikkerhed og stabilitet.
3. Kritiske Materialeattributter (CMA'er)
CMA'er (Critical Material Attributes) identificerer de fysiske, kemiske, biologiske eller mikrobiologiske egenskaber ved inputmaterialer (både API og hjælpestoffer), der har en betydelig indflydelse på produktkvaliteten. Dette kan omfatte API'ets renhed og polymorfe form eller et hjælpestofs partikelstørrelse, som kan påvirke opløseligheden.
4. Kritiske Procesparametre (CPP'er)
CPP'er (Critical Process Parameters) er procesvariable, der har en signifikant indvirkning på produktets CQA'er. At forstå forholdet mellem CPP'er og CQA'er er afgørende for et robust procesdesign. Eksempler inkluderer:
- Blandingsparametre: Tid, hastighed og rækkefølge.
- Granuleringsbetingelser: Væsketilsætningshastighed, endpoint-bestemmelse.
- Kompressionsindstillinger: Kraft, hastighed og opholdstid.
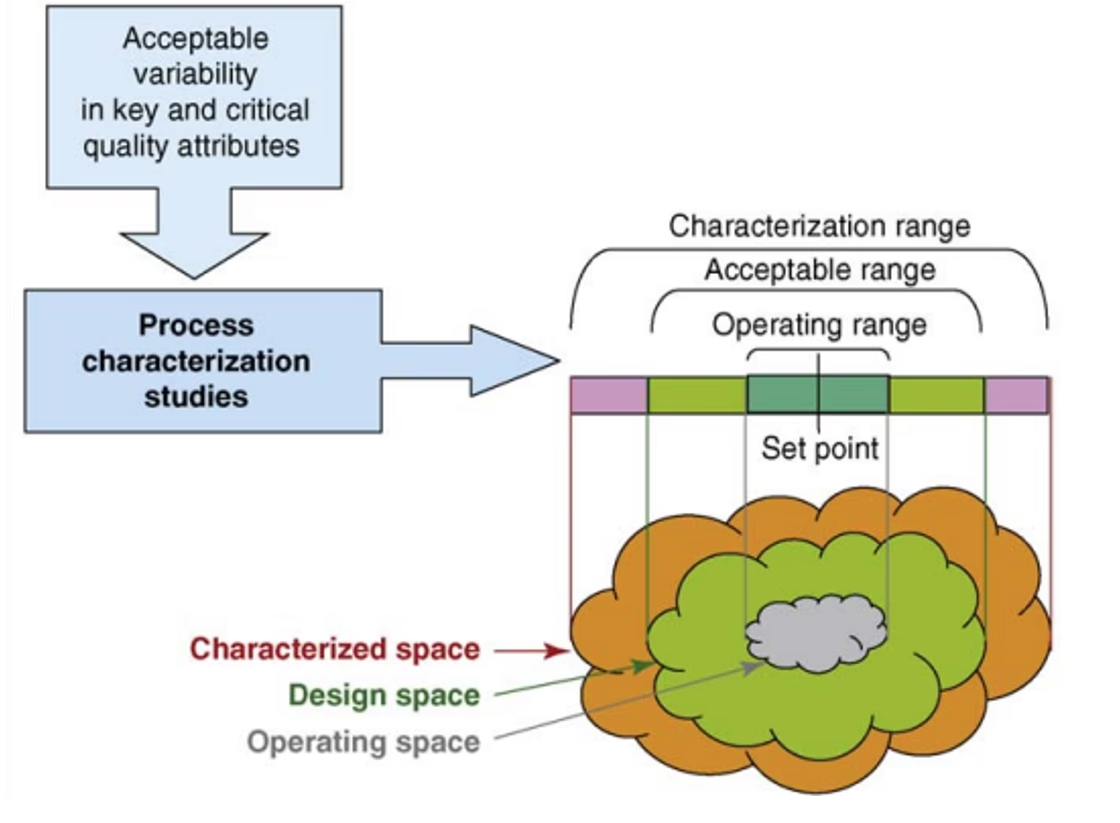
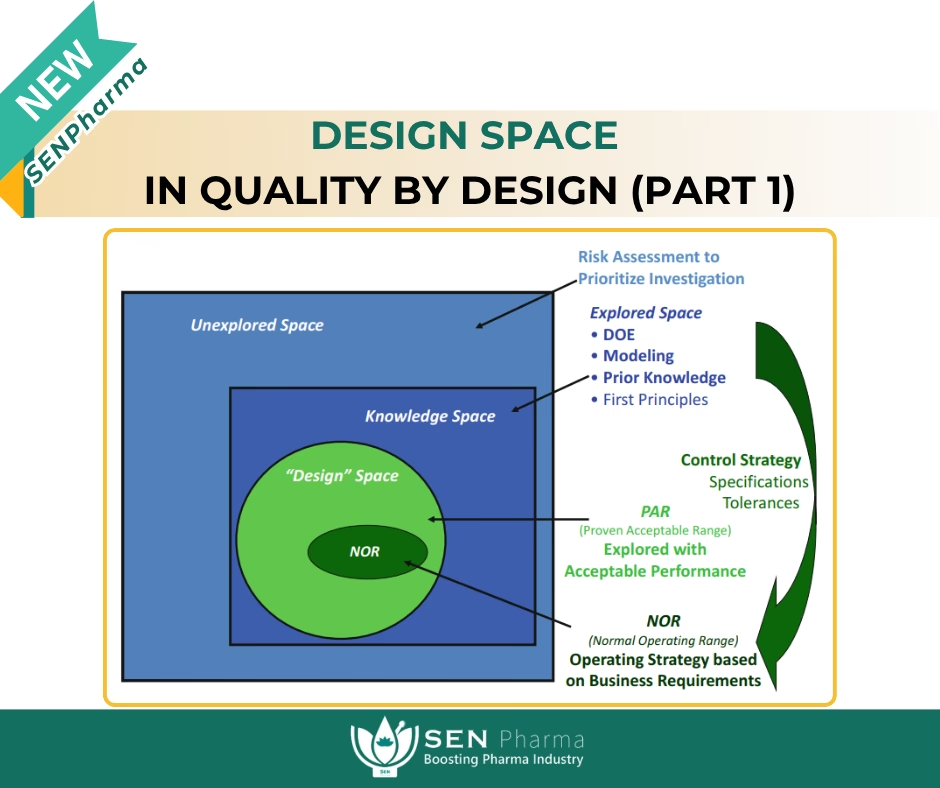
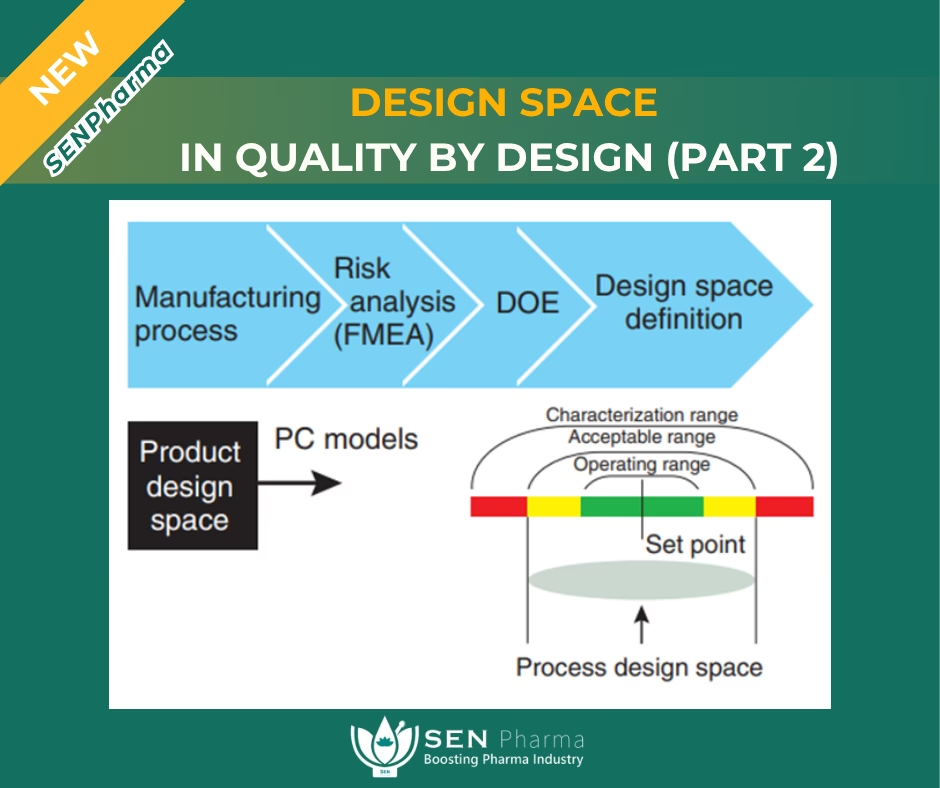
5. Design Space og Kontrolstrategi
Et Design Space er den flerdimensionelle kombination og interaktion af inputvariable (f.eks. materialeattributter) og procesparametre, der har vist sig at give sikkerhed for kvalitet. At operere inden for dette videnskabeligt begrundede rum kræver typisk ikke en ny regulatorisk godkendelse for ændringer. Kontrolstrategien er et planlagt sæt af kontroller, afledt af produkt- og procesforståelse, der sikrer procesydelse og produktkvalitet.

Process Analytisk Teknologi (PAT) - En Nøgle til QbD
Process Analytical Technology (PAT) er en afgørende facilitator for QbD-implementering. PAT giver en realtidsforståelse af fremstillingsprocesser gennem rettidig måling af kritiske kvalitetsattributter. I stedet for at tage prøver ud til et laboratorium og vente på resultater, måler PAT-værktøjer kvaliteten direkte i produktionslinjen. Teknologier som Nær-Infrarød (NIR) spektroskopi kan f.eks. overvåge blandingsuniformitet eller fugtindhold i realtid. Integrationen af PAT giver:
- Forbedret procesforståelse: Kontinuerlig overvågning giver et dynamisk billede af processen.
- Reduceret testbyrde: Realtidsvurdering af kvaliteten kan erstatte traditionel slutprodukttestning.
- Hurtigere batchfrigivelse: Eliminerer forsinkelser fra laboratorietestning.
- Forbedret proceskontrol: Gør det muligt at foretage proaktive justeringer for at holde processen inden for specifikationerne.
Fordele og Udfordringer ved QbD
Implementering af Quality by Design giver en lang række fordele, men det er ikke uden udfordringer.
Fordele
- Operationelle: En "rigtig første gang"-tilgang reducerer batchfejl og omarbejdning markant. Dette fører til lavere produktionsomkostninger og øget effektivitet.
- Kvalitet og Regulatorisk: Fører til mere konsistent produktkvalitet og reduceret variabilitet fra batch til batch. Den øgede procesforståelse giver betydelig regulatorisk fleksibilitet.
- Strategiske: Fremmer en kultur med kontinuerlig forbedring og innovation. Det styrker også forsyningskædens modstandsdygtighed gennem bedre leverandørkvalificering og styring.
Udfordringer
- Organisatoriske: Kræver en kulturændring og opbakning fra alle afdelinger. Modstand mod at ændre etablerede praksisser kan være en betydelig hindring.
- Tekniske: Kræver betydelige startinvesteringer i nyt udstyr (f.eks. PAT-instrumenter) og træning. Håndtering af de store datamængder kræver robuste IT-systemer.
- Regulatoriske: Selvom principperne er harmoniseret (f.eks. via ICH-guidelines), kan der være forskellige forventninger på tværs af globale markeder.
Fremtiden for QbD
Fremtiden for QbD er tæt forbundet med den digitale transformation af industrien, ofte kaldet Pharma 4.0. Integrationen af kunstig intelligens (AI) og machine learning vil muliggøre prædiktiv modellering for procesoptimering og automatiseret afvigelsesdetektion. Teknologier som Internet of Things (IoT) sensorer vil give endnu mere omfattende procesovervågning. Desuden vil QbD-principper være centrale for udviklingen af avancerede fremstillingsteknologier som kontinuerlig produktion og 3D-printning af lægemidler, hvilket åbner døren for mere personaliseret medicin.
Ofte Stillede Spørgsmål (FAQ)
- Hvad er forskellen mellem QbD og traditionelle kvalitetstilgange?
- QbD bygger proaktivt kvalitet ind i produkter og processer gennem videnskabelig forståelse, mens traditionelle tilgange primært er afhængige af testning af slutproduktet for at sikre kvalitet. QbD muliggør kontinuerlig forbedring og regulatorisk fleksibilitet inden for etablerede designrum.
- Hvad er CPP og CQA i farmaceutisk fremstilling?
- Kritiske Procesparametre (CPP'er) er procesvariable, der signifikant påvirker produktkvaliteten. Kritiske Kvalitetsattributter (CQA'er) er målbare produktegenskaber, der skal kontrolleres for at sikre den ønskede ydeevne. At forstå forholdet mellem CPP og CQA er fundamentalt for QbD.
- Hvordan relaterer ICH Q8 til Quality by Design?
- ICH Q8-guideline ("Pharmaceutical Development") udgør det regulatoriske fundament for QbD. Den opfordrer til en forbedret tilgang til farmaceutisk udvikling og gør det muligt for producenter at etablere et Design Space, inden for hvilket procesændringer kan foretages uden ny regulatorisk godkendelse.
- Hvilken rolle spiller risikovurdering i QbD?
- Risikostyring (i henhold til ICH Q9-principperne) er en integreret del af QbD. Det hjælper med at identificere og prioritere kritiske attributter og parametre, guide eksperimentelt design og etablere passende kontrolstrategier baseret på den potentielle indvirkning på produktkvalitet og patientsikkerhed.
Hvis du vil læse andre artikler, der ligner Kvalitet ved Design (QbD) i Lægemidler, kan du besøge kategorien Farmaci.