06/01/2008
I den moderne medicinske verden hører vi ofte om nye og avancerede behandlinger. Biologiske lægemidler er en af de mest betydningsfulde landvindinger, men de er ofte forbundet med høje omkostninger. Her kommer biosimilars ind i billedet som et afgørende alternativ. Men hvad er et biosimilar egentlig? Er det det samme som det originale lægemiddel, kendt som referencemedicinen? Svaret er, at det er et 'biosimilar' – et lægemiddel, der er udviklet til at være meget lig et eksisterende biologisk lægemiddel, men ikke identisk. Denne artikel vil afdække den komplekse, men fascinerende verden af biosimilars og den strenge proces, de skal igennem for at blive godkendt til brug i EU.
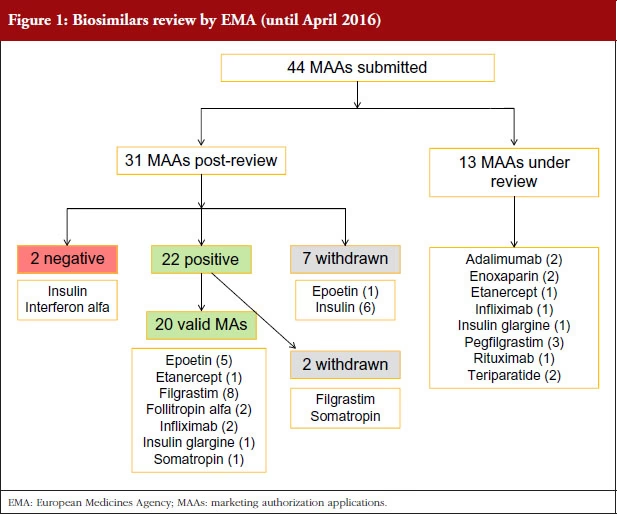
Hvad er et biologisk lægemiddel?
Før vi kan forstå biosimilars, må vi først forstå, hvad et biologisk lægemiddel er. I modsætning til traditionelle kemiske lægemidler, som f.eks. aspirin eller paracetamol, der er fremstillet gennem kemisk syntese og har en simpel, veldefineret struktur, er biologiske lægemidler langt mere komplekse. De fremstilles ved hjælp af levende organismer som bakterier, gærceller eller dyreceller. Denne proces gør dem meget større og mere komplekse i deres struktur.
Eksempler på biologiske lægemidler inkluderer:
- Monoklonale antistoffer til behandling af kræft og autoimmune sygdomme som leddegigt.
- Insulin til behandling af diabetes.
- Væksthormoner.
- Vacciner.
På grund af deres komplekse natur og fremstillingsproces er det praktisk talt umuligt at skabe en 100% identisk kopi af et biologisk lægemiddel, selv for den oprindelige producent. Små, naturlige variationer vil altid eksistere fra batch til batch. Det er denne kompleksitet, der fører til begrebet 'biosimilar' i stedet for 'generisk'.
Biosimilar vs. Referencemedicin: En afgørende forskel
Når patentet på et originalt biologisk lægemiddel (herefter kaldet referencemedicin) udløber, kan andre virksomheder udvikle og markedsføre deres egne versioner. Disse versioner kaldes biosimilars. Et biosimilar er altså et biologisk lægemiddel, der er udviklet til at være meget lig (similar) et allerede godkendt referencemedicin.
Hovedformålet med udviklingen af et biosimilar er ikke at genopfinde den dybe tallerken, men at bevise, at det er lige så sikkert og effektivt som det originale produkt. Hele godkendelsesprocessen er bygget op omkring en omfattende sammenligningsøvelse.
Den Strenge Godkendelsesproces hos EMA
For at et biosimilar kan blive markedsført i EU, skal det gennemgå en yderst grundig evaluering hos Det Europæiske Lægemiddelagentur (EMA - European Medicines Agency). Ansøgeren skal indsende en omfattende dokumentationspakke, kendt som Common Technical Document (CTD), der beviser ligheden med referencemedicinen. Denne proces er designet til at sikre, at der ikke er nogen klinisk meningsfulde forskelle mellem de to produkter med hensyn til kvalitet, sikkerhed og effekt.
Ansøgningen er opdelt i fem moduler:
- Modul 1: Administrativ Information. Dette modul indeholder et afgørende resumé, der forklarer, hvorfor lægemidlet betragtes som et biosimilar. Her beskrives ligheder og eventuelle mindre forskelle i fremstillingsprocessen i forhold til referencemedicinen.
- Modul 2: Resuméer. Indeholder overordnede sammenfatninger af lægemidlets kvalitet samt de prækliniske og kliniske data. Her fremhæves sammenlignelighedsresultaterne.
- Modul 3: Kvalitetsdata. Dette er en ekstremt detaljeret sektion, der beskriver alt om fremstillingsprocessen, råmaterialer og kvalitetskontrol. Kernen her er den direkte sammenlignelighedsøvelse, hvor biosimilaret analyseres og sammenlignes med referencemedicinen på et molekylært niveau for at demonstrere, at de er strukturelt og funktionelt meget ens.
- Modul 4 & 5: Prækliniske og Kliniske Data. I modsætning til et helt nyt lægemiddel behøver et biosimilar ikke at gentage alle de store, tidskrævende kliniske forsøg, som referencemedicinen gennemgik. I stedet udføres målrettede prækliniske (laboratorie- og dyreforsøg) og kliniske studier (på mennesker) for at bekræfte, at de små, uundgåelige forskelle i molekylet ikke har nogen indflydelse på, hvordan lægemidlet opfører sig i kroppen. Disse studier fokuserer typisk på farmakokinetik (hvordan kroppen optager og udskiller lægemidlet) og farmakodynamik (hvordan lægemidlet påvirker kroppen) samt studier for at bekræfte sikkerhed og effekt i mindst én patientgruppe.
Det er afgørende, at den referencemedicin, der bruges i alle disse sammenlignende studier, er et produkt, der er godkendt og markedsført i EU/EØS.
Sammenligning: Biosimilar vs. Generisk Medicin
Det er en almindelig misforståelse at tro, at et biosimilar er det samme som et generisk lægemiddel. Tabellen nedenfor illustrerer de vigtigste forskelle.
| Egenskab | Biosimilar | Generisk Medicin |
|---|---|---|
| Originalt Produkt | Biologisk lægemiddel (stort, komplekst molekyle) | Kemisk lægemiddel (lille, simpelt molekyle) |
| Fremstilling | Via levende celler/organismer | Kemisk syntese |
| Struktur | Meget lig, men ikke identisk med referencen | Identisk med det originale lægemiddel |
| Godkendelseskrav | Omfattende sammenlignelighedsøvelse (kvalitet, prækliniske og kliniske data) | Bioækvivalensstudie (beviser samme optagelse i kroppen) |
| Dataomfang | Meget stort og komplekst | Relativt simpelt |
Sikkerhed og Overvågning efter Godkendelse
Ligesom alle andre lægemidler i EU er biosimilars underlagt streng overvågning, efter de er kommet på markedet. Som en del af ansøgningen skal producenten indsende en detaljeret risikostyringsplan (Risk Management Plan). Denne plan beskriver, hvordan virksomheden vil fortsætte med at overvåge lægemidlets sikkerhed og effektivitet og håndtere eventuelle nye risici, der måtte opstå. Dette sikrer, at patienternes sikkerhed altid er i højsædet, også mange år efter godkendelsen.
Ofte Stillede Spørgsmål (FAQ)
Er biosimilars lige så sikre og effektive som de originale lægemidler?
Ja. Den strenge godkendelsesproces hos EMA sikrer, at et godkendt biosimilar har den samme høje standard for kvalitet, sikkerhed og effekt som referencemedicinen. Patienter og læger kan have fuld tillid til, at et biosimilar vil have den samme kliniske virkning.
Hvorfor er biosimilars ofte billigere?
Producenter af biosimilars skal ikke bære de enorme omkostninger til den oprindelige forskning og udvikling, som producenten af referencemedicinen har afholdt. De skal heller ikke udføre det samme omfattende program af kliniske forsøg. I stedet fokuserer de på at bevise ligheden. Denne mere effektive udviklingsvej, kombineret med øget konkurrence på markedet, fører til lavere priser. Dette frigør ressourcer i sundhedsvæsenet, som kan bruges på andre områder, og giver flere patienter adgang til vigtig behandling.
Kan jeg trygt skifte fra et referencelægemiddel til et biosimilar?
Et skifte fra et referencelægemiddel til et biosimilar (eller mellem forskellige biosimilars) betragtes generelt som sikkert og effektivt. Beslutningen om et eventuelt skifte skal dog altid træffes i samråd med din behandlende læge, som kender din specifikke medicinske situation.
Så et biosimilar er definitivt ikke en 'referencemedicin'?
Korrekt. Et biosimilar er en efterfølger til en referencemedicin. Selve navnet 'biosimilar' understreger dets forhold til det originale, allerede godkendte lægemiddel. Det er en kategori for sig selv, skabt for at anerkende den unikke natur af biologiske lægemidler.
Hvis du vil læse andre artikler, der ligner Biosimilars: Hvad er de, og hvordan godkendes de?, kan du besøge kategorien Medicin.
