07/03/2017
Rabies er et navn, der ofte fremkalder billeder af en farlig og dødelig sygdom. Men i den moderne neurovidenskabs verden har forskere formået at tæmme dette virus og omdanne det til et af de mest kraftfulde værktøjer til at forstå hjernens indre funktioner. Ved at fjerne en enkelt, men afgørende, genetisk komponent har de skabt det G-slettede rabiesvirus – en modificeret version, der sikkert og med hidtil uset præcision kan kortlægge de indviklede neurale kredsløb, der ligger til grund for vores tanker, bevægelser og følelser. Denne teknologi repræsenterer et kvantespring i vores evne til at afkode nervesystemets kompleksitet og åbner nye døre for forskning i neurologiske og psykiatriske lidelser.
Hvad er et G-slettet Rabiesvirus?
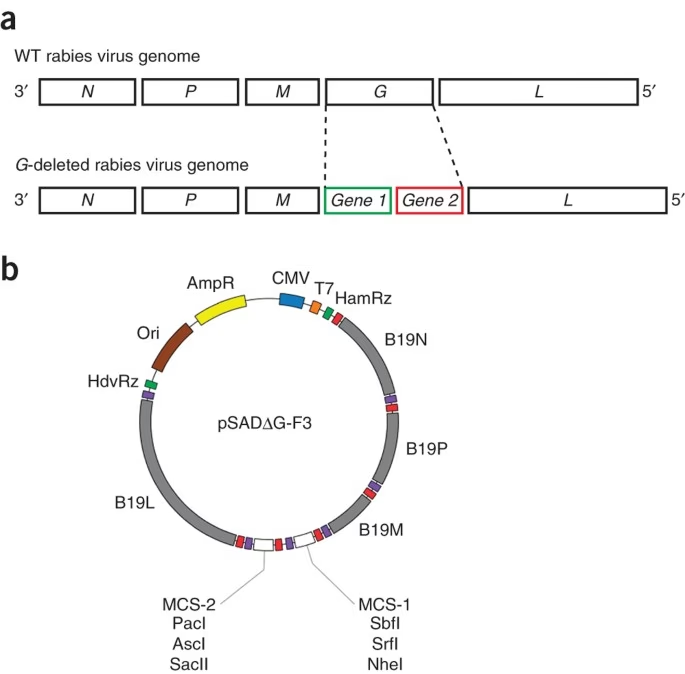
For at forstå, hvad et G-slettet rabiesvirus er, må vi først se på det oprindelige virus. Rabiesvirus er et neurotropt virus, hvilket betyder, at det har en naturlig forkærlighed for at inficere nerveceller (neuroner). En afgørende del af virussets struktur er et overfladeprotein kendt som glykoprotein (forkortet 'G'). Dette protein fungerer som en slags universelnøgle, der giver virusset mulighed for at binde sig til receptorer på overfladen af en neuron og trænge ind i den. Endnu vigtigere er det, at glykoproteinet er essentielt for, at virusset kan sprede sig fra en inficeret neuron til den næste hen over synaptiske kløfter – de små mellemrum, hvor neuroner kommunikerer med hinanden.
Forskere har ved hjælp af genteknologi fjernet genet, der koder for dette glykoprotein, fra virussets genom. Resultatet er et 'G-slettet' rabiesvirus. Dette modificerede virus kan stadig inficere en nervecelle, hvis det introduceres direkte, og det kan replikere sit genetiske materiale inde i cellen. Men uden glykoproteinet kan de nye viruspartikler, der dannes, ikke forlade den inficerede celle for at inficere naboceller. Virusset er med andre ord blevet fanget; det er sprednings-inkompetent. Denne ene ændring forvandler et ukontrollerbart patogen til et yderst kontrollerbart forskningsværktøj.
Fra Patogen til Præcisionsværktøj: Monosynaptisk Retrograd Sporing
Den virkelige genialitet ved det G-slettede rabiesvirus ligger i, hvordan det bruges til en teknik kaldet monosynaptisk retrograd sporing. Målet med denne teknik er at identificere alle de neuroner, der sender direkte signaler til én bestemt, udvalgt neuron. Forestil dig hjernen som et gigantisk, komplekst vejnet. Forskerne ønsker ikke at se hele kortet på én gang, men kun de veje, der fører direkte til ét specifikt kryds. Processen foregår typisk i flere trin:
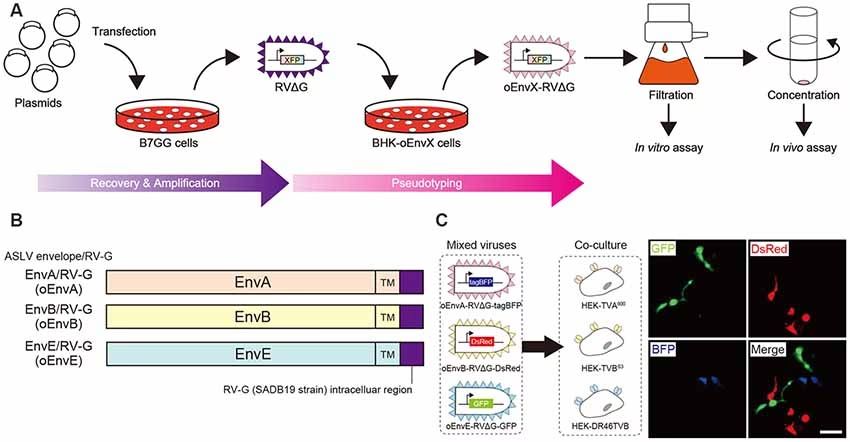
- Trin 1: Forberedelse af 'startcellen'. Først identificerer forskerne den specifikke neuron eller gruppe af neuroner, de vil undersøge (vi kalder den 'startcellen'). Ved hjælp af et harmløst 'hjælpevirus' (ofte et adeno-associeret virus, AAV) udstyres denne startcelle med to nye gener. Det ene gen er for selve rabies-glykoproteinet (G), og det andet er for en receptor (TVA), som det modificerede rabiesvirus specifikt kan binde sig til. Dette sikrer, at kun denne ene celle i første omgang kan blive inficeret af rabiesvirusset.
- Trin 2: Introduktion af det G-slettede rabiesvirus. Nu introduceres det G-slettede rabiesvirus, som også er blevet udstyret med et gen for et fluorescerende protein (som f.eks. grønt fluorescerende protein, GFP). Virusset kan nu kun inficere startcellen, fordi det kun er dén, der har TVA-receptoren.
- Trin 3: Den ene synaptiske spredning. Inde i startcellen begynder rabiesvirusset at replikere sig. Fordi cellen midlertidigt producerer glykoproteinet fra hjælpevirusset, bliver de nye rabiespartikler pakket med dette G-protein på deres overflade. Disse komplette viruspartikler kan nu rejse 'baglæns' (retrogradt) over synapserne og inficere alle de neuroner, der er direkte forbundet med startcellen.
- Trin 4: Sporingen stopper. Når rabiesvirusset ankommer til disse 'anden-ordens' neuroner, kan det ikke sprede sig yderligere. Disse neuroner har nemlig ikke fået tilført genet for glykoproteinet, så de nye viruspartikler, der dannes her, mangler den nødvendige 'nøgle' til at inficere flere celler.
Resultatet er, at kun startcellen og alle de neuroner, der er præsynaptiske (dvs. sender input) til den, lyser grønt under et mikroskop. Forskerne har dermed skabt et præcist og statisk kort over et enkelt, funktionelt neuralt mikrokredsløb.
Fordele Sammenlignet med Andre Metoder
Før udviklingen af det G-slettede rabiesvirus var forskere afhængige af andre, mindre præcise metoder til at spore neurale forbindelser. Her er en sammenligning, der illustrerer fordelene:
| Metode | Præcision | Retning | Sikkerhed | Begrænsninger |
|---|---|---|---|---|
| G-slettet Rabiesvirus | Monosynaptisk (ét trin) | Primært retrograd | Høj (sprednings-inkompetent) | Kræver genetisk manipulation af startceller |
| Klassiske virale tracere (f.eks. Herpesvirus) | Polysynaptisk (flere trin) | Retrograd og anterograd | Moderat til lav (ukontrolleret spredning) | Svært at bestemme antallet af synaptiske trin |
| Kemiske tracere (f.eks. HRP, dextraner) | Variabel, kan fortyndes over afstand | Retrograd eller anterograd | Høj | Kan ikke krydse synapser effektivt; mærker kun axoner |
Anvendelser i Forskning og Medicin
Denne teknologis indvirkning på neurovidenskab er enorm. Forskere bruger den til at besvare fundamentale spørgsmål om hjernen, som før var uden for rækkevidde:
- Kortlægning af motoriske systemer: Ved at starte i en motorneuron i rygmarven, der styrer en specifik muskel, kan forskere spore hele kommandovejen tilbage til de områder i hjernen, der initierer bevægelsen. Dette er afgørende for at forstå sygdomme som ALS og Parkinsons sygdom.
- Afkodning af sansekredsløb: Forskere kan undersøge, hvordan information fra vores sanser (syn, hørelse, følesans) behandles trin for trin ved at spore forbindelserne fra de primære sanseområder i hjernen.
- Forståelse af kognition og følelser: Ved at målrette neuroner i områder som hippocampus (hukommelse) eller amygdala (frygt) kan man identificere de netværk, der ligger til grund for komplekse kognitive funktioner og følelsesmæssige reaktioner.
- Identifikation af nye behandlingsmål: Ved præcist at vide, hvordan hjerneområder er forbundet, kan forskere bedre identificere, hvor man kan gribe ind med behandlinger som dyb hjernestimulation (DBS) for lidelser som epilepsi eller svær depression.
Teknologien giver et hidtil uset detaljeret øjebliksbillede af hjernens 'ledningsdiagram', hvilket er et essentielt fundament for at forstå både normal hjernefunktion og de fejl, der opstår ved sygdom.
Ofte Stillede Spørgsmål
Er G-slettet rabiesvirus farligt for forskerne eller offentligheden?
Nej. Netop fordi genet for glykoprotein er fjernet, kan virusset ikke sprede sig fra celle til celle af sig selv. Det er klassificeret som et biosikkerhedsniveau 2 (BSL-2) agens, hvilket betyder, at det håndteres under kontrollerede laboratorieforhold, men det udgør ikke en fare for folkesundheden. Det er fundamentalt anderledes end det vilde rabiesvirus.
Hvorfor bruge et virus i stedet for en anden metode?
Virus er naturens egne mestre i at trænge ind i celler og udnytte deres maskineri. Forskere udnytter denne evolutionært finpudsede evne. Specifikt er rabiesvirus' evne til at bevæge sig effektivt og retningsbestemt over synapser noget, som syntetiske eller kemiske metoder endnu ikke kan efterligne med samme præcision og effektivitet.
Kan denne teknologi bruges til at behandle hjernesygdomme?
Ikke direkte som en behandling i sig selv. G-slettet rabiesvirus er primært et forskningsværktøj – et kortlægningsinstrument. Men den viden, vi opnår ved hjælp af dette værktøj, er fundamental for udviklingen af fremtidige behandlinger. Ved at forstå, hvilke neurale kredsløb der er dysfunktionelle i f.eks. skizofreni eller kronisk smerte, kan medicinalfirmaer og læger udvikle mere målrettede og effektive terapier.
Hvis du vil læse andre artikler, der ligner G-slettet rabiesvirus: Hjernens kortlægger, kan du besøge kategorien Sundhed.