23/06/2016
Klinisk forskning er i en rivende udvikling. Den traditionelle model, hvor patienter jævnligt skal rejse til et centralt hospital for at deltage i et forsøg, udfordres af nye, mere fleksible og patientvenlige metoder. En af de mest lovende udviklinger er decentraliserede kliniske forsøg (DCTs). I Danmark spiller Lægemiddelstyrelsen (DKMA) en afgørende rolle i at fremme og understøtte denne transformation. Med en vision om at være en facilitator for innovation, arbejder styrelsen aktivt på at skabe et regulatorisk miljø, der omfavner fremtidens forskningsmetoder til gavn for både patienter og life science-sektoren.
Denne artikel dykker ned i, hvordan Lægemiddelstyrelsen konkret understøtter implementeringen af decentraliserede kliniske forsøg, hvilken rolle Danmarks unikke sundhedsdata spiller, og hvordan europæisk samarbejde er med til at forme fremtidens kliniske forskning.
Hvad Er Decentraliserede Kliniske Forsøg?
Før vi ser på Lægemiddelstyrelsens rolle, er det vigtigt at forstå, hvad et decentraliseret klinisk forsøg egentlig er. I sin essens er et DCT et forsøg, hvor nogle eller alle forsøgsrelaterede aktiviteter foregår steder, der er mere bekvemme for deltageren, typisk i deres eget hjem eller på en lokal klinik, frem for på et centralt forskningscenter.
Dette er muliggjort af en kombination af teknologiske fremskridt og nye metoder:
- Digitale Værktøjer: Smartphones, apps, bærbare sensorer (wearables) og andre digitale enheder bruges til at indsamle data direkte fra patienten, uanset hvor de befinder sig. Det kan være alt fra rapportering af symptomer til måling af puls og aktivitetsniveau.
- Telemedicin: Videokonsultationer med læger og sygeplejersker erstatter mange fysiske besøg, hvilket sparer patienten for tid og rejseomkostninger.
- Hjemmebesøg: Specialiserede sygeplejersker kan udføre visse procedurer, såsom blodprøvetagning, direkte i patientens hjem.
- Lokal Logistik: Forsøgsmedicin kan sendes direkte til patientens adresse, og lokale apoteker eller klinikker kan inddrages i processen.
Målet er at gøre deltagelse i klinisk forskning mindre byrdefuld og mere integreret i patientens hverdag. Dette kan føre til hurtigere rekruttering, lavere frafald og adgang til en mere mangfoldig patientpopulation, som måske ikke ville kunne deltage i et traditionelt forsøg på grund af geografisk afstand eller mobilitetsproblemer.
Lægemiddelstyrelsens Strategiske Støtte til DCTs
Lægemiddelstyrelsen, under ledelse af direktør Nils Falk Bjerregaard, har anerkendt potentialet i decentraliserede forsøg og arbejder målrettet på at skabe de bedste rammer for deres udbredelse i Danmark. Dette er en del af en bredere strategi, der flugter med Danmarks Life Science Strategi 2030, hvor styrelsen ser sig selv som en "facilitator for innovation" snarere end blot en regulator.
Udvikling af Nationale Retningslinjer
Et af de mest konkrete skridt, Lægemiddelstyrelsen har taget, er udviklingen af nationale retningslinjer for decentraliserede kliniske forsøg. Disse retningslinjer giver forskere og virksomheder klarhed over, hvad der forventes, og hvordan man kan designe og udføre et DCT, der lever op til de højeste standarder for patientsikkerhed og datakvalitet. Ved at skabe en gennemsigtig og forudsigelig ramme reduceres usikkerheden for sponsorer og forskere. Responsen fra det kliniske forskningsmiljø har været overvældende positiv, hvilket indikerer et stort behov for denne type vejledning.
Fokus på Dialog og Samarbejde
Styrelsen har bevæget sig væk fra en lukket tilgang og prioriterer i stedet en åben dialog med alle interessenter – fra industri og akademia til sundhedspersonale og patientorganisationer. Gennem både formelle platforme som interessentfora og uformelle udvekslinger sikrer Lægemiddelstyrelsen, at de regulatoriske rammer er både videnskabeligt robuste og operationelt fornuftige. Denne samarbejdsorienterede tilgang sikrer, at regulering ikke bliver en utilsigtet barriere for innovation, men derimod en støtte, der hjælper med at bringe nye behandlinger hurtigere og mere effektivt til patienterne.
Danmarks Unikke Data-Infrastruktur som Drivkraft
En af Danmarks absolutte styrker i denne sammenhæng er landets avancerede digitale infrastruktur og omfattende sundhedsregistre. Dette giver en unik position til at udnytte Real-World Data (RWD) og understøtte moderne forsøgsdesigns som DCTs.
Fra Sundhedsdata til Real-World Evidence
Hver borger i Danmark har et unikt CPR-nummer, som muliggør en sømløs kobling af sundhedsdata på tværs af sektorer. Dette skaber et solidt fundament for at anvende RWD – data indsamlet uden for rammerne af traditionelle kliniske forsøg – til at supplere og berige den viden, der opnås i kliniske studier. RWD er især kritisk inden for områder som sjældne sygdomme og personlig medicin, hvor store, randomiserede studier er vanskelige at gennemføre. Lægemiddelstyrelsen har accelereret sit arbejde med RWD, blandt andet gennem etableringen af Data Analytics Centre (DAC) i 2020. Målet er at øge antallet af RWD-projekter markant og dermed styrke beslutningsgrundlaget for godkendelse og overvågning af lægemidler. Denne datadrevne tilgang er en perfekt partner til DCTs, hvor data ofte indsamles kontinuerligt i patientens naturlige miljø.
Offentlig Tillid er Afgørende
Brugen af sundhedsdata er afhængig af en høj grad af samfundsmæssig tillid. I Danmark er der generelt stor tiltro til, at myndigheder håndterer data ansvarligt. Lægemiddelstyrelsen er meget bevidst om, at denne tillid skal bevares gennem fuld gennemsigtighed, streng overholdelse af GDPR-lovgivningen og klar kommunikation om formålene med dataindsamlingen. Uden denne tillid ville fundamentet for både RWD-initiativer og dataintensive DCTs smuldre.

Sammenligning: Traditionelle vs. Decentraliserede Forsøg
For at illustrere forskellene og fordelene ved den nye tilgang, er her en sammenligningstabel:
| Aspekt | Traditionelt Klinisk Forsøg | Decentraliseret Klinisk Forsøg (DCT) |
|---|---|---|
| Lokation | Centraliserede forskningscentre (hospitaler) | Patientens hjem, lokale klinikker |
| Patientbyrde | Høj (rejsetid, fravær fra arbejde, omkostninger) | Lav (minimal rejse, fleksibilitet) |
| Dataindsamling | Episodisk, under klinikbesøg | Kontinuerlig, via digitale enheder og apps |
| Rekruttering | Begrænset af geografi, ofte langsom | Bredere geografisk rækkevidde, ofte hurtigere |
| Diversitet | Ofte begrænset til befolkninger nær centrene | Potentielt højere, inkluderer flere patientgrupper |
Europæisk Samarbejde Fremmer Udviklingen
Selvom mange initiativer er nationale, er Lægemiddelstyrelsens arbejde tæt forbundet med det europæiske regulatoriske landskab. De fleste godkendelser af avancerede lægemidler sker gennem centraliserede procedurer i Det Europæiske Lægemiddelagentur (EMA), hvor Danmark er en aktiv og indflydelsesrig deltager.
COMBINE-initiativet
Et eksempel på europæisk samarbejde er COMBINE-initiativet, der sigter mod at harmonisere kravene til kliniske forsøg, der involverer både lægemidler og medicinsk udstyr. Sådanne kombinationsstudier er ofte komplekse at navigere regulatorisk. COMBINE samler nationale myndigheder for at sikre, at forskere modtager sammenhængende og ikke-modstridende vejledning. Dette skaber en mere strømlinet vej for komplekse og innovative forsøg i hele Europa.
Clinical Trials Information System (CTIS)
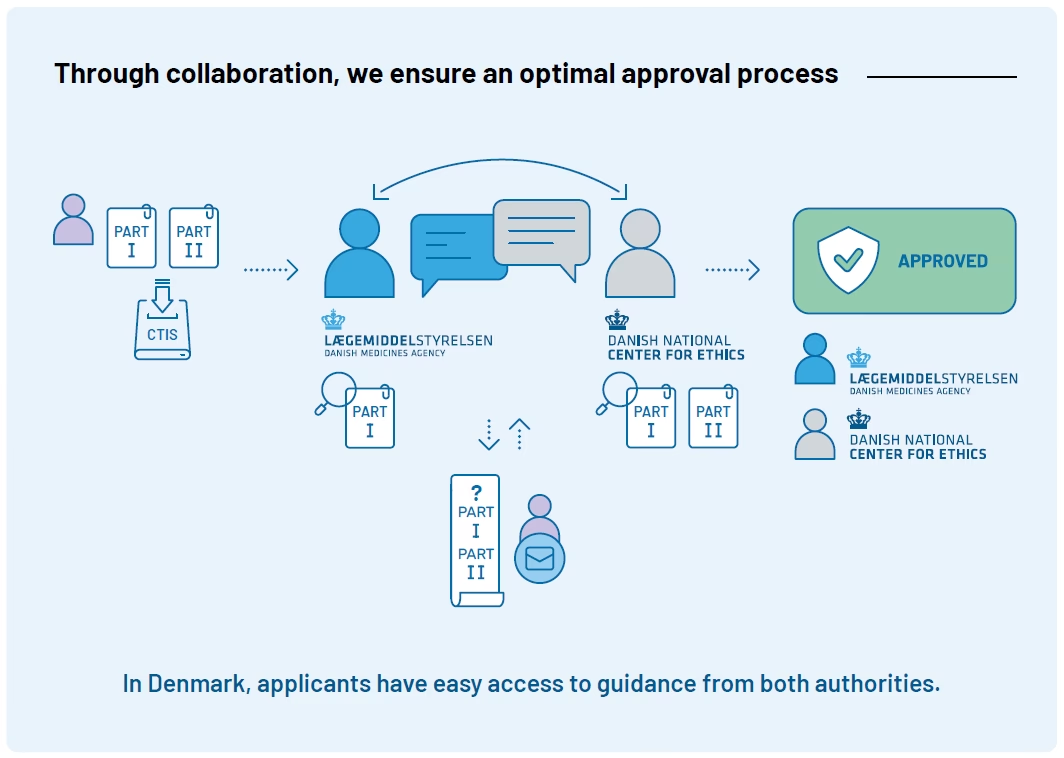
Danmark var et af de første EU-lande til fuldt ud at implementere CTIS, den nye europæiske platform til håndtering af ansøgninger om kliniske forsøg. Systemet skaber gennemsigtighed, harmonisering og lettere adgang til information om forsøg på tværs af medlemslandene. En effektiv og digitaliseret ansøgningsproces er en fundamental forudsætning for at kunne gennemføre moderne forsøg som DCTs smidigt i hele EU.
Ofte Stillede Spørgsmål (FAQ)
Hvad er den største fordel ved decentraliserede forsøg for patienter?
Den største fordel er en markant reduceret byrde. Patienter sparer tid og penge på transport, tager mindre fri fra arbejde og kan deltage i forskning fra deres eget hjem. Dette gør det muligt for flere mennesker, herunder dem med mobilitetsproblemer eller dem, der bor langt fra hospitaler, at bidrage til medicinsk udvikling.
Er data fra decentraliserede forsøg lige så sikre og pålidelige?
Ja. Lægemiddelstyrelsen og andre regulatoriske myndigheder stiller strenge krav til datakvalitet og -sikkerhed, uanset hvordan data indsamles. De digitale platforme, der anvendes, skal valideres for at sikre, at data er nøjagtige, pålidelige og beskyttede mod uautoriseret adgang. Patientsikkerheden er altid den højeste prioritet.
Hvordan sikrer Lægemiddelstyrelsen, at patienternes data beskyttes?
Al databehandling i kliniske forsøg skal overholde den generelle forordning om databeskyttelse (GDPR). Lægemiddelstyrelsen sikrer gennem vejledning og tilsyn, at sponsorer implementerer robuste tekniske og organisatoriske foranstaltninger for at beskytte personoplysninger. Gennemsigtighed over for deltagerne om, hvordan deres data bruges, er ligeledes et centralt krav.
Kan alle kliniske forsøg blive decentraliserede?
Ikke nødvendigvis. Nogle forsøg kræver komplekse procedurer, avanceret billeddiagnostik eller tæt overvågning, som kun kan udføres på et hospital. Fremtiden ligger sandsynligvis i hybride modeller, hvor man kombinerer elementer fra både traditionelle og decentraliserede forsøg for at skabe det mest hensigtsmæssige design for det specifikke studie og den pågældende patientgruppe.
Samlet set er Lægemiddelstyrelsens proaktive tilgang til decentraliserede kliniske forsøg et klart signal om, at Danmark er klar til at omfavne fremtidens forskning. Ved at kombinere en innovationsvenlig regulering, en unik datainfrastruktur og et stærkt internationalt engagement er Danmark godt på vej til at cementere sin position som et førende land inden for life science – til gavn for patienter både nationalt og globalt.
Hvis du vil læse andre artikler, der ligner Decentraliserede Forsøg: DKMA's Nye Vej, kan du besøge kategorien Sundhed.
