11/05/2001
Tuberkulose (TB), forårsaget af bakterien Mycobacterium tuberculosis (Mtb), er fortsat en af de mest dødelige infektionssygdomme i verden. I århundreder har denne mikroskopiske organisme perfektioneret sin overlevelsesstrategi, ikke ved at bruge traditionelle våben som toksiner eller kapsler, men ved at udvikle en sofistikeret evne til at manipulere selve de celler, der er designet til at ødelægge den. Kernen i denne strategi er et lille, men utroligt potent protein kendt som ESAT-6. Dette molekyle er nøglen til Mtb's succes som en af menneskehedens mest vedholdende patogener. Ved at forstå ESAT-6's rolle kan vi ikke kun afdække bakteriens evolutionære rejse, men også finde nye veje til at diagnosticere, behandle og i sidste ende udrydde tuberkulose.
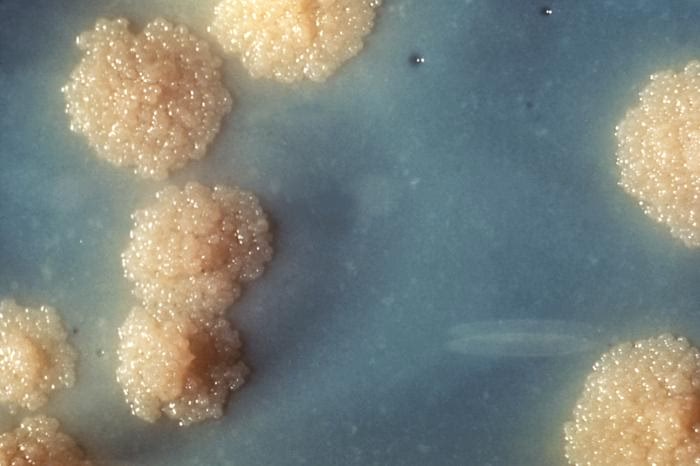
Mtb's Skjulte Våben: Virulensfaktoren ESAT-6
I modsætning til mange andre bakterier, der invaderer kroppen med et arsenal af aggressive virulensfaktorer, har Mtb valgt en mere snigende tilgang. Dens primære våben er evnen til at leve og formere sig inde i værtens immunceller, specifikt makrofager. Makrofager er kroppens 'skraldemænd', hvis opgave er at opsluge og nedbryde fremmede partikler og patogener. Mtb lader sig villigt opsluge, men i stedet for at blive ødelagt, omdanner den makrofagen til et beskyttet levested og en transportmekanisme.
Denne kapring er i høj grad orkestreret af ESAT-6. ESAT-6 (Early Secreted Antigenic Target of 6 kDa) er et protein, som bakterien aktivt udskiller ved hjælp af et specialiseret sekretionssystem kaldet ESX-1. Man kan forestille sig ESX-1 som en molekylær sprøjte, som Mtb bruger til at injicere ESAT-6 og andre proteiner direkte fra sin egen krop og ud i makrofagens indre. Den genetiske kode for dette system findes i en region af bakteriens DNA kendt som 'Region of Difference 1' (RD1). Denne region er afgørende for Mtb's evne til at forårsage sygdom. Faktisk er fraværet af RD1-regionen den primære årsag til, at BCG-vaccinen (Bacille Calmette-Guérin), som er en svækket version af den beslægtede kvægtuberkulosebakterie, ikke er virulent. Den kan ikke producere og udskille ESAT-6, og mister dermed sin evne til at manipulere værtscellen effektivt.
Mængden af udskilt ESAT-6 styres af et andet komplekst system i bakterien, PhoPR-systemet. Variationer i dette system forklarer, hvorfor nogle Mtb-stammer er mere aggressive og smitsomme end andre. Evolutionært set har Mtb bevaret og finjusteret dette system for at maksimere sin overlevelse og spredningsevne.
Infektionens Faser: ESAT-6's Rolle Trin for Trin
En Mtb-infektion er en lang og kompleks proces, der kan opdeles i tre hovedfaser: den tidlige infektion, latensperioden og progressionen til aktiv sygdom. ESAT-6 spiller en afgørende, men forskelligartet rolle i hver af disse faser.
Den Tidlige Fase: Invasion og Etablering
Når en person indånder Mtb-holdige dråber, rejser bakterierne ned i lungernes mindste luftrum, alveolerne, hvor de mødes af alveolære makrofager. Efter at være blevet opslugt, befinder Mtb sig inde i en lille blære kaldet et fagosom. Normalt ville fagosomet smelte sammen med et lysosom, en anden blære fyldt med nedbrydende enzymer, hvilket ville dræbe bakterien. Her udfører ESAT-6 sin første kritiske handling: det perforerer eller ødelægger fagosomets membran. Dette giver bakterien og dens molekyler adgang til makrofagens cytoplasma, cellens indre 'gelé'.
Denne flugt fra fagosomet har to vigtige konsekvenser. For det første undgår bakterien at blive ødelagt. For det andet bliver dens tilstedeværelse i cytoplasmaet opdaget af værtscellens indre alarmsystemer, såsom NLRP3-inflammasomet. Dette udløser en inflammatorisk reaktion og produktion af signalstoffer som IL-1β. Paradoksalt nok udnytter Mtb denne inflammation til sin egen fordel. Inflammationen tiltrækker flere immunceller, herunder flere makrofager, til infektionsstedet. Mtb kan derefter inficere disse nye celler, hvilket giver den mulighed for at udvide sin population og etablere et fodfæste dybt inde i lungevævet.
Latensperioden: En Langvarig Våbenhvile
Efter den indledende fase reagerer kroppens adaptive immunsystem, især T-celler. Dette fører til dannelsen af en strukturel enhed kaldet et granulom. Et granulom er en organiseret samling af immunceller, der danner en mur omkring de inficerede makrofager. Formålet er at inddæmme bakterierne og forhindre dem i at sprede sig. For mange mennesker (omkring en fjerdedel af verdens befolkning) fører dette til en tilstand af latent tuberkulose. Personen er smittet, men ikke syg, og kan ikke smitte andre.
ESAT-6 er også aktiv under denne fase. Det hjælper med at modulere immunresponset inde i granulomet. For eksempel kan det forsinke ankomsten af effektive T-celler og forstyrre antigenpræsentationen, hvilket gør det sværere for immunsystemet at genkende og eliminere inficerede celler. Dette skaber en hårfin balance, en slags våbenhvile, hvor hverken værten eller bakterien kan vinde. Denne tilstand kan vare i årtier og sikrer Mtb's langsigtede overlevelse i værten.
Progression til Aktiv Sygdom: Angreb og Transmission
Hvis en persons immunsystem svækkes (på grund af alder, underernæring, HIV-infektion eller andre sygdomme), kan balancen tippe til bakteriens fordel. Mtb begynder at formere sig hurtigt, og ESAT-6 skifter strategi fra stealth til fuldt angreb. Det fremkalder en type celledød kaldet nekrose i de stærkt inficerede makrofager. I modsætning til den kontrollerede, 'rene' celledød (apoptose), er nekrose en kaotisk proces, der frigiver store mængder bakterier og pro-inflammatoriske molekyler.
Dette fører til, at granulomets struktur bryder sammen. Det centrale område bliver til en osteagtig, flydende masse (kaseøs nekrose), som er et ideelt miljø for bakteriens vækst. Den intense inflammation ødelægger lungevævet og skaber hulrum (kaverner). Når disse hulrum får forbindelse til luftvejene, kan den smittede person hoste millioner af bakterier op, som derefter kan smitte nye værter. ESAT-6 er således ikke kun afgørende for at etablere infektionen, men også for det sidste, afgørende skridt: at sikre sin egen transmission og evolutionære overlevelse.
Evolutionær Forskel: Hvorfor Nogle Mykobakterier er Farligere end Andre
Ved at sammenligne genomerne af forskellige mykobakterier kan vi se evolutionen i aktion. Den centrale rolle, som RD1-regionen og ESAT-6 spiller, bliver tydelig, når man sammenligner den humane Mtb med andre medlemmer af Mycobacterium tuberculosis-komplekset.
| Mykobakterie | Primær Vært | RD1-region (ESAT-6) | Virulens hos Mennesker |
|---|---|---|---|
| Mycobacterium tuberculosis | Menneske | Intakt | Høj |
| Mycobacterium bovis | Kvæg | Intakt, men med mutationer i reguleringssystemet (PhoPR) | Moderat (forårsager zoonotisk TB) |
| BCG Vaccine | Laboratoriekultur (oprindeligt fra M. bovis) | Slettet (manglende) | Meget lav (svækket) |
| Mycobacterium microti | Gnavere | Slettet (manglende) | Meget lav |
Tabellen viser tydeligt, at evnen til at producere og effektivt udskille ESAT-6 er direkte korreleret med bakteriens evne til at forårsage alvorlig sygdom hos mennesker. Evolutionært har Mtb bevaret dette system, mens arter, der har tilpasset sig andre værter eller er blevet svækket i laboratoriet, har mistet dele af det.
Fra Fjende til Ven: ESAT-6 i Diagnostik og Vacciner
Selvom ESAT-6 er en potent virulensfaktor, er det også bakteriens akilleshæl. Fordi kroppen lancerer et stærkt immunrespons mod dette fremmede protein, kan vi udnytte det til medicinske formål.
Diagnostik
En af de største udfordringer ved TB-kontrol er at diagnosticere latent infektion. Her har ESAT-6 revolutioneret feltet. Moderne blodprøver, kendt som IGRA-tests (Interferon-Gamma Release Assays), er baseret på dette princip. En blodprøve fra patienten blandes med ESAT-6-antigener. Hvis patientens T-celler tidligere har mødt Mtb, vil de genkende ESAT-6 og reagere ved at frigive signalstoffet interferon-gamma. Måling af dette stof kan derfor bekræfte en infektion. En stor fordel ved IGRA-tests er, at de kan skelne mellem en ægte Mtb-infektion og en tidligere BCG-vaccination, da BCG-bakterien som nævnt ikke producerer ESAT-6.
Vacciner
Den nuværende BCG-vaccine giver en vis beskyttelse til børn, men er langt fra perfekt, især hos voksne. Forskere arbejder intensivt på at udvikle nye og bedre vacciner, og mange af disse har ESAT-6 i fokus. Strategierne omfatter:
- Subunit-vacciner: Disse vacciner indeholder kun udvalgte dele af patogenet, f.eks. ESAT-6-proteinet, kombineret med et adjuvans (et stof, der booster immunresponset). Målet er at træne immunsystemet til at genkende denne nøglekomponent uden at udsætte kroppen for hele bakterien.
- Nye levende svækkede vacciner: En lovende kandidat, MTBVAC, er baseret på en genetisk modificeret Mtb-stamme. Forskerne har slettet to gener, herunder et, der er nødvendigt for at udskille ESAT-6. Bakterien producerer altså proteinet (så immunsystemet kan 'se' det), men kan ikke frigive det (så det ikke kan forårsage skade). Dette forventes at give et bredere og mere robust immunrespons end BCG.
Ofte Stillede Spørgsmål (FAQ)
Hvad er tuberkulose?
Tuberkulose er en infektionssygdom forårsaget af bakterien Mycobacterium tuberculosis. Den rammer oftest lungerne (lungetuberkulose), men kan også påvirke andre dele af kroppen. Den spredes gennem luften, når en person med aktiv lungetuberkulose hoster, nyser eller taler.
Hvad gør ESAT-6 så specielt?
ESAT-6 er et nøgleprotein, som tuberkulosebakterien bruger til at undslippe ødelæggelse inde i immunceller (makrofager). Det giver bakterien mulighed for at etablere en infektion, overleve i årtier i en latent tilstand og til sidst forårsage vævsskade, der muliggør smitte til nye værter.
Hvorfor er den nuværende BCG-vaccine ikke fuldt ud effektiv?
BCG-vaccinen er baseret på en svækket bakterie, der mangler den genetiske region (RD1), som koder for ESAT-6 og dets sekretionssystem. Selvom vaccinen kan stimulere en del af immunsystemet, mangler den vigtige antigener som ESAT-6, hvilket menes at begrænse dens langsigtede effektivitet, især mod lungetuberkulose hos voksne.
Hvordan kan man teste for latent tuberkulose?
Latent tuberkulose, hvor personen er smittet men ikke syg, kan påvises med en IGRA-blodprøve eller en tuberkulinhudtest (Mantoux-test). IGRA-testen er ofte foretrukket, da den er mere specifik og ikke påvirkes af en tidligere BCG-vaccination.
Studiet af Mycobacterium tuberculosis og dets virulensfaktor ESAT-6 er et fascinerende indblik i den evolutionære kamp mellem patogen og vært. ESAT-6 er symbolet på bakteriens succes: et enkelt molekyle, der kan afvæbne vores forsvar, kapre vores celler og sikre sin egen overlevelse. Men ved at afkode dets funktioner har videnskaben vendt bakteriens stærkeste våben mod den selv. Denne viden er nu grundlaget for udviklingen af de diagnostiske værktøjer og vacciner, der kan give os overtaget i den årtusindgamle kamp mod tuberkulose.
Hvis du vil læse andre artikler, der ligner Mycobacterium tuberculosis: En Patogens Evolution, kan du besøge kategorien Sundhed.
