22/08/1999
MYC-proto-onkogenerne udgør en familie af transkriptionsfaktorer, der er blandt de hyppigst aktiverede onkoproteiner i menneskelige kræftsygdomme. Faktisk forekommer afvigelser i MYC eller opregulering af MYC-relaterede signalveje i langt de fleste kræftformer. MYC-proteiner fungerer som overordnede regulatorer af cellulære programmer, hvilket betyder, at kræftformer med MYC-aktivering udviser mange af de kendetegn, der er nødvendige for autonom neoplastisk vækst. At forstå dette komplekse gen er afgørende for at udvikle fremtidens kræftbehandlinger.
Hvad er MYC-onkogenfamilien?
MYC er ikke blot ét enkelt gen, men en familie af beslægtede gener, der omfatter c-MYC (ofte blot kaldet MYC), MYCL (L-MYC) og MYCN (N-MYC). Oprindeligt troede man, at deres roller var strengt opdelte: MYC var involveret i de fleste kræftformer, L-MYC i småcellet lungekræft og N-MYC i neuroblastom. Nyere genomsekventeringsstudier har dog afsløret et meget bredere billede, hvor både N-MYC og L-MYC spiller en rolle i mange andre kræfttyper. Tilsammen betyder det, at de fleste menneskelige kræftformer har en genetisk aktivering af et medlem af MYC-familien.
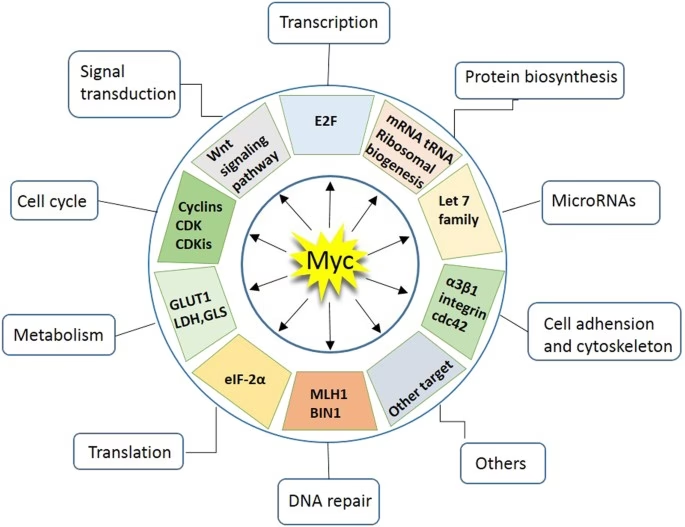
Disse gener koder for proteiner, der fungerer som en transkriptionsfaktor. Det betyder, at de binder sig til DNA og kontrollerer udtrykket (tænd/sluk) af tusindvis af andre gener. Ved at gøre dette fungerer MYC som en slags hovedafbryder for en lang række fundamentale cellulære processer, herunder:
- Cellevækst og deling (proliferation): MYC driver celler til at gå igennem cellecyklussen hurtigere.
- Metabolisme: Det omprogrammerer cellens stofskifte for at understøtte hurtig vækst.
- Celleoverlevelse: Det kan forhindre celler i at undergå programmeret celledød (apoptose).
- Genomisk ustabilitet: Det kan bidrage til en øget mutationsrate i kræftceller.
Hvordan aktiveres MYC i kræftceller?
Normalt er MYC-aktiviteten stramt kontrolleret i sunde celler. I kræftceller er denne kontrol brudt sammen, hvilket fører til vedvarende og ukontrolleret MYC-aktivitet. Dette kan ske gennem flere mekanismer:
Genetiske ændringer
De mest direkte måder at aktivere MYC på involverer ændringer i selve DNA'et.
- Genamplifikation: Kræftcellen skaber mange ekstra kopier af MYC-genet. Med flere kopier produceres der meget mere MYC-protein. Dette ses i op til 28% af alle tumorer på tværs af forskellige kræfttyper.
- Kromosomale translokationer: En del af et kromosom, der indeholder MYC-genet, brækker af og sætter sig fast et andet sted i genomet. Dette placerer ofte MYC under kontrol af en meget stærk 'promotor' (et tænd/sluk-signal), hvilket fører til konstant høj produktion af MYC-protein. Dette er klassisk i B-celle lymfomer.
Regulatoriske og post-translationelle mekanismer
Selv uden ændringer i selve genet kan MYC-aktiviteten øges:
- Opstrøms signalveje: Andre kræftfremkaldende signalveje (som WNT eller RAS) kan sende signaler, der øger produktionen af MYC.
- Øget proteinstabilitet: MYC-proteinet har normalt en meget kort levetid i cellen, før det nedbrydes. I kræftceller kan mekanismer, der normalt nedbryder MYC, være deaktiveret. For eksempel kan ændringer i fosforyleringsmønstre på proteinet gøre det mere stabilt og aktivt i længere tid.
Onkogen afhængighed: Kræftens akilleshæl
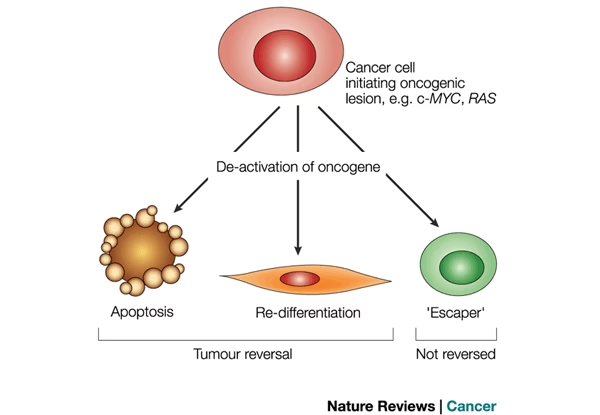
En af de mest spændende opdagelser inden for MYC-forskning er fænomenet onkogener afhængighed. Selvom MYC driver kræftens vækst, gør det også tumoren ekstremt sårbar. Prækliniske studier i musemodeller har vist noget bemærkelsesværdigt: Når MYC-aktiviteten slukkes i en etableret tumor, holder tumoren ikke bare op med at vokse – den kollapser og forsvinder ofte helt. Cellerne holder op med at dele sig, gennemgår aldring (senescens) eller dør simpelthen.
Dette fænomen tyder på, at selvom tumoren har mange andre mutationer, er den blevet så afhængig af den konstante stimulation fra MYC, at den ikke kan overleve uden den. Dette giver et enormt terapeutisk potentiale: Hvis man kan udvikle en medicin, der specifikt blokerer MYC, kan man potentielt få tumorer til at regrediere dramatisk.
MYC og immunsystemet: En mester i undvigelse
Kræft er ikke kun en kamp mellem sunde og syge celler; det er også en kamp mellem tumoren og kroppens immunsystem. MYC spiller en afgørende rolle i at hjælpe kræftceller med at undvige og undertrykke immunforsvaret. Dette sker gennem flere smarte strategier:
Regulering af immun-checkpoints
Immunsystemet har bremser, kaldet immun-checkpoints, for at forhindre det i at angribe kroppens egne celler. Kræftceller udnytter disse bremser.
- PD-L1: MYC kan direkte øge udtrykket af et protein kaldet PD-L1 på kræftcellens overflade. Når PD-L1 binder til sin receptor (PD-1) på T-celler (immunceller), sendes et signal til T-cellen om at lade kræftcellen være i fred.
- CD47: MYC øger også udtrykket af CD47, som fungerer som et 'spis mig ikke'-signal til andre immunceller som makrofager.
Gør sig selv usynlig
For at immunsystemet kan genkende en kræftcelle, skal cellen præsentere små stykker af sine proteiner (antigener) på overfladen via et molekyle kaldet MHC I. MYC har vist sig at undertrykke udtrykket af MHC I, hvilket gør kræftcellen mere eller mindre usynlig for T-cellerne.
Metabolisk krigsførelse
MYC-drevne kræftceller har et umætteligt behov for næringsstoffer som glukose og glutamin for at vokse. De omprogrammerer deres stofskifte (kendt som Warburg-effekten) til at forbruge disse ressourcer i et ekstremt tempo. Dette skaber et næringsfattigt mikromiljø omkring tumoren, hvor immuncellerne bogstaveligt talt sulter og ikke har energi til at udføre deres angreb.
Sammenligning af høj og lav MYC-aktivitet
For at illustrere MYC's indflydelse kan vi opstille en tabel, der sammenligner effekterne af høj MYC-aktivitet med effekterne af at inaktivere MYC.
| Egenskab | Høj MYC-aktivitet | MYC-inaktivering |
|---|---|---|
| Cellevækst | Hurtig og ukontrolleret | Stop af vækst, aldring eller celledød |
| Immunundvigelse | Stærk (højt PD-L1 & CD47, lavt MHC I) | Reduceret (immunsystemet genaktiveres) |
| Metabolisme | Højt forbrug af glukose (glykolyse) | Normaliseret metabolisme |
| Tumorvækst | Aggressiv progression og metastase | Tumorregression |
Fremtidens behandlinger: At målrette MYC
På trods af at være et af de vigtigste kræftgener, har MYC vist sig at være notorisk svært at ramme med medicin. Der er dog ingen godkendte lægemidler, der direkte hæmmer MYC, men forskningen er i rivende udvikling, og flere strategier forfølges:
- Direkte hæmmere: Forskere arbejder på at udvikle små molekyler, der kan binde direkte til MYC-proteinet og forhindre det i at fungere.
- Indirekte strategier: En anden tilgang er at ramme de proteiner, som MYC er afhængig af for at være stabil eller aktiv. For eksempel er hæmmere af BET-bromodomæner (som JQ1) under udvikling, da de kan reducere MYC-udtrykket.
- Syntetisk letalitet: Idéen er at finde et gen, som kræftceller med høj MYC-aktivitet er afhængige af, men som normale celler kan undvære. Ved at ramme dette 'partner-gen' kan man selektivt dræbe kræftcellerne.
- Kombinationsbehandlinger: En lovende strategi er at kombinere MYC-rettede terapier med immunterapi. Ved at hæmme MYC kan man gøre 'kolde' tumorer (som immunsystemet ignorerer) 'varme' og dermed modtagelige for immunterapi som PD-1-hæmmere.
Fremtiden ligger sandsynligvis i at bruge MYC som en biomarkør. Ved at analysere en patients tumor for MYC-aktivering (f.eks. genamplifikation eller et højt udtryk) kan læger stratificere patienter og vælge den mest effektive behandling. En patient med en MYC-høj tumor kan have gavn af en direkte MYC-hæmmer, mens en anden kan respondere bedre på en kombination af immunterapi og metabolisk terapi.
Ofte Stillede Spørgsmål om MYC og Kræft
Er MYC-genet altid skadeligt?
Nej, MYC er et essentielt gen for normal udvikling og cellevækst, f.eks. under sårheling eller i immunsystemet. Problemet opstår, når genet bliver permanent overaktivt og dets funktion løber løbsk, hvilket driver ukontrolleret celledeling og kræft.
Hvilke kræftformer er oftest forbundet med MYC?
MYC-aktivering ses i et meget bredt spektrum af kræftformer. Det er en definerende egenskab ved visse lymfomer (som Burkitts lymfom) og neuroblastom, men det er også hyppigt aktiveret i mange solide tumorer, herunder brystkræft, lungekræft, leverkræft og tyktarmskræft.
Hvorfor er det så svært at udvikle medicin mod MYC?
MYC-proteinet har en uordnet struktur uden de klassiske 'lommer', som lægemidler normalt binder til. Desuden er dets funktion så central for både normale og syge celler, at det er en udfordring at hæmme det i kræftceller uden at forårsage alvorlige bivirkninger i raske væv.
Kan man blive testet for MYC-aktivering?
Ja, i klinisk praksis og forskning kan man analysere tumorvæv (en biopsi) for tegn på MYC-aktivering. Dette kan omfatte test for genamplifikation (f.eks. via FISH) eller måling af protein- eller mRNA-niveauer. I fremtiden vil sådanne test blive afgørende for at skræddersy behandlingen til den enkelte patient.
Hvis du vil læse andre artikler, der ligner MYC-onkogenet: Kræftens centrale drivkraft, kan du besøge kategorien Kræft.