08/09/2009
Forestil dig en fremtid, hvor uhelbredelige sygdomme kan behandles ved at erstatte kroppens beskadigede celler med nye, sunde celler, der er dyrket i et laboratorium. Dette er ikke længere ren science fiction, men et aktivt forskningsområde takket være potentialet i pluripotente stamceller. Disse bemærkelsesværdige celler har evnen til at udvikle sig til næsten enhver celletype i den menneskelige krop, hvilket åbner døren for revolutionerende behandlinger inden for regenerativ medicin. Gennem mere end to årtiers intens forskning er vi nu ved at se de første kliniske forsøg, der bringer disse terapier fra laboratoriet til patienterne. Men vejen er kompleks og fyldt med udfordringer, fra storskalaproduktion til at sikre patienternes sikkerhed.
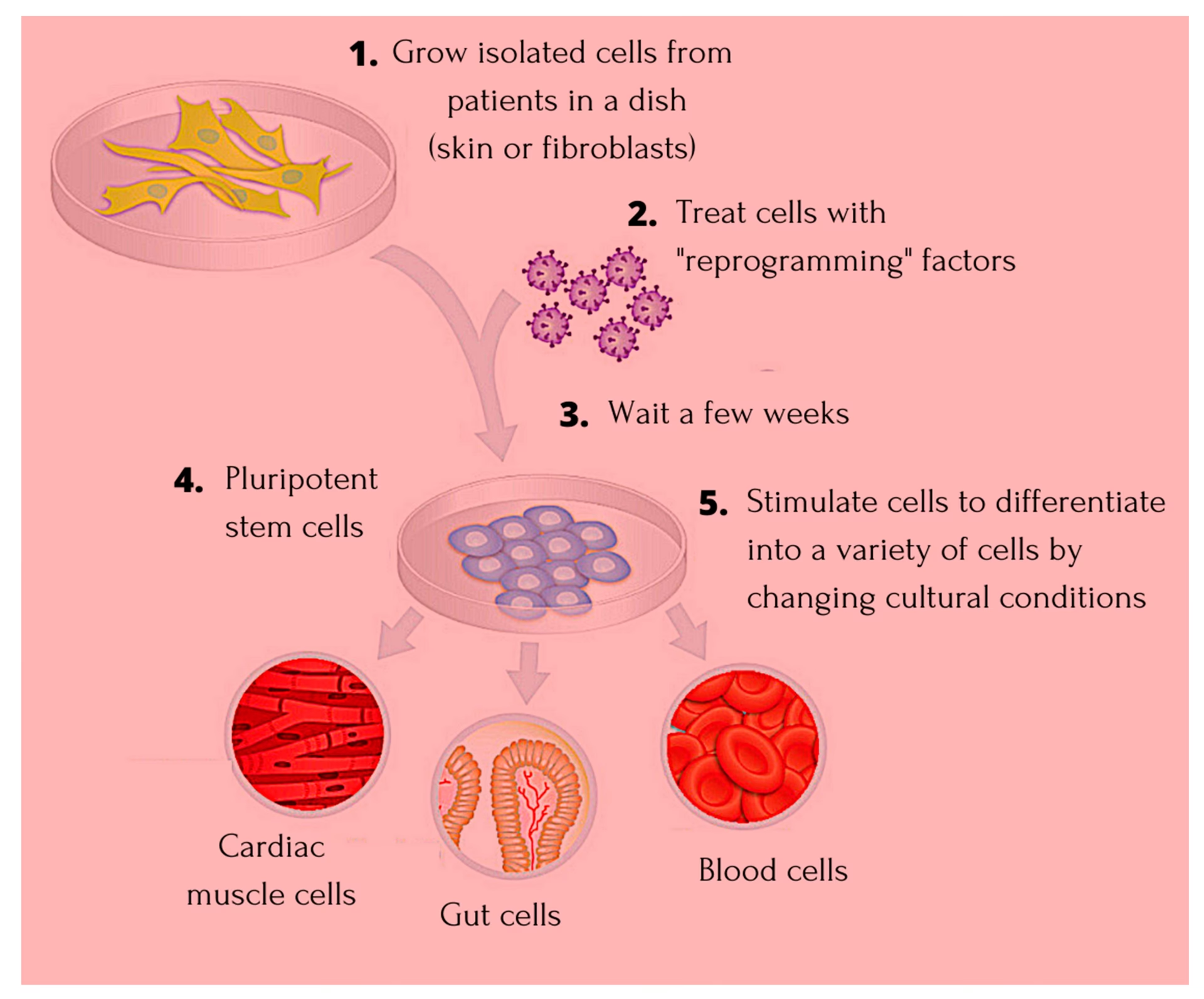
Hvad er Pluripotente Stamceller?
For at forstå potentialet er det vigtigt at vide, hvad pluripotente stamceller er. Ordet 'pluripotent' betyder 'i stand til mange ting'. Disse celler er uspecialiserede og har to unikke egenskaber:
- Selvfornyelse: De kan dele sig og skabe flere stamceller over en lang periode.
- Differentiering: De kan blive instrueret til at udvikle sig til specialiserede celler, såsom nerveceller, hjerteceller, insulinproducerende celler eller nethindeceller.
Der findes primært to typer af pluripotente stamceller, som er centrale i forskningen:
- Embryonale Stamceller (ESC'er): Disse stammer fra tidlige stadier af et embryo og er naturligt pluripotente. Deres brug er forbundet med etiske debatter, men de har været afgørende for at forstå de grundlæggende principper for celledifferentiering.
- Inducerede Pluripotente Stamceller (iPS-celler): Dette er en teknologisk landvinding, hvor forskere kan tage en specialiseret voksen celle, f.eks. en hudcelle eller blodcelle, og omprogrammere den genetisk tilbage til en pluripotent tilstand. Disse iPS-celler opfører sig meget ligesom embryonale stamceller. Fordelen er enorm: Man kan potentielt skabe patient-specifikke stamceller, hvilket minimerer risikoen for immunafstødning og omgår de etiske problemer forbundet med ESC'er. Omprogrammeringen sker typisk ved midlertidigt at introducere fire specifikke gener (OCT4, SOX2, KLF4 og c-MYC) i de voksne celler.
Udfordringen: Fra Laboratoriebænk til Fabriksproduktion
Selvom videnskaben bag at skabe og differentiere stamceller er kommet langt, er en af de største forhindringer for udbredt klinisk brug produktionen. At fremstille nok celler til et enkelt forsøg i en petriskål er én ting; at producere milliarder af celler af høj, ensartet kvalitet til behandling af tusindvis af patienter er en helt anden udfordring. Denne proces skal overholde strenge retningslinjer kendt som Good Manufacturing Practice (GMP), som sikrer, at celleprodukterne er sikre, rene og effektive.
International Society for Cell and Gene Therapy (ISCT) har fremhævet, at overgangen til storskalaproduktion kræver betydelige investeringer i automatisering og ny teknologi. Manuelle processer, der fungerer fint i et forskningslaboratorium, er ikke reproducerbare eller skalerbare nok til kommerciel produktion. Derfor arbejder udviklere med at integrere automatiserede systemer til både dyrkning (ekspansion) og specialisering (differentiering) af cellerne. Dette inkluderer bioreaktorer, der kan dyrke celler i store mængder under kontrollerede forhold, og avancerede analysesystemer, der løbende overvåger cellernes kvalitet.
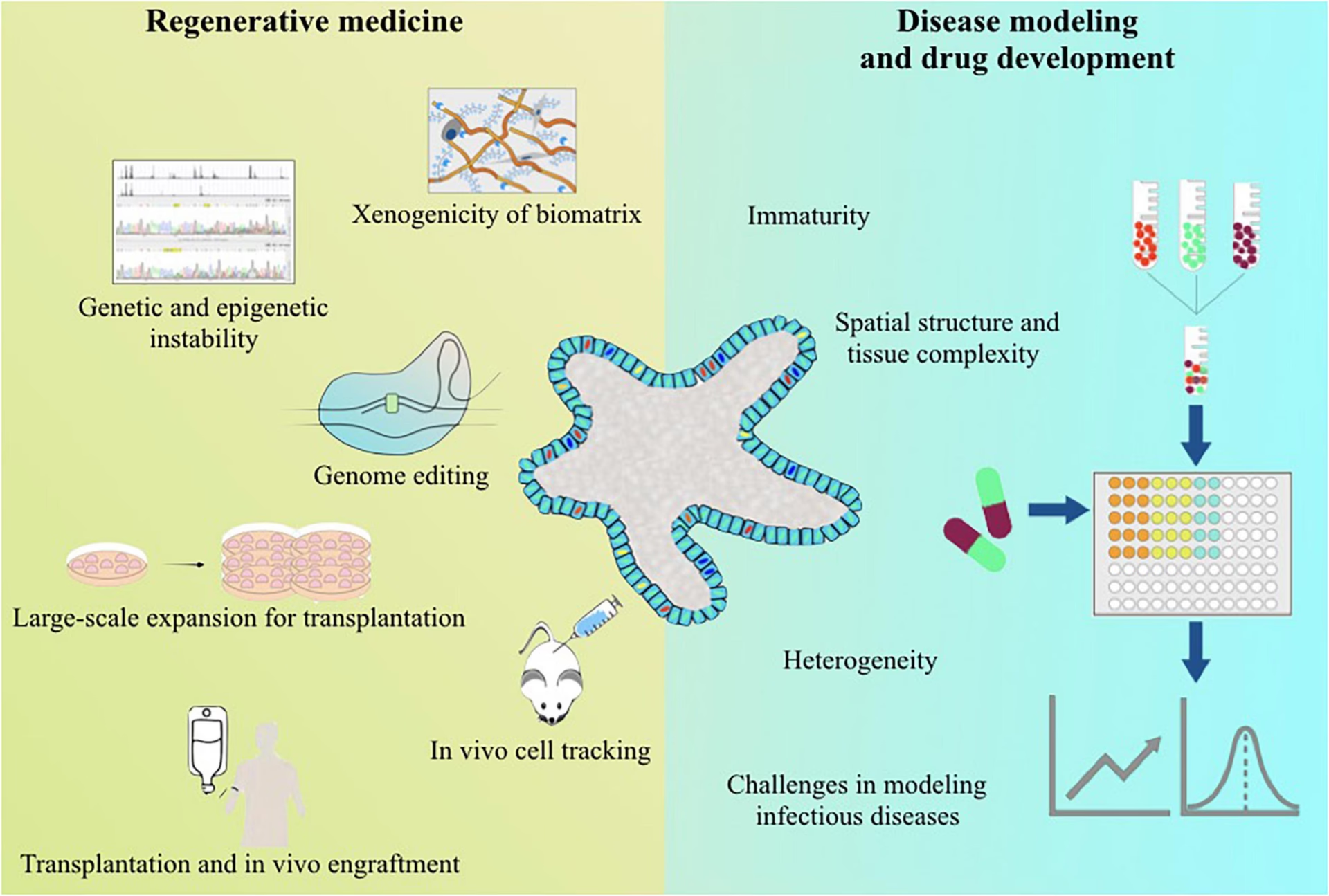
Potentielle Terapier: Hvilke Sygdomme Kan Behandles?
Forskningen i stamcelleterapi spænder bredt og sigter mod at behandle sygdomme, der er kendetegnet ved tab eller beskadigelse af specifikke celletyper. Nedenstående tabel giver et overblik over nogle af de mest lovende områder.
Sammenligning af Potentielle Stamcellebaserede Terapier
| Sygdom | Målcelle | Terapeutisk Mål |
|---|---|---|
| Parkinsons Sygdom | Dopaminproducerende neuroner | Erstatte de mistede neuroner i hjernen for at gendanne motorisk kontrol. |
| Aldersrelateret Makuladegeneration (AMD) | Nethindens pigmentepitelceller (RPE) | Erstatte beskadigede RPE-celler for at bremse synstab og potentielt forbedre synet. |
| Hjertesvigt efter blodprop | Hjertemuskelceller (kardiomyocytter) | Reparere arvæv i hjertet og forbedre pumpefunktionen. |
| Type 1 Diabetes | Insulinproducerende betaceller | Transplantere nye betaceller for at genoprette kroppens evne til at regulere blodsukkeret. |
| Rygmarvsskader | Oligodendrocytter og neuroner | Fremme reparation af nervevæv og genoprette tabt funktion. |
Teknologiske Gennembrud Driver Udviklingen
To teknologier har i særlig grad accelereret fremskridtene inden for stamcelleforskning: genredigering med CRISPR-Cas9 og udviklingen af 3D-organoider.
CRISPR-Cas9: Genetisk Reparation
CRISPR-Cas9 er en slags 'gen-saks', der gør det muligt for forskere at klippe og klistre i DNA med utrolig præcision. I kombination med iPS-celleteknologi åbner dette for fantastiske muligheder:
- Korrektion af arvelige sygdomme: For en patient med en genetisk sygdom som Duchennes muskeldystrofi kan man tage patientens egne hudceller, omdanne dem til iPS-celler, reparere den genetiske fejl med CRISPR og derefter differentiere de 'raske' celler til muskelceller, som kan transplanteres tilbage til patienten.
- Skabelse af 'universelle' donorceller: En stor udfordring er immunafstødning. Selvom man bruger patientens egne celler, kan der opstå immunreaktioner. For at skabe celler, der kan gives til alle patienter, bruger forskere CRISPR til at fjerne de HLA-molekyler på celleoverfladen, som immunforsvaret genkender som fremmede. Disse 'hypoimmune' celler kan potentielt blive en universel kilde til celleterapi uden behov for immundæmpende medicin.
3D-Organoider: Mini-organer i en Skål
Ved at dyrke stamceller i et tredimensionelt miljø kan forskere få dem til at selvorganisere sig til små, simple versioner af organer, kaldet organoider. Disse 'mini-hjerner', 'mini-levere' eller 'mini-tarme' er uvurderlige værktøjer. De gør det muligt at studere sygdomsudvikling på en måde, der tæt efterligner menneskelig biologi, og de kan bruges til at teste nye lægemidlers effekt og sikkerhed, før de afprøves i mennesker.

Sikkerhed Først: Risici og Etiske Overvejelser
Med stort potentiale følger også stort ansvar. Sikkerhed er den absolut højeste prioritet, når stamcelleterapier skal i klinikken. Den primære bekymring er risikoen for tumorudvikling, specifikt teratomer. Hvis ikke alle pluripotente stamceller bliver fuldt differentieret til den ønskede celletype, kan de resterende uspecialiserede celler danne tumorer efter transplantation. Derfor er strenge kvalitetskontrolprocedurer, der sikrer renheden af celleproduktet, afgørende.
En anden risiko er genetisk ustabilitet. Celler, der dyrkes i laboratoriet over længere tid, kan ophobe genetiske mutationer. Forskere skal derfor omhyggeligt overvåge cellernes genom for at sikre, at der ikke opstår skadelige ændringer.
Endelig er der de etiske retningslinjer, som løbende skal tilpasses i takt med teknologiens udvikling. Gennemsigtighed, informeret samtykke fra patienter og en ansvarlig tilgang til forskning er fundamentet for, at feltet kan udvikle sig på en måde, der gavner samfundet.

Ofte Stillede Spørgsmål (FAQ)
Er stamcelleterapi tilgængelig for patienter nu?
For de fleste sygdomme er stamcelleterapier baseret på pluripotente stamceller stadig på forsøgsstadiet i kliniske forsøg. De er endnu ikke standardbehandlinger. Den eneste veletablerede stamcelleterapi er knoglemarvstransplantation, som bruger voksne hæmatopoietiske stamceller.
Hvad er den største forskel på embryonale og inducerede pluripotente stamceller (iPS-celler)?
Den primære forskel er deres oprindelse. Embryonale stamceller (ESC'er) stammer fra et embryo, mens iPS-celler skabes ved at omprogrammere voksne celler (f.eks. hudceller). Dette betyder, at iPS-celler kan laves specifikt til en patient og undgår de etiske dilemmaer forbundet med brugen af embryoner.
Hvad er den største risiko ved iPS-celleterapi?
Den mest alvorlige risiko er dannelsen af tumorer (teratomer), hvis der er rester af uspecialiserede pluripotente celler i det transplanterede produkt. Andre risici inkluderer immunafstødning og potentielle genetiske ændringer i cellerne under dyrkning.

Kan disse celler helbrede alle sygdomme?
Nej, stamcelleterapi er ikke en mirakelkur for alt. Dets potentiale ligger primært i behandling af sygdomme forårsaget af celledød eller vævsskade, hvor funktion kan genoprettes ved at erstatte de tabte celler. Det er en del af fremtidens personaliserede medicin, men ikke en universalløsning.
Konklusion: Et Kig ind i Fremtiden
Feltet for regenerativ medicin, anført af forskningen i pluripotente stamceller, står på tærsklen til en ny æra. Vi bevæger os fra grundlæggende opdagelser mod reelle kliniske anvendelser, der har potentiale til at ændre livet for millioner af mennesker. Vejen er stadig lang og kræver løsninger på komplekse udfordringer inden for produktion, sikkerhed og regulering. Men med den fortsatte innovation inden for bioteknologi, genredigering og bioengineering er håbet om at kunne reparere og regenerere den menneskelige krop stærkere end nogensinde før.
Hvis du vil læse andre artikler, der ligner Pluripotente Stamceller: Fremtidens Medicin?, kan du besøge kategorien Sundhed.
