08/04/2017
I en verden, hvor antibiotikaresistens udgør en stadigt voksende trussel mod global sundhed, er præcise og pålidelige metoder til at teste bakteriers følsomhed over for antibiotika vigtigere end nogensinde før. En af de mest grundlæggende og anerkendte metoder inden for mikrobiologi er Kirby-Bauer-testen, også kendt som diskdiffusionsmetoden. Selvom den er blevet suppleret af mere moderne, automatiserede systemer, forbliver denne test en hjørnesten i mange laboratorier på grund af sin enkelhed, omkostningseffektivitet og pålidelighed. Denne artikel vil dykke ned i, hvad Kirby-Bauer-testen er, hvordan den udføres, og hvorfor den fortsat er et uundværligt værktøj i kampen mod infektionssygdomme.
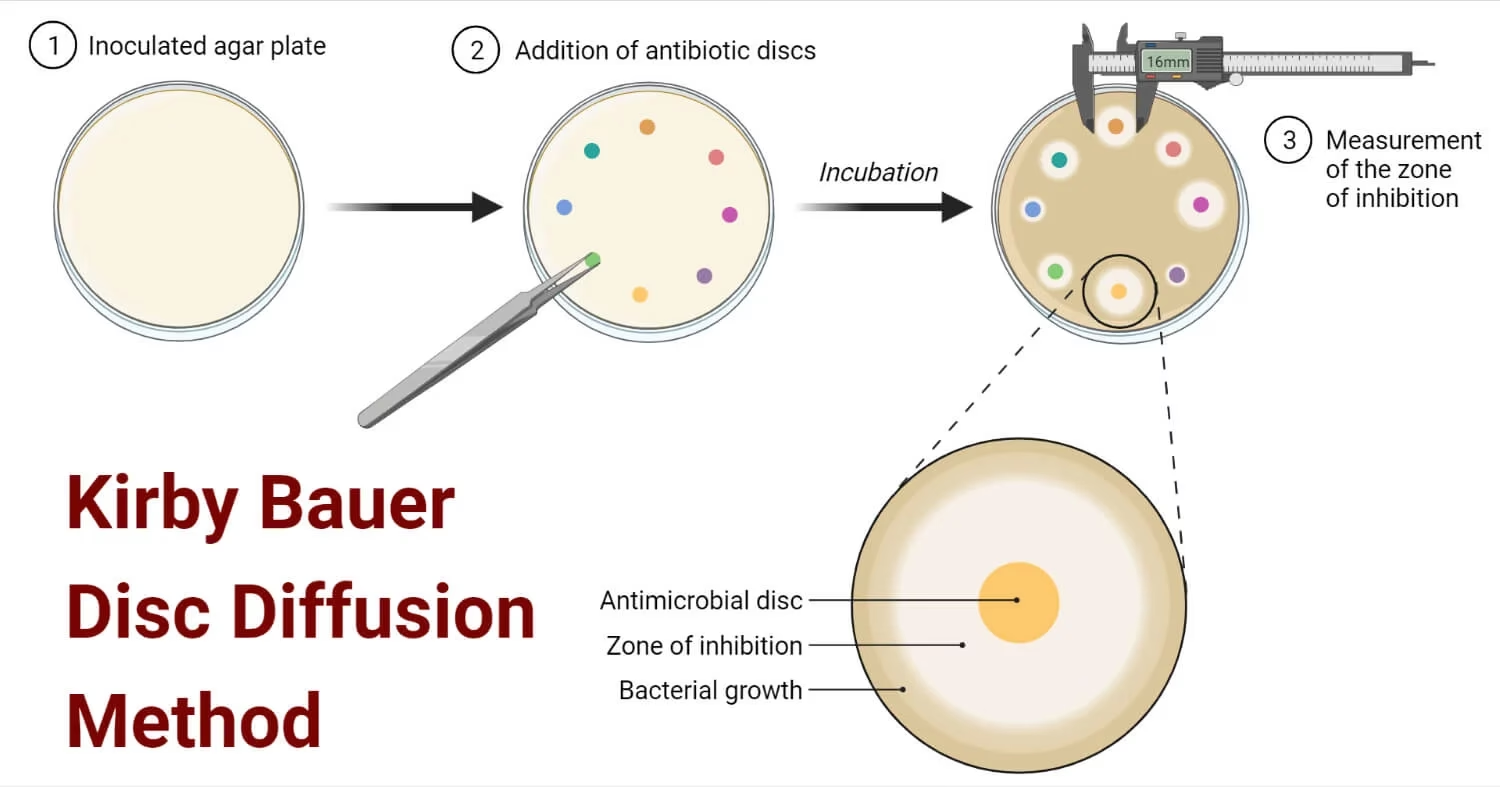
Historie og Principper bag Kirby-Bauer-testen
Konceptet med at bruge papirskiver imprægneret med antimikrobielle stoffer til at teste bakteriers følsomhed kan spores tilbage til 1940'erne. Det var dog først i 1950'erne, at metoden blev videreudviklet og raffineret af forskerne W. M. M. Kirby og A. W. Bauer. Deres arbejde førte til en standardiseret procedure, som blev officielt anerkendt og standardiseret af Verdenssundhedsorganisationen (WHO) i 1961. Denne standardisering var afgørende for at sikre, at resultaterne var sammenlignelige og reproducerbare på tværs af forskellige laboratorier verden over.
Princippet bag testen er elegant i sin enkelhed. Det bygger på diffusion. Først bliver en agarplade, typisk en Mueller-Hinton agar, jævnt podet med den bakterie, der skal testes. Derefter placeres små papirskiver (diske), som hver især er imprægneret med en kendt koncentration af et specifikt antibiotikum, på agaroverfladen. Når pladen inkuberes, sker der to ting samtidigt: bakterierne begynder at vokse og danne en tæt 'plæne' på agaren, og antibiotikummet diffunderer ud fra disken og ind i agaren. Dette skaber en koncentrationsgradient, hvor koncentrationen af antibiotikum er højest tættest på disken og falder, jo længere væk man kommer.
Hvis bakterien er følsom over for det pågældende antibiotikum, vil dens vækst blive hæmmet i et område omkring disken. Dette resulterer i en klar, cirkulær zone, hvor der ikke er nogen bakterievækst. Denne zone kaldes en hæmningszone. Størrelsen på denne zone er direkte relateret til, hvor følsom bakterien er over for antibiotikummet: en større zone indikerer større følsomhed, mens ingen eller en meget lille zone indikerer resistens.
Nødvendige Materialer og Forberedelse
For at opnå nøjagtige og pålidelige resultater med Kirby-Bauer-metoden er det afgørende at følge en standardiseret procedure og anvende de korrekte materialer. Afvigelser kan føre til fejlagtige resultater, som kan have alvorlige konsekvenser for patientbehandlingen.

Udstyr og materialer:
- Mueller-Hinton agarplader: Dette er standardmediet, da dets sammensætning er veldefineret og understøtter god vækst for de fleste patogene bakterier samt optimal diffusion af antibiotika.
- Bakteriekulturer: Rene kulturer af de bakterier, der skal testes (f.eks. Staphylococcus aureus, Escherichia coli).
- Sterile podepinde: Bruges til at pode bakterierne jævnt ud på agarpladen.
- Antibiotikadiske: Små papirskiver imprægneret med specifikke antibiotika i standardiserede koncentrationer.
- Steril pincet eller diskdispenser: Til at placere diskene på agaren.
- Inkubator: Et varmeskab, der kan holde en konstant temperatur, typisk 35-37°C.
- Lineal eller skydelære: Til præcis måling af hæmningszonernes diameter.
Forberedelse af inokulum:
Et af de mest kritiske trin er forberedelsen af bakteriesuspensionen (inokulum). Tætheden af bakterier skal være standardiseret for at sikre, at resultaterne er sammenlignelige. Dette gøres typisk ved at sammenligne suspensionens turbiditet (uklarhed) med en 0.5 McFarland standard, hvilket svarer til en bakteriekoncentration på cirka 1.5 x 10^8 CFU/ml. En for tynd suspension kan resultere i for store hæmningszoner, mens en for tæt suspension kan give for små zoner.
Udførelse af Testen: En Trin-for-Trin Guide
Selve proceduren er metodisk og kræver omhyggelighed og aseptisk teknik for at undgå forurening.
- Podning af pladen: En steril podepind dyppes i den standardiserede bakteriesuspension. Overskydende væske presses af mod indersiden af røret. Hele overfladen af Mueller-Hinton agarpladen podes jævnt ved at stryge podepinden i tre forskellige retninger, hvor pladen drejes 60-90 grader mellem hver strygning. Til sidst køres podepinden rundt langs kanten af pladen for at sikre fuld dækning.
- Tørring: Pladen får lov at tørre i 5-10 minutter, så overfladefugtigheden absorberes af agaren, før diskene påføres.
- Placering af diske: Ved hjælp af en steril pincet eller en automatisk dispenser placeres de ønskede antibiotikadiske på agaroverfladen. Det er vigtigt at sikre, at de er jævnt fordelt og ikke ligger for tæt på hinanden eller kanten af pladen.
- Sikring af kontakt: Hver disk presses forsigtigt ned med pincetten for at sikre fuld kontakt med agaroverfladen. Dette er afgørende for en korrekt diffusion af antibiotikummet.
- Inkubation: Pladerne vendes på hovedet (for at undgå kondens på låget) og inkuberes ved 35-37°C i 16-24 timer.
Aflæsning og Tolkning af Resultater
Efter inkubation undersøges pladerne for vækst og hæmningszoner. Diameteren af hver hæmningszone måles i millimeter (mm) ved hjælp af en lineal eller skydelære. Målingen foretages på bagsiden af pladen, og den skal være på tværs af zonens bredeste diameter.
Den målte diameter sammenlignes derefter med standardiserede fortolkningstabeller, som f.eks. dem udgivet af Clinical and Laboratory Standards Institute (CLSI) eller European Committee on Antimicrobial Susceptibility Testing (EUCAST). Baseret på disse tabeller klassificeres bakterien som en af tre kategorier for hvert antibiotikum:
- Følsom (S - Susceptible): En stor hæmningszone indikerer, at bakterien sandsynligvis vil blive hæmmet af den koncentration af antibiotikum, der kan opnås i kroppen ved en standarddosis. Infektionen kan forventes at respondere på behandling med dette lægemiddel.
- Intermediær (I - Intermediate): Zonen er mindre, hvilket indikerer, at antibiotikummet kan være effektivt, men kun i situationer, hvor det kan koncentreres i kroppen (f.eks. i urinen) eller ved brug af højere doser end normalt.
- Resistent (R - Resistant): En meget lille eller ingen hæmningszone betyder, at bakterien ikke hæmmes af de koncentrationer af antibiotikummet, der er opnåelige i kroppen. Lægemidlet vil sandsynligvis ikke være effektivt til behandling af infektionen.
Eksempel på Fortolkningstabel
Tabellen nedenfor viser eksempler på, hvordan zonestørrelser kan fortolkes for udvalgte antibiotika. Bemærk, at disse værdier kan variere afhængigt af bakterieart og den anvendte standard.
| Antibiotikum | Resistent (≤ mm) | Intermediær (mm) | Følsom (≥ mm) |
|---|---|---|---|
| Ampicillin (AM) | 11 | 12-13 | 14 |
| Ciprofloxacin (CIP) | 15 | 16-20 | 21 |
| Erythromycin (E) | 13 | 14-22 | 23 |
| Tetracyklin (Te) | 14 | 15-18 | 19 |
Faktorer der Påvirker Nøjagtigheden
For at opnå troværdige resultater er standardisering altafgørende. Flere faktorer kan påvirke udfaldet af en Kirby-Bauer-test, og det er vigtigt at kontrollere dem nøje:
- Inokulumtæthed: Som nævnt kan en forkert bakteriekoncentration give misvisende resultater.
- Agartykkelse: Tykkelsen på Mueller-Hinton agaren skal være ensartet (typisk 4 mm), da den påvirker den vertikale diffusion af antibiotikummet.
- Inkubationsforhold: Temperatur og tid skal være standardiseret for at sikre optimal og reproducerbar bakterievækst.
- Kvaliteten af antibiotikadiske: Diskenes styrke kan aftage over tid, især hvis de opbevares forkert. De skal opbevares koldt og tørt og må ikke anvendes efter udløbsdatoen.
- pH i mediet: Mediets pH kan påvirke aktiviteten af visse antibiotika, hvorfor Mueller-Hinton agar har en nøje kontrolleret pH-værdi.
Ofte Stillede Spørgsmål (FAQ)
Hvad er en hæmningszone helt præcist?
En hæmningszone er det cirkulære, klare område omkring en antibiotikadisk på en agarplade, hvor bakterievæksten er blevet stoppet eller hæmmet af det antibiotikum, der er diffunderet ud i agaren. Diameteren af denne zone bruges til at bestemme, hvor følsom bakterien er over for det pågældende antibiotikum.

Hvorfor er Mueller-Hinton agar det foretrukne medie?
Mueller-Hinton agar anvendes, fordi den har flere fordelagtige egenskaber: den har en standardiseret sammensætning, den indeholder ikke stoffer, der hæmmer visse antibiotika (som sulfonamider og trimethoprim), den understøtter god vækst for de fleste almindelige patogener, og dens konsistens tillader god og reproducerbar diffusion af antibiotika.
Hvad betyder det, hvis en bakterie er 'intermediær'?
En intermediær klassificering betyder, at antibiotikummet muligvis ikke er effektivt ved en standarddosis. Det kan dog virke, hvis der gives en højere dosis, eller hvis infektionen er lokaliseret et sted i kroppen, hvor lægemidlet kan opnå en høj koncentration, f.eks. i urinvejene.
Er Kirby-Bauer-testen den eneste metode til resistensbestemmelse?
Nej, der findes flere andre metoder. Nogle af de mest almindelige inkluderer broth microdilution (bouillonfortynding), som bestemmer den Minimale Inhibitoriske Koncentration (MIC), og automatiserede systemer, der ofte bruges på store kliniske laboratorier for hurtigere resultater. E-test er en anden metode, der kombinerer principperne fra diffusion og fortynding for at give en direkte MIC-værdi.
Hvorfor er standardisering så vigtig for denne test?
Standardisering er afgørende, fordi resultatet (zonens diameter) er påvirket af mange variabler, såsom bakteriekoncentration, agartykkelse og inkubationstid. Uden faste standarder ville resultaterne ikke være pålidelige eller sammenlignelige mellem forskellige tests eller laboratorier, hvilket ville gøre det umuligt at træffe korrekte kliniske beslutninger baseret på testen.
Hvis du vil læse andre artikler, der ligner Kirby-Bauer-testen: En Guide til Resistens, kan du besøge kategorien Sundhed.
