05/05/2017
Når du står på apoteket med en recept i hånden, har du måske aldrig tænkt over det navn, der står på pakken. For de fleste er det blot en etiket, en identifikation af det lægemiddel, der skal hjælpe dem. Men bag hvert eneste navn på et godkendt lægemiddel ligger en yderst kompleks og strengt reguleret proces, hvor intet er overladt til tilfældighederne. Navngivning af medicin er en videnskab i sig selv, en balancegang mellem markedsføring, identitet og frem for alt patientsikkerhed. Et forkert eller vildledende navn kan i værste fald føre til alvorlige medicineringsfejl med katastrofale konsekvenser. I Danmark er det Lægemiddelstyrelsen, der varetager denne vigtige opgave, og de følger et nøje fastlagt regelsæt for at sikre, at navnet på din medicin er både sikkert og entydigt.

Processen er ikke kun en national affære. I en globaliseret verden, hvor lægemidler ofte markedsføres i hele EU, spiller Det Europæiske Lægemiddelagentur (EMA) også en afgørende rolle. Deres specialiserede navnekomité, Name Review Group (NRG), gransker hvert eneste navneforslag for at undgå forveksling på tværs af sprog og kulturer. Denne artikel vil guide dig gennem den fascinerende verden af lægemiddelnavngivning og afdække de regler, overvejelser og udfordringer, der er forbundet med at give et lægemiddel sit navn.
I Danmark kan et godkendt lægemiddel navngives på tre forskellige måder. Hver metode har sine egne specifikke regler og anvendelsesområder, som medicinalvirksomhederne skal navigere i, når de ansøger om markedsføringstilladelse.
- Et opfundet navn: Et unikt og kreativt navn, som virksomheden selv har udviklet. Dette er den mest almindelige metode for nye, innovative lægemidler.
- Et generisk navn efterfulgt af et varemærke eller navnet på indehaveren af markedsføringstilladelsen: Her bruges navnet på det aktive stof i lægemidlet, f.eks. "Paracetamol 'Firma A'".
- Et videnskabeligt navn efterfulgt af et varemærke eller navnet på indehaveren af markedsføringstilladelsen: Denne metode ligner den generiske, men bruger det mere komplekse kemiske navn (f.eks. IUPAC-navnet).
Valget af navngivningsstrategi afhænger af mange faktorer, herunder lægemidlets type, virksomhedens markedsføringsstrategi og de regulatoriske krav.
At skabe et opfundet navn til et lægemiddel er en kreativ proces, men den er langt fra fri. Lægemiddelstyrelsen har en række ufravigelige krav, der alle har til formål at beskytte patienterne.

Grundlæggende Principper: Klarhed og Sikkerhed
Ifølge Lægemiddellovens § 58, stk. 3, er de to vigtigste principper, at navnet ikke må være vildledende og ikke må kunne forveksles med andre lægemidler. Et navn må altså ikke antyde en virkning, sammensætning eller egenskab, som produktet ikke har. For eksempel ville et navn som "MirakelKur" aldrig blive godkendt. Desuden må navnet ikke kunne forveksles med det internationale anerkendte navn for det aktive stof (et såkaldt INN-navn), da dette kunne skabe farlig forvirring for sundhedspersonale. Danmark har tilsluttet sig både WHO-konventionen og Den Europæiske Farmakopé, hvilket betyder, at navne, der ligner disse standardiserede navne, vil blive afvist.
Hvad er Tilladt, og Hvad er Ikke?
Ud over de overordnede principper findes der en række konkrete regler:
- Udtale: Navnet skal som hovedregel kunne udtales. Derfor accepteres symboler, som f.eks. @ eller #, ikke som en del af et navn.
- Egennavne: Navnet må ikke bestå af et personnavn eller et stednavn.
- Tal: Tal kan kun indgå i navne på kombinationspræparater. Hvis begge styrker angives, skal de adskilles af en skråstreg (f.eks. Produktnavn 50/12,5 mg). For p-piller kan det være relevant at angive antallet af tabletter pr. cyklus.
- Udvidelser: Hvis en virksomhed ønsker at markedsføre en ny styrke eller form af et eksisterende lægemiddel, skal det ske under samme navn, eventuelt med et relevant suffiks (f.eks. "Depot" eller "Junior").
Forvekslingsrisiko: Den Vigtige Tre-Bogstavs-Regel
For at vurdere risikoen for forveksling med andre lægemiddelnavne arbejder myndighederne ud fra en tommelfingerregel om, at der generelt skal være en forskel på mindst tre bogstaver mellem to navne. Dette er dog ikke en absolut regel. Myndighederne ser på helheden, herunder hvordan navnene udtales og staves. To navne kan godt have mere end tre forskellige bogstaver, men stadig lyde så ens, at de kan forveksles i en travl klinisk hverdag. Omvendt kan navne med kun to forskellige bogstaver i sjældne tilfælde blive godkendt, hvis de visuelt og fonetisk er tilstrækkeligt forskellige. Denne vurdering er afgørende for at undgå medicineringsfejl, hvor en patient ved en fejl får udleveret et forkert præparat.
Når et lægemiddels patent udløber, kommer der ofte mange kopipræparater på markedet. Disse navngives typisk ved at bruge det generiske navn for det aktivt stof, efterfulgt af producentens navn. Dette skaber gennemsigtighed for både læger, apotekere og patienter.
Her er det afgørende, at det anvendte generiske navn er det korrekte danske navn, som det fremgår af Danske Lægemiddelstandarder (DLS). Navnet skal også afspejle, hvordan styrken er angivet. Hvis styrken er angivet i forhold til basen af det aktive stof, skal basens navn bruges. Hvis den er angivet i forhold til et salt, skal saltets navn bruges. Dette er teknisk, men vigtigt for at sikre korrekt dosering.
Lægemiddelstyrelsen har dog åbnet for en vis fleksibilitet. For at lette produktionen af fælles emballage til flere nordiske eller europæiske lande kan man acceptere afvigelser i stavemåden på selve pakningen, så længe det ikke er vildledende. I den officielle produktinformation (produktresuméet) og indlægssedlen skal den korrekte danske stavemåde fra DLS dog altid anvendes. Hvis der er uoverensstemmelse mellem det anvendte navn og den angivne styrke, kræver Lægemiddelstyrelsen, at der tilføjes en tydelig bemærkning i indlægssedlen for at undgå enhver tvivl hos brugeren.
Den Europæiske Dimension: EMA's Nåleøje
For lægemidler, der søges godkendt i hele EU via den centrale procedure, skal navneforslaget igennem en grundig evaluering hos Det Europæiske Lægemiddelagenturs (EMA) Name Review Group (NRG). Denne gruppe består af repræsentanter fra de nationale lægemiddelmyndigheder og har til formål at sikre, at et navn er sikkert at bruge i alle medlemslande.
NRG's proces er notorisk streng. De analyserer navneforslag ud fra lingvistiske, kulturelle og semantiske aspekter for at sikre, at navnet ikke har uheldige eller vildledende betydninger på et af de mange sprog i EU. Afvisningsraten er høj – helt op til 55% af de indsendte navneforslag bliver afvist. Selvom dette kan virke frustrerende for medicinalvirksomhederne, er formålet udelukkende at maksimere patientsikkerheden og minimere risikoen for fejl på tværs af landegrænser.
For at give et bedre overblik er her en tabel, der sammenligner de tre navngivningstyper.
| Navnetype | Kendetegn | Fordele | Udfordringer |
|---|---|---|---|
| Opfundet Navn | Unikt brandnavn skabt af virksomheden. | Stærk branding, let at huske for patienter, skaber unik identitet. | Meget streng godkendelsesproces, høj afvisningsrate hos EMA, risiko for forveksling. |
| Generisk Navn + Firma | Navnet på det aktive stof + producentens navn. | Høj gennemsigtighed, let at identificere det aktive stof, fremmer priskonkurrence. | Mindre markedsføringsværdi, kan skabe forvirring med mange enslydende navne. |
| Videnskabeligt Navn + Firma | Det kemiske navn + producentens navn. | Præcis videnskabelig identifikation. | Svært at udtale og huske for patienter, bruges sjældent. |
Ofte Stillede Spørgsmål (FAQ)
De strenge regler eksisterer primært for at garantere patientsikkerhed. Et navn, der er let at forveksle med et andet, eller som er vildledende om produktets effekt, kan føre til alvorlige og potentielt dødelige medicineringsfejl. Reglerne sikrer, at navnet er så klart og entydigt som muligt.
Nej, absolut ikke. Ethvert forslag til et opfundet navn skal gennemgå en grundig evaluering hos de nationale myndigheder som Lægemiddelstyrelsen og/eller EMA. Navnet må ikke være vildledende, ligne andre navne for meget, minde om INN-navne eller overtræde andre specifikke regler.
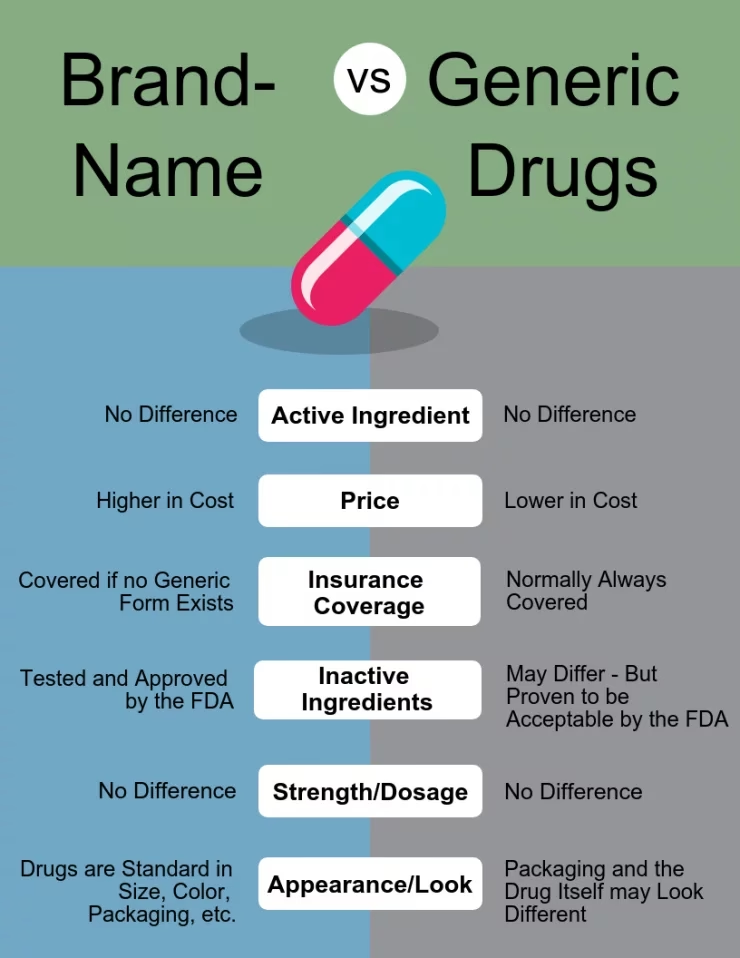
Et generisk navn (også kendt som det aktive stofnavn) er det alment anerkendte, ikke-kommercielle navn for den kemiske substans i medicinen, f.eks. 'Ibuprofen'. Et opfundet navn er et unikt varemærke skabt af producenten, f.eks. 'Ipren' eller 'Brufen', som begge indeholder ibuprofen.
Nej. Lægemiddelstyrelsen vurderer kun forslag til lægemiddelnavne som en del af en konkret ansøgning om markedsføringstilladelse. De foretager ikke forhåndsvurderinger.
Hvis EMA's Name Review Group (NRG) afviser et navneforslag, skal medicinalvirksomheden indsende et eller flere nye forslag til evaluering. Med en afvisningsrate på op til 55% er dette en meget almindelig del af processen, og virksomheder har ofte flere backup-navne klar.
Afslutningsvis er navnet på en medicinpakke kulminationen på en lang og omhyggelig proces. Det er et bevis på, at myndighederne har vejet hvert et bogstav på en vægtskål, hvor patientsikkerhed vejer tungest. Næste gang du ser et lægemiddelnavn, kan du tænke på den skjulte verden af regler, analyser og sikkerhedstjek, der sikrer, at navnet er mere end bare et navn – det er en fundamental del af en sikker og effektiv behandling.
Hvis du vil læse andre artikler, der ligner Navngivning af medicin: Mere end et navn, kan du besøge kategorien Sundhed.

