09/12/2011
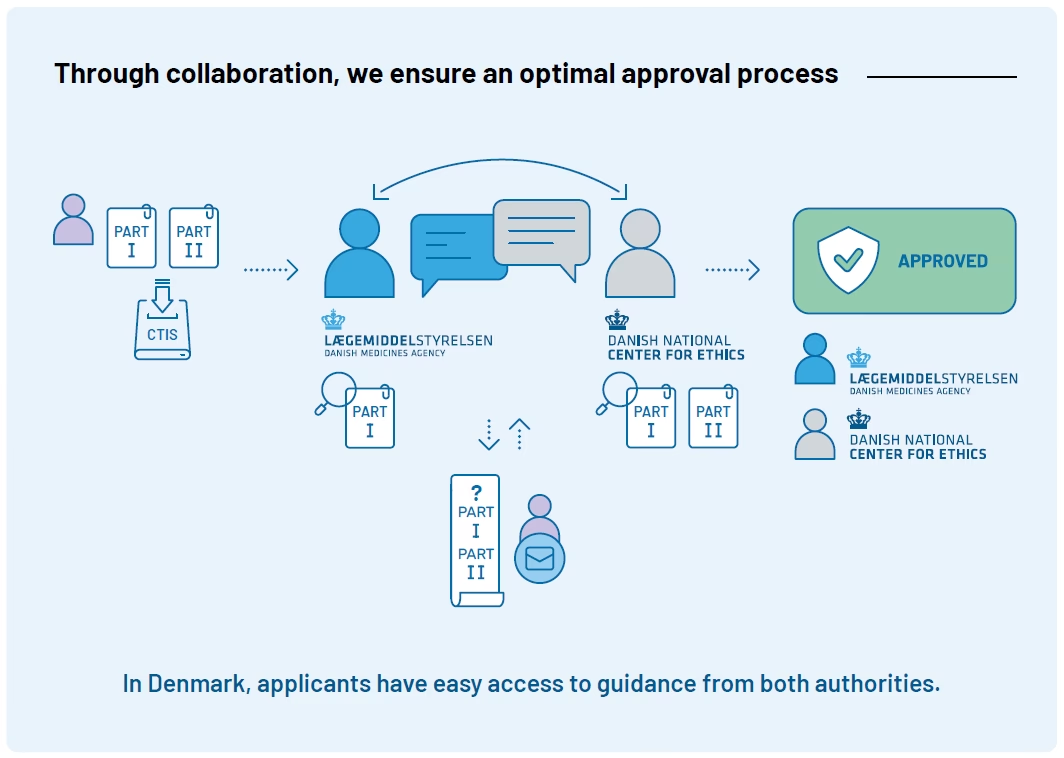
I Danmark kan man ikke bare sælge et hvilket som helst lægemiddel. Før en pille, en creme eller en indsprøjtning kan findes på apotekets hylder eller udleveres på et hospital, skal den gennemgå en yderst grundig og streng godkendelsesproces. Denne proces er designet til at beskytte dig som patient og sikre, at den medicin, du tager, er både sikker og effektiv. Det er Lægemiddelstyrelsen i Danmark eller Europa-Kommissionen, der står for denne afgørende opgave. Reglerne gælder ikke kun for konventionel medicin, men også for naturlægemidler samt stærke vitamin- og mineralpræparater. Uden en officiel markedsføringstilladelse er et lægemiddel ulovligt at sælge i Danmark.
Hvorfor er en godkendelse så vigtig?
Kravet om en markedsføringstilladelse er fundamentet for patientsikkerheden i vores sundhedssystem. Formålet er at garantere, at ethvert lægemiddel på det danske marked lever op til tre helt centrale principper:
- Sikkerhed: Myndighederne vurderer omhyggeligt alle kendte bivirkninger og risici ved lægemidlet. Fordelene ved at bruge medicinen skal klart opveje de potentielle risici. Dette baseres på omfattende data fra laboratorieforsøg og kliniske studier med mennesker.
- Effektivitet: Virksomheden, der har udviklet medicinen, skal kunne bevise, at den rent faktisk virker mod den sygdom eller de symptomer, den er beregnet til. Det er ikke nok at have en teori; effekten skal dokumenteres gennem videnskabelige undersøgelser.
- Kvalitet: Lægemidlet skal have en høj farmaceutisk kvalitet. Det betyder, at det skal produceres under kontrollerede forhold, så hver eneste pille eller dosis indeholder den præcise mængde aktivt stof. Derudover skal det være stabilt og fri for forurening.
Disse tre søjler sikrer, at læger kan ordinere medicin med tillid, og at patienter kan føle sig trygge ved deres behandling. Uden denne kontrol ville markedet være åbent for produkter, der i bedste fald er virkningsløse og i værste fald direkte skadelige.
De fire veje til en markedsføringstilladelse
En medicinalvirksomhed, der ønsker at sælge sit produkt i Danmark, kan vælge mellem fire forskellige procedurer for at opnå en godkendelse. Valget af procedure afhænger ofte af virksomhedens strategi og hvor bredt de ønsker at markedsføre lægemidlet i Europa.
Tabel over godkendelsesprocedurer
| Procedurens Navn | Geografisk Omfang | Beskrivelse |
|---|---|---|
| Den nationale procedure | Kun Danmark | Virksomheden ansøger kun om godkendelse i ét enkelt EU/EØS-land. Bruges ofte til produkter med et begrænset lokalt marked. |
| Den centrale procedure | Hele EU/EØS | Én enkelt ansøgning til Det Europæiske Lægemiddelagentur (EMA) giver en markedsføringstilladelse, der gælder i alle medlemslande samtidigt. Obligatorisk for visse typer avanceret medicin (f.eks. mod kræft, HIV, diabetes). |
| Den decentrale procedure (DCP) | Flere valgfrie EU/EØS-lande | Virksomheden ansøger i flere lande på samme tid, hvor et land fungerer som 'reference'-land og leder vurderingen. |
| Procedure for gensidig anerkendelse (MRP) | Flere valgfrie EU/EØS-lande | En allerede eksisterende national godkendelse i ét EU-land bruges som grundlag for at søge godkendelse i andre EU-lande. |
Fra laboratorium til patient: Ansøgningsprocessen
En ansøgning om markedsføringstilladelse er ikke blot et simpelt formular. Det er et enormt dossier, der kan fylde tusindvis af sider, og som indeholder al den videnskabelige dokumentation, der er indsamlet under lægemidlets udvikling. Processen starter typisk med prækliniske studier i laboratoriet og på dyr for at vurdere den grundlæggende sikkerhed og virkningsmekanisme. Hvis resultaterne er lovende, fortsætter udviklingen til kliniske forsøg med mennesker, som normalt er opdelt i tre faser, hvor man tester sikkerhed, dosering og effekt på stadigt større grupper af patienter. Hele denne dokumentation for effektivitet og sikkerhed skal indgå i ansøgningen.
Derudover skal virksomheden levere detaljeret dokumentation for den farmaceutiske kvalitet, herunder produktionsmetoder, kontrol af råvarer og stabilitetstest af det færdige produkt. Eksperter hos Lægemiddelstyrelsen eller EMA gennemgår minutiøst alle disse data for at sikre, at konklusionerne er velbegrundede, og at lægemidlet lever op til de høje standarder.
Produktresumé og indlægsseddel: Din guide til sikker brug
Når et lægemiddel bliver godkendt, udarbejder myndighederne et officielt dokument kaldet produktresuméet (SPC - Summary of Product Characteristics). Dette dokument er primært rettet mod sundhedspersonale som læger og farmaceuter og indeholder al essentiel information om lægemidlet: dets virkning, bivirkninger, advarsler, dosering, aktive stoffer og meget mere.
Produktresuméet danner grundlag for den indlægsseddel, som du finder i medicinpakken. Indlægssedlen er en version af produktresuméet, der er skrevet i et letforståeligt sprog for patienter. Den er din vigtigste kilde til information om, hvordan du skal tage din medicin korrekt og sikkert. Det er også i produktresuméet, rammerne for virksomhedens markedsføring af lægemidlet fastlægges – de må ikke love mere, end hvad der er videnskabeligt dokumenteret og godkendt.

Når en godkendelse trækkes tilbage
En markedsføringstilladelse er ikke nødvendigvis evig. Lægemiddelstyrelsen kan under særlige omstændigheder trække en tilladelse tilbage. Dette kan ske, hvis:
- Balance mellem fordele og risici ændres: Der kan efter markedsføring opdages nye, alvorlige bivirkninger, som gør, at risiciene ved at bruge medicinen ikke længere står mål med fordelene.
- Manglende videnskabelig relevans: Lægemidlet er måske blevet overhalet af nyere og bedre behandlinger, så det ikke længere følger med den videnskabelige udvikling.
- Kvalitetsproblemer: Der opdages alvorlige problemer med produktionen eller kvaliteten af lægemidlet.
Dette system for overvågning sikrer, at medicin på markedet konstant vurderes, så sikkerheden for patienterne forbliver i højsædet.
Ofte Stillede Spørgsmål (FAQ)
Kan jeg lovligt købe medicin fra udlandet, som ikke er godkendt i Danmark?
Reglerne for privatimport af medicin er meget strenge. Selvom det i visse tilfælde er muligt at medbringe medicin til personligt brug fra et andet EU/EØS-land, er det generelt ulovligt at få tilsendt medicin, der kræver recept i Danmark. At købe medicin fra ukendte hjemmesider online er ekstremt risikabelt, da der er stor fare for at modtage forfalskede, virkningsløse eller direkte farlige produkter.
Hvad med naturmedicin og stærke kosttilskud?
Som nævnt gælder reglerne også for naturlægemidler og stærke vitamin- og mineralpræparater. Disse skal også have en markedsføringstilladelse fra Lægemiddelstyrelsen for at kunne sælges med påstande om at kunne forebygge eller behandle sygdomme. Almindelige kosttilskud, der ikke har en lægemiddelgodkendelse, må ikke markedsføres med medicinske anprisninger og er underlagt Fødevarestyrelsens regler.
Hvordan kan jeg tjekke, om et lægemiddel er godkendt i Danmark?
Den nemmeste måde er at se, om pakken og indlægssedlen er på dansk. Alle godkendte lægemidler skal have dansk mærkning. Du kan også søge i Lægemiddelstyrelsens officielle database over produktresuméer for at finde detaljeret information om alle lægemidler, der er godkendt til salg i Danmark.
Er en godkendelse det samme som at få tilskud?
Nej, en markedsføringstilladelse og medicintilskud er to forskellige ting. Lægemiddelstyrelsen vurderer medicinens sikkerhed, effekt og kvalitet. Når medicinen er godkendt, vurderer Medicintilskudsnævnet, om prisen på medicinen står i et rimeligt forhold til dens behandlingsmæssige værdi. Først derefter træffes der beslutning om, hvorvidt der skal ydes offentligt tilskud til medicinen, så den bliver billigere for patienten.
Hvis du vil læse andre artikler, der ligner Din medicins vej til det danske marked, kan du besøge kategorien Sundhed.