19/01/2025
Leveren er et af kroppens mest bemærkelsesværdige organer, ikke mindst på grund af dens utrolige evne til at regenerere sig selv. Hvis en del af leveren fjernes, kan den resterende del vokse tilbage til sin oprindelige størrelse på blot få uger. Denne proces er hjørnestenen i feltet kendt som regenerativ medicin, et område, der søger at reparere, erstatte eller regenerere beskadigede celler, væv og organer. Men ved kroniske leversygdomme, såsom non-alkoholisk fedtleversygdom (NAFLD) eller skrumpelever (cirrose), svigter denne regenerative evne. Vævet bliver i stedet arret i en proces kaldet fibrose, hvilket forhindrer organet i at fungere korrekt. Ny forskning har dog identificeret en potentiel terapeutisk nøgle, proteinet Mfap4, som, når det undertrykkes, ser ud til at genstarte leverens helingsproces og give nyt håb til millioner af patienter verden over.
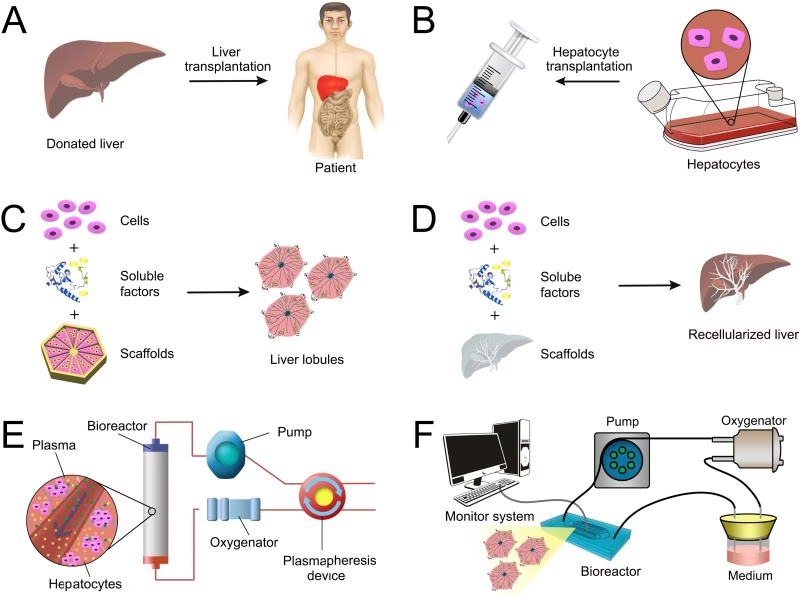
- Leverens Komplekse Regenerationsevne
- Identifikationen af Mfap4: En Ny Terapeutisk Målsætning
- Forbedret Celleproliferation og Regeneration in Vitro og in Vivo
- Terapeutisk Potentiale ved Kronisk Leversygdom som NASH
- Fra Mus til Menneske: Er Effekten Konserveret?
- Sikkerhedsprofil: En Vigtig Overvejelse
- Ofte Stillede Spørgsmål
Leverens Komplekse Regenerationsevne
For at forstå potentialet i den nye opdagelse er det vigtigt at kende til leverens regenerative mekanismer. Hovedparten af leverens celler kaldes hepatocytter. Disse specialiserede celler er i stand til at dele sig og forny sig selv for at erstatte beskadiget væv. I en sund lever er denne proces yderst effektiv. Forskning på mus har vist, at selv når to tredjedele af leveren fjernes, kan den genvinde sin oprindelige vægt på omkring 10 dage. Denne viden er afgørende for patienter, der skal gennemgå store leveroperationer eller har brug for transplantation.
Ved kronisk skade, som ses ved langvarige leversygdomme, ændres billedet dog. Her opstår en såkaldt "duktulær reaktion", hvor en anden type celler, leverstamceller (LPCs), begynder at formere sig. Selvom disse celler teoretisk set kan udvikle sig til både hepatocytter og galdegangsceller, er deres rolle i praksis uklar. Faktisk er en øget mængde af disse celler ofte forbundet med forværret fibrose og en dårligere prognose. Forskere diskuterer stadig, hvor disse celler stammer fra – nogle studier peger på, at de kommer fra dedifferentierede hepatocytter, mens andre tyder på, at de stammer fra galdegangsceller. Denne kompleksitet understreger behovet for at finde mere direkte måder at stimulere de primære hepatocytters regenerative evne på.
Identifikationen af Mfap4: En Ny Terapeutisk Målsætning
Med det formål at finde nye måder at forbedre leverens endogene (interne) regenerative kapacitet, gennemførte forskere en avanceret genetisk screening i en musemodel for kronisk leversygdom. Målet var at identificere gener, der, når de blev "slukket" eller dæmpet, ville give levercellerne en overlevelses- eller vækstfordel under kronisk stress. Ved hjælp af en teknik, der bruger små RNA-strenge (shRNA) til at hæmme specifikke gener i omkring 5-10% af leverens hepatocytter, skabte de et konkurrencepræget miljø. Musene blev udsat for et leverskadeligt stof (thioacetamid) i 8 uger, hvilket simulerede kronisk sygdom.
Hypotesen var simpel: Hvis nedlukningen af et bestemt gen forbedrede cellernes evne til at regenerere, ville netop disse celler formere sig hurtigere end de andre og blive mere talrige i leveren. Efter forsøgsperioden analyserede forskerne levervævet og fandt, at celler med en hæmning af genet for microfibril associated protein 4 (Mfap4) var blevet markant beriget. Fire uafhængige shRNA-strenge rettet mod Mfap4 viste alle en stærk positiv effekt, hvilket gjorde Mfap4 til den mest lovende kandidat fra screeningen. Som en kontrol viste screeningen også, at hæmning af genet for c-MET, en kendt receptor essentiel for leverregeneration, førte til, at cellerne forsvandt, hvilket bekræftede metodens pålidelighed.
Forbedret Celleproliferation og Regeneration in Vitro og in Vivo
Efter at have identificeret Mfap4 som et potentielt mål, gik forskerne videre med at validere dets funktion. Først i laboratoriet (in vitro) skabte de udødeliggjorte levercellelinjer, hvor Mfap4 var permanent nedreguleret. Resultaterne var slående:
- Hurtigere sårheling: I en "wound healing assay", hvor et hul skrabes i et cellelag, lukkede cellerne med reduceret Mfap4 hullet signifikant hurtigere end kontrolcellerne.
- Øget celledeling: Målinger viste, at en større andel af Mfap4-hæmmede celler var i gang med at replikere deres DNA, et tegn på hurtigere celledeling.
- Kortere fordoblingstid: Cellerne fordoblede deres antal på kortere tid.
Disse resultater blev derefter testet i levende mus (in vivo) ved hjælp af en avanceret model (FAH knockout mus). I denne model kan kun genetisk modificerede celler overleve og repopulere leveren. Da forskerne introducerede celler med Mfap4-hæmning, observerede de en markant hurtigere repopulering af leveren sammenlignet med kontrolgruppen. I en mere ekstrem version af forsøget, hvor kun et meget lille antal celler blev introduceret, overlevede musene med Mfap4-hæmning, mens kontrolmusene døde af leversvigt. Dette demonstrerede en klar overlevelsesfordel.
Endelig blev effekten testet i en model med partiel hepatektomi, hvor to tredjedele af leveren kirurgisk fjernes. Også her viste mus med Mfap4-hæmning en signifikant hurtigere regeneration med flere celler i aktiv deling 42 og 48 timer efter operationen.
Sammenligning af Regenerative Evner
Den observerede effekt kan opsummeres i en sammenligningstabel:
| Parameter | Kontrolgruppe (Normal Mfap4) | Testgruppe (Reduceret Mfap4) |
|---|---|---|
| Celleproliferation (in vitro) | Normal hastighed | Signifikant hurtigere |
| Leverrepopulation (FAH mus) | Langsommere klonal ekspansion | Markant hurtigere |
| Regeneration efter operation | Normal regenerationsrate | Forøget antal delende celler |
| Overlevelse ved leversvigt | Lav | Høj |
Terapeutisk Potentiale ved Kronisk Leversygdom som NASH
Med de stærke pro-regenerative effekter bevist, var det næste logiske skridt at undersøge, om hæmning af Mfap4 kunne modvirke skaderne ved kroniske leversygdomme. Forskerne brugte to relevante musemodeller:
- Thioacetamid (TAA)-induceret skade: En aggressiv model, der forårsager alvorlig fibrose.
- "Western Diet"-model: En mere fysiologisk relevant model, hvor mus fodres med en fedt- og sukkerholdig kost for at udvikle non-alkoholisk steatohepatitis (NASH), en fremskreden form for fedtleversygdom, der ligner den humane tilstand.
I begge modeller var resultaterne bemærkelsesværdige. Mus, hvis leverceller havde reduceret Mfap4, udviklede signifikant mindre fibrose (arvæv). Deres levere havde en glattere overflade og så generelt sundere ud. I NASH-modellen observerede man desuden en reduktion i steatose (fedtophobning i leveren). Dette indikerer, at en forbedret regenerativ kapacitet ikke kun reparerer skader, men også kan dæmpe selve sygdomsprocessen. En interessant observation var fraværet af ovalcelle-hyperplasi hos Mfap4-musene, hvilket tyder på, at deres hepatocytter ikke var udmattede og stadig var i stand til at kompensere for skaden – et tegn på en sundere lever.

Fra Mus til Menneske: Er Effekten Konserveret?
Et afgørende spørgsmål er altid, om resultater fra mus kan overføres til mennesker. For at undersøge dette genererede forskerne humane levercellelinjer med nedsat MFAP4-ekspression. Resultaterne afspejlede dem fra musecellerne: de humane celler viste også signifikant hurtigere sårheling og øget celledeling. Dette tyder stærkt på, at mekanismen er konserveret mellem arterne.
Ydermere fandt forskerne, at MFAP4-niveauerne er forhøjede i levervæv fra mennesker med skrumpelever sammenlignet med raske levere. Proteinet blev fundet både i de fibrotiske ar-områder og inde i selve hepatocytterne i de syge levere. Dette understøtter ideen om, at MFAP4 spiller en rolle i sygdomsprogressionen og styrker rationalet for at målrette det terapeutisk.
Sikkerhedsprofil: En Vigtig Overvejelse
Når man taler om at øge celleproliferation, opstår der naturligt en bekymring for kræftrisiko. Forskerne tog denne bekymring meget alvorligt. I et langvarigt studie fulgte de mus med Mfap4-hæmning i leveren i et helt år. Ved afslutningen af studiet var musene sunde, og der var ingen tegn på tumorer eller andre unormale vækstforhold i deres levere. I et andet forsøg viste de, at mens hæmning af et kendt tumor-suppressorgen (Pten) førte til tumorvækst, gjorde hæmning af Mfap4 det ikke. Dette indikerer, at Mfap4-hæmning fremmer en kontrolleret, regenerativ proliferation snarere end den ukontrollerede vækst, der kendetegner kræft, hvilket peger på en lovende sikkerhedsprofil.
Ofte Stillede Spørgsmål
Hvad er Mfap4 helt præcist?
Mfap4 (microfibril associated protein 4) er et protein, der er en del af den ekstracellulære matrix – det stillads, der omgiver cellerne. Det er kendt for at være involveret i vævsstruktur, og tidligere studier har vist, at dets niveauer er forhøjede ved fibrose i både lever og lunger. Denne nye forskning peger på, at det også spiller en direkte regulerende rolle i hepatocytters evne til at dele sig.
Hvornår kan vi forvente en behandling baseret på dette?
Det er vigtigt at understrege, at dette er præklinisk forskning, udført i cellekulturer og dyremodeller. Selvom resultaterne er yderst lovende, er næste skridt kliniske forsøg på mennesker for at teste både sikkerhed og effekt. Denne proces tager typisk adskillige år. Dog åbner opdagelsen op for udviklingen af nye lægemidler, f.eks. baseret på siRNA-teknologi, der specifikt kan målrette MFAP4 i leveren.
Er denne tilgang kun relevant for leversygdom?
Forskningen fokuserer specifikt på leveren, da den har en unik regenerativ kapacitet, og Mfap4 ser ud til at være en vigtig regulator her. Princippet om at fjerne en "bremse" på regeneration for at fremme heling kan potentielt være relevant for andre væv, men det vil kræve separat forskning. Lige nu er det største potentiale inden for behandling af kroniske leversygdomme som NASH og cirrose.
Hvordan adskiller dette sig fra en levertransplantation?
En levertransplantation er en sidste udvej, hvor hele det syge organ erstattes med et sundt organ fra en donor. Den tilgang, der beskrives her, er en form for regenerativ medicin, der sigter mod at hjælpe kroppens *eget* organ med at hele sig selv. Ved at forbedre leverens naturlige regenerative evne kan man potentielt bremse eller endda vende sygdomsprogressionen, hvilket kan hjælpe patienter med at undgå eller udskyde behovet for en transplantation.
Hvis du vil læse andre artikler, der ligner Nyt Håb for Kronisk Leversygdom: Mfap4 Nøglen, kan du besøge kategorien Sundhed.