19/04/2020
Spørgsmålet om, hvorvidt HIV-medicin er godkendt af FDA (U.S. Food and Drug Administration), er afgørende for millioner af mennesker verden over. Svaret er et rungende ja. I modsætning til enhver misforståelse er der ikke kun én, men adskillige FDA-godkendte lægemidler til behandling af HIV. Disse lægemidler, kendt som antiretroviral terapi (ART), har revolutioneret behandlingen af HIV og omdannet, hvad der engang var en dødsdom, til en håndterbar kronisk tilstand. FDA's godkendelse er et globalt anerkendt stempel for sikkerhed og effektivitet, og processen bag er ekstremt grundig for at beskytte folkesundheden.

Hvad er FDA, og hvorfor er deres godkendelse vigtig?
FDA er den amerikanske fødevare- og lægemiddelmyndighed. Det er en statslig myndighed under det amerikanske sundhedsministerium, der har ansvaret for at beskytte folkesundheden ved at sikre sikkerheden, effektiviteten og kvaliteten af humane og veterinære lægemidler, biologiske produkter og medicinsk udstyr. Deres ansvarsområde omfatter også regulering af fødevarer, kosttilskud og kosmetik.
Når FDA godkender et lægemiddel, betyder det, at agenturet har gennemgået omfattende videnskabelige data og kliniske forsøg og konkluderet, at fordelene ved lægemidlet opvejer de kendte risici for den tilsigtede anvendelse. For en alvorlig sygdom som HIV er denne godkendelsesproces ikke kun en formalitet; det er en livsvigtig garanti for patienter og sundhedspersonale om, at behandlingen er både virkningsfuld og så sikker som muligt. Mange landes egne sundhedsmyndigheder, herunder Det Europæiske Lægemiddelagentur (EMA), ser ofte hen til FDA's beslutninger som en vigtig reference.
Den Strenge Proces for Godkendelse af HIV-medicin
Vejen fra et kemisk molekyle i et laboratorium til et godkendt lægemiddel på apotekets hylder er lang og kompleks. Processen er designet til at være omhyggelig og er opdelt i flere faser for at sikre maksimal patientsikkerhed.
Prækliniske Studier
Før et potentielt lægemiddel overhovedet testes på mennesker, gennemgår det omfattende prækliniske studier. Dette indebærer laboratorieundersøgelser (in vitro) og dyreforsøg (in vivo) for at vurdere den grundlæggende sikkerhed og farmakologiske profil. Forskere undersøger, hvordan stoffet absorberes, fordeles, metaboliseres og udskilles, samt dets potentielle toksicitet.
Kliniske Forsøg på Mennesker
Hvis de prækliniske studier er lovende, kan lægemiddelproducenten ansøge FDA om tilladelse til at starte kliniske forsøg på mennesker. Disse er typisk opdelt i tre faser:
- Fase I: I denne fase testes lægemidlet på en lille gruppe (20-80) raske frivillige. Hovedformålet er at vurdere sikkerheden, bestemme et sikkert dosisinterval og identificere eventuelle umiddelbare bivirkninger.
- Fase II: Lægemidlet gives til en større gruppe patienter (100-300), der har den sygdom, det er beregnet til at behandle – i dette tilfælde HIV. Formålet er at vurdere lægemidlets effektivitet og fortsat evaluere dets sikkerhed på kort sigt.
- Fase III: Dette er den mest omfattende fase, der involverer store patientgrupper (flere tusinde) på tværs af forskellige geografiske områder. Lægemidlet sammenlignes ofte med eksisterende standardbehandlinger eller placebo for definitivt at bekræfte dets effektivitet, overvåge bivirkninger og indsamle oplysninger, der vil muliggøre sikker anvendelse.
FDA-gennemgang og Godkendelse
Efter vellykkede fase III-forsøg indsender lægemiddelproducenten en New Drug Application (NDA) til FDA. Denne ansøgning indeholder alle data fra de prækliniske og kliniske studier. Et team af FDA-eksperter – herunder læger, statistikere, kemikere og farmakologer – gennemgår grundigt alle oplysninger for at træffe en beslutning. For livsvigtige lægemidler, som dem mod HIV, benytter FDA sig ofte af fremskyndede programmer ('Fast Track', 'Breakthrough Therapy') for at gøre nye, lovende behandlinger tilgængelige hurtigere, uden at gå på kompromis med de videnskabelige standarder.
Fase IV: Overvågning efter Markedsføring
Selv efter et lægemiddel er godkendt og tilgængeligt for offentligheden, stopper overvågningen ikke. Fase IV-studier, også kendt som post-marketing surveillance, fortsætter med at indsamle data om lægemidlets sikkerhed, risici, fordele og optimal anvendelse i en bredere befolkning og over længere tid.
Typer af FDA-godkendt HIV-medicin
Moderne HIV-behandling, antiretroviral terapi (ART), består typisk af en kombination af tre eller flere lægemidler fra forskellige klasser for at angribe virussen på forskellige stadier af dens livscyklus. Dette minimerer risikoen for, at virussen udvikler resistens. Der er flere klasser af FDA-godkendte antiretrovirale lægemidler.
| Lægemiddelklasse | Virkningsmekanisme | Eksempel på aktivt stof |
|---|---|---|
| Nukleosid/nukleotid revers transkriptasehæmmere (NRTI'er) | Blokerer enzymet revers transkriptase, som HIV bruger til at kopiere sit genetiske materiale. | Tenofovir, Emtricitabin, Abacavir |
| Non-nukleosid revers transkriptasehæmmere (NNRTI'er) | Binder sig til og ændrer revers transkriptase, så det ikke længere fungerer. | Efavirenz, Rilpivirin, Doravirin |
| Proteasehæmmere (PI'er) | Blokerer enzymet protease, som HIV har brug for til at samle nye viruspartikler. | Darunavir, Atazanavir, Ritonavir |
| Integrasehæmmere (INSTI'er) | Blokerer enzymet integrase, som HIV bruger til at indsætte sit DNA i værtscellens DNA. | Dolutegravir, Bictegravir, Raltegravir |
| Entry-hæmmere | Forhindrer HIV i at trænge ind i værtscellen (CD4-cellen). | Maraviroc, Enfuvirtid |
Kombinationstabletter, der indeholder flere aktive stoffer i én pille, er også blevet godkendt og er i dag standardbehandling for mange, da de forenkler behandlingsregimet betydeligt.
Ofte Stillede Spørgsmål (FAQ)
Betyder FDA-godkendelse, at et lægemiddel er 100% sikkert?
Ingen medicin er 100% sikker. FDA-godkendelse betyder, at efter en grundig gennemgang af videnskabelige data er det blevet fastslået, at lægemidlets fordele for patienterne opvejer dets kendte og potentielle risici. Alle lægemidler har potentielle bivirkninger, og det er vigtigt at diskutere disse med sin læge.
Er medicin godkendt i USA automatisk godkendt i Danmark?
Nej. I Danmark og resten af EU er det Det Europæiske Lægemiddelagentur (EMA) og den nationale Lægemiddelstyrelse, der står for godkendelsen. Processerne hos FDA og EMA er dog meget ens og baseret på de samme videnskabelige principper, og de samarbejder ofte. En godkendelse fra den ene myndighed fører ofte hurtigt til en godkendelse fra den anden.
Hvad er PrEP, og er det FDA-godkendt?
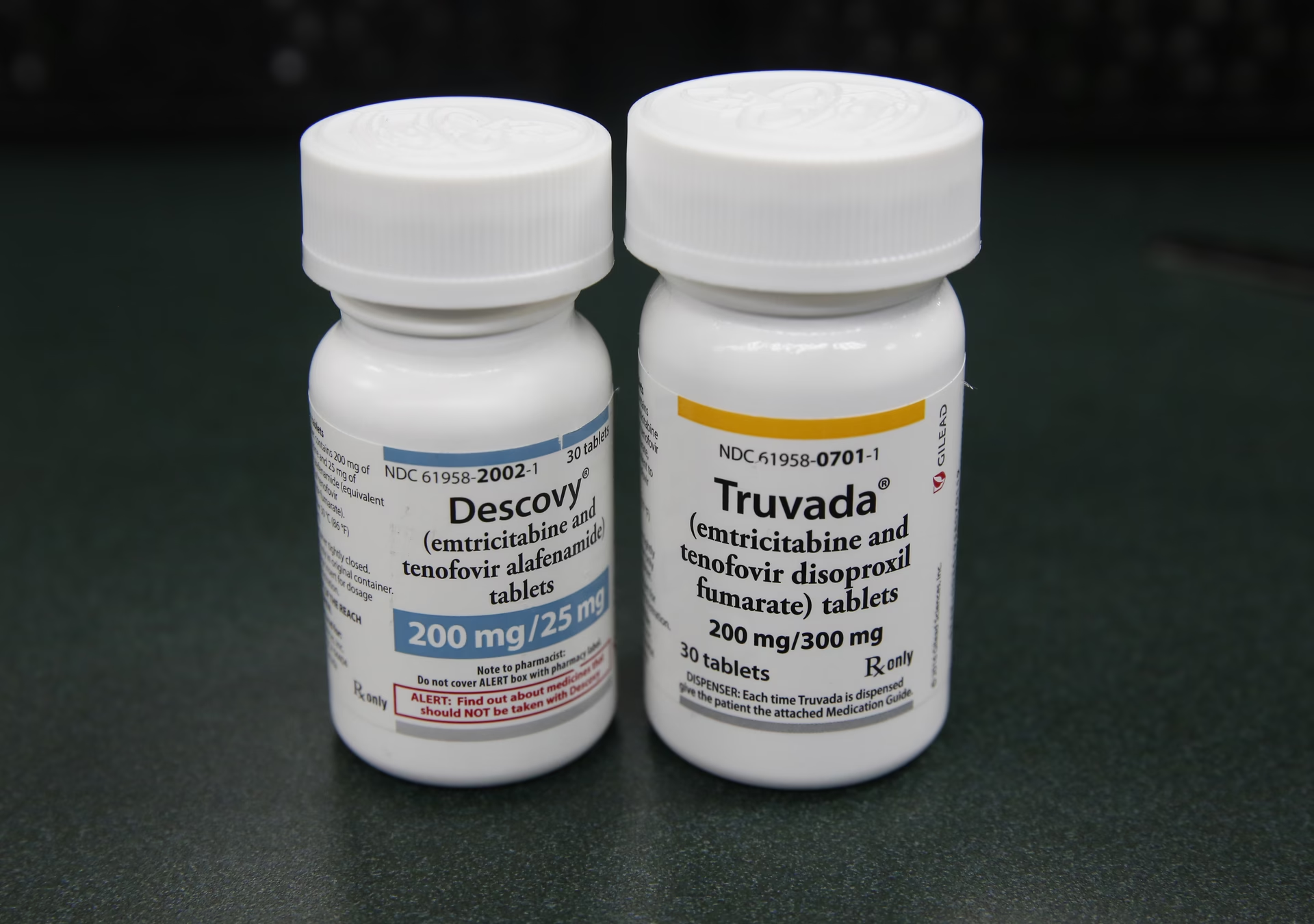
PrEP står for Pre-Exposure Prophylaxis. Det er en forebyggende behandling, hvor personer, der er i høj risiko for at blive smittet med HIV, tager en daglig pille for at beskytte sig. De lægemidler, der anvendes til PrEP (f.eks. kombinationen af tenofovir og emtricitabin), er fuldt ud godkendt af FDA til dette formål og har vist sig at være yderst effektive.
Hvorfor kommer der hele tiden ny HIV-medicin?
Forskningen står aldrig stille. Selvom de nuværende behandlinger er meget effektive, arbejder forskere konstant på at udvikle nye lægemidler, der er endnu mere effektive, har færre bivirkninger, kræver færre doser (f.eks. langtidsvirkende injektioner i stedet for daglige piller) og kan bekæmpe resistent HIV. Hvert nyt lægemiddel skal gennemgå den samme strenge FDA-godkendelsesproces.
Hvis du vil læse andre artikler, der ligner Er HIV-medicin godkendt af FDA?, kan du besøge kategorien Medicin.