15/07/2001
I den komplekse verden af hæmostase og trombose spiller blodplader en afgørende, men tveægget rolle. De er livsvigtige for at standse blødninger, men de er også centrale aktører i dannelsen af farlige blodpropper, der kan føre til hjerteanfald og slagtilfælde. I årtier har forskere og læger søgt efter effektive måder at hæmme blodpladernes funktion på uden at kompromittere kroppens evne til at hele. Dette har ført til udviklingen af en række blodpladehæmmende lægemidler. Mens tidlige lægemidler som aspirin og clopidogrel har vist sig effektive, retter de sig mod specifikke aktiveringsveje. Den ultimative strategi er dog at blokere den fælles endelige vej for blodpladeaggregation, og her er en specifik receptor kommet i fokus: Integrin αIIbβ3 (også kendt som glykoprotein IIb/IIIa). Denne artikel dykker ned i, hvorfor netop denne receptor er et så afgørende mål for moderne antitrombotisk behandling.

Forståelse af blodplader og deres funktion
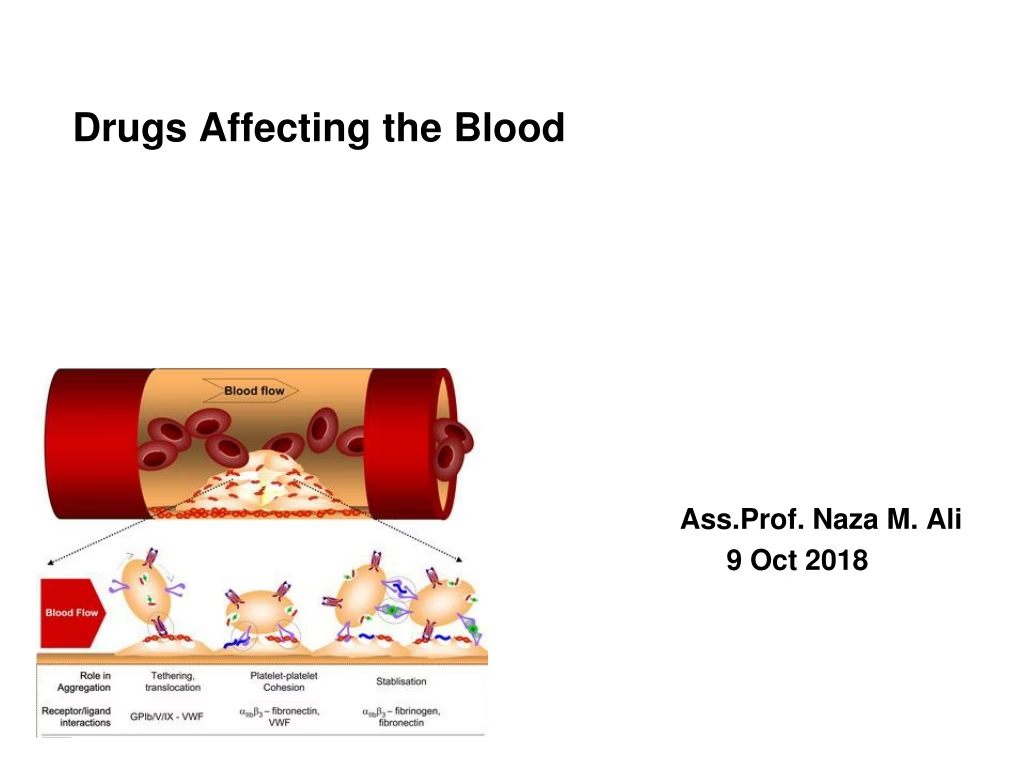
Blodplader, eller trombocytter, er små, kerneløse cellefragmenter i vores blod. Deres primære opgave er at reagere på skader i blodkarrene. Når et kar beskadiges, aktiveres blodpladerne, ændrer form og klæber sig fast til det skadede område og til hinanden. Denne proces, kendt som blodpladeaggregation, danner en prop, der midlertidigt standser blødningen. For at styrke denne prop, aktiverer blodpladerne koagulationskaskaden, hvilket fører til dannelsen af et fibrinetværk, som fanger røde blodlegemer og andre blodplader og danner en stabil blodprop (trombe).
Problemet opstår, når denne proces sker på det forkerte sted, typisk i en pulsåre, der er forsnævret af åreforkalkning (aterosklerose). Her kan en blodprop blokere blodforsyningen til vitale organer som hjertet eller hjernen, hvilket resulterer i henholdsvis et myokardieinfarkt (hjerteanfald) eller et iskæmisk slagtilfælde. Derfor er lægemidler, der kan hæmme denne proces, essentielle i moderne kardiologi.
Tidlige generationer af blodpladehæmmere
Før udviklingen af lægemidler rettet mod Integrin αIIbβ3, var behandlingen baseret på stoffer, der påvirkede andre dele af blodpladernes aktiveringsproces.
Dipyridamol
Dipyridamol blev oprindeligt syntetiseret for over et halvt århundrede siden som et karudvidende middel til hjertet. Senere blev det opdaget, at det kunne hæmme blodpladernes klæbeevne. Dets primære virkningsmekanisme er at hæmme genoptagelsen af adenosin i cellerne, hvilket øger koncentrationen af adenosin i plasma. Adenosin er en potent hæmmer af blodpladeaggregation. Selvom effekten af dipyridamol alene har været omdiskuteret, viste det store ESPS-2-studie positive resultater i forebyggelsen af slagtilfælde, især i en ny formulering med forbedret biotilgængelighed, ofte i kombination med aspirin.
Thienopyridiner: Ticlopidin og Clopidogrel
Denne klasse af lægemidler blev opdaget gennem dyreforsøg. Ticlopidin, det første i klassen, viste sig at hæmme ADP-induceret blodpladeaggregation. Det tog over 20 år at identificere den præcise mekanisme: et aktivt stofskifteprodukt af lægemidlet blokerer irreversibelt en specifik ADP-receptor på blodpladerne kaldet P2Y12. Senere kom Clopidogrel, en strukturelt beslægtet efterfølger, som havde en bedre sikkerhedsprofil, især med hensyn til alvorlige bivirkninger som knoglemarvstoksicitet. Ligesom aspirin forårsager clopidogrel en permanent defekt i blodpladen, hvilket betyder, at effekten varer hele blodpladens levetid (ca. 7-10 dage). Dette muliggør dosering én gang dagligt. Clopidogrel, ofte i kombination med aspirin (kendt som dobbelt blodpladehæmmende behandling), er en hjørnesten i behandlingen af patienter med akut koronarsyndrom og efter indsættelse af stents.
Integrin αIIbβ3: Den afgørende fælles vej
Ulempen ved lægemidler som aspirin og clopidogrel er, at de kun blokerer én aktiveringsvej hver (henholdsvis TXA2-vejen og ADP/P2Y12-vejen). Blodplader kan dog aktiveres af mange forskellige stimuli, herunder trombin, kollagen og adrenalin. Uanset hvilken stimulus der starter processen, er det sidste og afgørende skridt for, at blodpladerne kan klumpe sig sammen, det samme: aktiveringen af Integrin αIIbβ3-receptoren.
Når en blodplade aktiveres, gennemgår denne receptor en konformationsændring. Dette gør det muligt for den at binde sig med høj affinitet til adhæsive proteiner, primært fibrinogen. Fibrinogen fungerer som en bro, der forbinder to blodplader via deres αIIbβ3-receptorer. Med op til 80.000 af disse receptorer på overfladen af hver blodplade, skabes der hurtigt et stærkt og stabilt aggregat. Ved at blokere denne receptor kan man teoretisk set stoppe blodpladeaggregation, uanset hvad der oprindeligt udløste den.
Inspirationen til at målrette denne receptor kom fra studier af en sjælden arvelig sygdom kaldet Glanzmanns trombasteni. Patienter med denne lidelse mangler funktionelle GPIIb/IIIa-receptorer. Deres blodplader kan ikke aggregere som reaktion på nogen af de kendte agonister, hvilket fører til en alvorlig blødningstendens. Dette "naturens eksperiment" beviste, at en effektiv blokade af denne receptor ville være en yderst potent blodpladehæmmende strategi.
GPIIb/IIIa-antagonister: Fra laboratorium til klinik
Baseret på denne viden begyndte udviklingen af lægemidler, der kunne blokere Integrin αIIbβ3-receptoren. De første succesfulde midler var baseret på monoklonale antistoffer.
Intravenøse midler
Forskeren Barry Coller udviklede et monoklonalt antistof (10E5), der specifikt kunne blokere fibrinogenbindingen til GPIIb/IIIa og dermed inducere en tilstand, der lignede Glanzmanns trombasteni. For at undgå et immunrespons hos mennesker blev antistoffet humaniseret og udviklet til lægemidlet Abciximab. Dette middel, sammen med andre intravenøse GPIIb/IIIa-hæmmere som eptifibatid (en syntetisk peptid) og tirofiban (et ikke-peptid molekyle), viste sig at være ekstremt effektivt. Det store EPIC-studie demonstrerede, at Abciximab, givet i tillæg til standardbehandling, markant reducerede risikoen for iskæmiske komplikationer hos højrisikopatienter, der gennemgik ballonudvidelse af kranspulsårerne (PTCA). Disse lægemidler administreres intravenøst på hospitaler og bruges primært i akutte situationer med høj trombotisk risiko.
| Lægemiddel | Type | Binding | Primær anvendelse |
|---|---|---|---|
| Abciximab | Monoklonalt antistof-fragment | Irreversibel (lang virkning) | Højrisiko perkutan koronar intervention (PCI) |
| Eptifibatid | Syntetisk cyklisk heptapeptid | Reversibel (kort virkning) | Akut koronarsyndrom, PCI |
| Tirofiban | Ikke-peptid tyrosin-derivat | Reversibel (kort virkning) | Akut koronarsyndrom, PCI |
De skuffende orale midler
Successen med de intravenøse midler førte til et stort ønske om at udvikle orale GPIIb/IIIa-hæmmere til langtidsbehandling af patienter med kronisk hjertesygdom. Desværre blev dette en stor skuffelse. Flere store kliniske forsøg med tusindvis af patienter, der testede lægemidler som xemilofiban, orbofiban og sibrafiban, viste konsekvent, at de ikke var mere effektive end aspirin. I nogle tilfælde observerede man endda en øget dødelighed. Årsagerne er komplekse, men flere teorier er blevet fremsat. En forklaring er, at den lave og variable biotilgængelighed af de orale midler førte til en utilstrækkelig og svingende hæmning af blodpladerne. En anden, mere bekymrende hypotese er, at disse lægemidler, ved delvist at binde til receptoren, paradoksalt nok kunne sende et aktiverende signal ind i blodpladen. Uanset årsagen blev udviklingen af orale GPIIb/IIIa-hæmmere stort set opgivet.
Ofte Stillede Spørgsmål
- Hvorfor er Integrin αIIbβ3 et så vigtigt mål for lægemidler?
- Det er vigtigt, fordi aktiveringen af denne receptor er det absolut sidste og nødvendige skridt for, at blodplader kan klumpe sig sammen (aggregere), uanset hvad der startede processen. Ved at blokere denne "fælles endelige vej" kan man opnå en meget kraftig og bredspektret hæmning af blodpladefunktionen.
- Hvad er den største risiko ved at bruge GPIIb/IIIa-hæmmere?
- På grund af deres potente virkning er den primære risiko blødning. Disse lægemidler forstyrrer en fundamental del af kroppens evne til at standse blødninger. Derfor anvendes de primært under kontrollerede hospitalsforhold, hvor patienterne kan overvåges nøje, og blødningsrisikoen kan håndteres.
- Hvorfor mislykkedes de orale GPIIb/IIIa-hæmmere, når de intravenøse var en succes?
- De intravenøse midler giver en høj, forudsigelig og vedvarende blokade af receptorerne, hvilket er nødvendigt for deres effekt i akutte situationer. De orale midler kæmpede med lav og uforudsigelig optagelse i kroppen, hvilket resulterede i en utilstrækkelig hæmning. Der er også tegn på, at en delvis blokade kan have uønskede, aktiverende effekter på blodpladerne.
Konklusion: En rejse mod præcisionsmedicin
Udviklingen af blodpladehæmmende lægemidler er et fremragende eksempel på, hvordan en dybere forståelse af grundlæggende biologiske mekanismer kan føre til livreddende behandlinger. Fra de tidlige, bredere virkende midler til de højt specialiserede lægemidler, der retter sig mod Integrin αIIbβ3, har forskningen transformeret behandlingen af arteriel trombose. Selvom vejen har haft sine bump, som de mislykkede orale midler, har succesen med de intravenøse GPIIb/IIIa-antagonister i akutte situationer reddet utallige liv. Effektiviteten af disse lægemidler i at reducere risikoen for de store kardiovaskulære dræbere er et glædeligt bidrag til moderne medicinsk praksis – og et bevis på, hvordan enorm fremgang kan komme fra at forstå meget små celler.
Hvis du vil læse andre artikler, der ligner Integrin αIIbβ3: Målet for blodpladehæmmere, kan du besøge kategorien Sundhed.