14/09/2024
Vores kroppe består af billioner af celler, der alle skal arbejde sammen for at holde os sunde. For at kroppen kan vokse eller erstatte døde celler, er det nødvendigt for vores celler at kunne dele sig. Denne proces med cellevækst og -deling skal dog være nøje kontrolleret, så cellerne ikke vokser uhæmmet og fortrænger de omkringliggende celler. Man kan tænke på en celle som en bil: Den har brug for en speeder til at sætte farten op (cellevækst), en bremse til at sænke farten (kontrollere væksten), og en mekaniker til at reparere eventuelle skader. Kontrollen med cellevækst styres normalt af specifikke gener inde i hver celle. Kræft opstår, når celler i kroppen bliver unormale og begynder at vokse ude af kontrol. Dette sker, når der opstår ændringer, eller mutationer, i de gener, der påvirker cellevæksten.
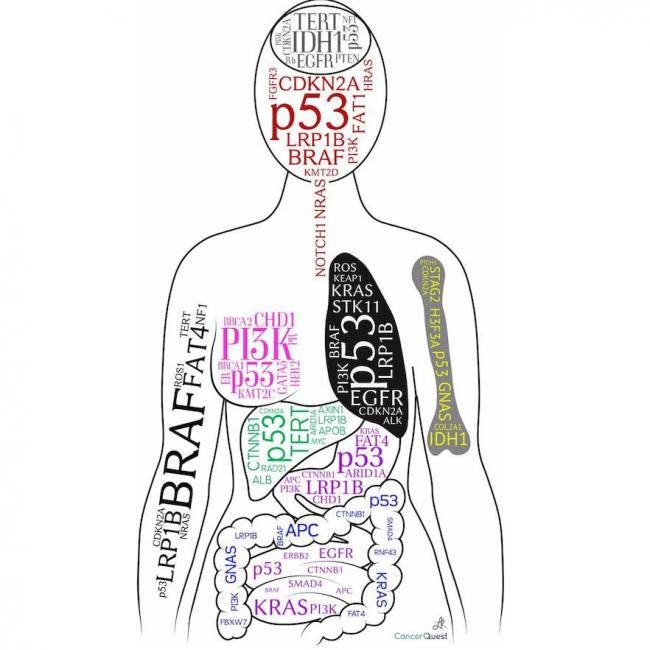
De primære typer af gener, der spiller en afgørende rolle i udviklingen af kræft, kan inddeles i tre hovedkategorier, som hver især har en unik funktion i cellens livscyklus.
- Onkogener: Fungerer som cellens 'speeder'.
- Tumorsuppressorgener: Fungerer som cellens 'bremse'.
- DNA-reparationsgener: Fungerer som cellens 'mekaniker'.
Kræft er ofte resultatet af en ophobning af ændringer i flere af disse gentyper inden for den samme celle, hvilket får den til at ignorere alle normale kontrolsignaler og dele sig ukontrolleret.
Onkogener: Den Fastlåste Speeder
Proto-onkogener er normale gener, der hjælper celler med at vokse, dele sig for at skabe nye celler, eller simpelthen overleve. De er afgørende for normal udvikling og vedligeholdelse af væv. Når et proto-onkogen muterer eller der opstår for mange kopier af det, kan det blive permanent aktiveret. I denne aktiverede tilstand kaldes det et onkogen. Et onkogener fungerer som en speeder, der sidder fast, hvilket får cellen til at dele sig konstant og ude af kontrol. Denne ukontrollerede vækst kan føre til dannelsen af en tumor og i sidste ende kræft.
Der er flere måder, hvorpå et proto-onkogen kan blive til et onkogen:
- Genmutationer: Nogle mennesker har variationer i deres genetiske kode, der kan forårsage, at et onkogen er konstant tændt. Disse genændringer kan være arvet fra en forælder eller opstå i løbet af en persons liv, for eksempel ved en fejl under DNA-kopiering ved celledeling.
- Epigenetiske ændringer: Celler har mekanismer til at tænde og slukke for gener uden at ændre selve DNA-sekvensen. Kemiske grupper kan blive tilføjet genetisk materiale (DNA eller RNA), hvilket påvirker, om et gen er aktivt. Sådanne epigenetiske ændringer kan undertiden føre til, at et onkogen bliver aktiveret.
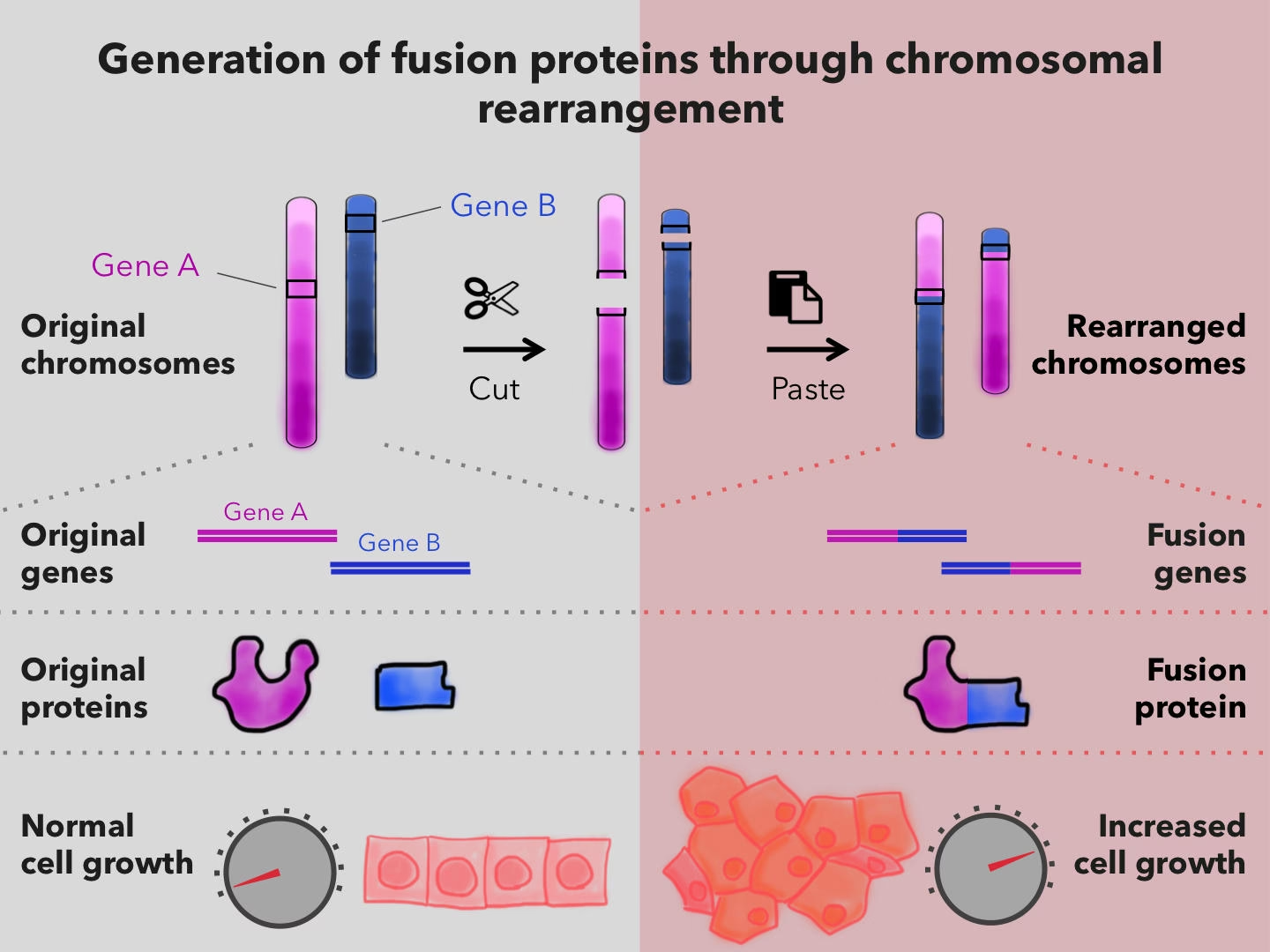
- Kromosomale omlejringer: Kromosomer er lange DNA-strenge, der indeholder vores gener. Nogle gange under celledeling kan DNA-sekvensen i et kromosom ændre sig. Dette kan placere et gen, der fungerer som en slags 'tænd'-kontakt, ved siden af et proto-onkogen, hvilket holder det tændt, selv når det ikke burde være det.
- Genduplikation: Nogle celler kan have ekstra kopier af et gen, hvilket kan føre til en overproduktion af et bestemt protein, der fremmer cellevækst.
Selvom et lille antal kræftsyndromer i familier er forbundet med en arvelig ændring i et onkogen, er de fleste ændringer, der involverer onkogener, erhvervet i løbet af en persons levetid og er derfor ikke arvelige.
Tumorsuppressorgener: De Defekte Bremser
Tumorsuppressorgener er normale gener, hvis funktion er at bremse celledeling, reparere DNA-fejl eller instruere celler i at dø på det rigtige tidspunkt (en proces kendt som apoptose eller programmeret celledød). De fungerer som bilens bremsepedal og sikrer, at cellevæksten forbliver under kontrol. Når tumorsuppressorgener ikke fungerer korrekt, for eksempel på grund af en mutation, mister cellen sin evne til at stoppe delingen. Dette kan føre til ukontrolleret cellevækst og dermed kræft.
Et vigtigt eksempel er TP53-genet, som koder for p53-proteinet. Dette protein spiller en central rolle i at kontrollere celledeling og kan udløse celledød, hvis DNA-skader er for alvorlige til at blive repareret. Arvelige ændringer i TP53-genet kan føre til Li-Fraumeni syndrom, hvor familiemedlemmer har en stærkt øget risiko for flere typer kræft, da alle deres celler bærer denne genfejl. Ændringer i TP53-genet er også ekstremt almindelige i kræftceller hos personer uden et arveligt syndrom. Disse er erhvervede mutationer, der kun findes i kræftcellerne og derfor ikke kan gives videre til børn.
DNA-reparationsgener: Den Fraværende Mekaniker
Når en celle deler sig, skal den lave en nøjagtig kopi af alt sit DNA. Dette er en utrolig kompleks proces, og fejl kan let opstå. Gener kendt som DNA-reparationsgener fungerer som en dygtig mekaniker, der konstant overvåger DNA'et for fejl og reparerer dem. Hvis skaden er for omfattende til at blive repareret, kan disse gener signalere til cellen, at den skal undergå programmeret celledød for at forhindre, at fejlene føres videre.
Når et af disse DNA-reparationsgener er defekt, kan fejl i DNA'et ophobes hurtigere. Nogle af disse nye mutationer kan ramme onkogener eller tumorsuppressorgener, hvilket skubber cellen endnu tættere på at blive en kræftcelle. Ligesom med andre gentyper kan ændringer i DNA-reparationsgener enten være arvelige eller erhvervede.
Kendte eksempler er BRCA1- og BRCA2-generne. Personer, der arver en mutation i et af disse gener, har en markant højere risiko for visse kræftformer, især bryst- og æggestokkræft hos kvinder. Men ændringer i disse gener ses også i tumorer hos personer, der ikke har arvet en mutation.

Arvelige Kræftsyndromer: Når Risikoen Går i Arv
Selvom de fleste kræfttilfælde skyldes tilfældige mutationer, der opstår i løbet af livet, er en vis andel (ca. 5-10%) forbundet med arvelige genmutationer. Disse mutationer øger en persons risiko for at udvikle kræft markant. Nedenfor er en oversigt over nogle af de kendte arvelige kræftsyndromer.
Oversigt over Vigtige Arvelige Syndromer
Her er en tabel, der sammenligner nogle af de mest kendte arvelige kræftsyndromer.
| Syndrom | Associeret Gen | Primære Kræftformer med Øget Risiko |
|---|---|---|
| Li-Fraumeni Syndrom | TP53 | Brystkræft, sarkomer, hjernetumorer, leukæmi, binyrebarkkræft |
| PTEN Hamartom Tumor Syndrom | PTEN | Brystkræft, skjoldbruskkirtelkræft, livmoderkræft, tarmkræft, nyrekræft, modermærkekræft |
| Familiær Adenomatøs Polypose (FAP) | APC | Tarmkræft (næsten 100% risiko uden behandling), mavekræft, bugspytkirtelkræft |
| MUTYH-Associeret Polypose (MAP) | MUTYH | Tarmkræft |
| Peutz-Jeghers Syndrom (PJS) | STK11 | Brystkræft, tarmkræft, bugspytkirtelkræft, mavekræft, æggestokkræft |
| Von Hippel-Lindau Sygdom (VHL) | VHL | Nyrekræft (renalcellet karcinom), neuroendokrine tumorer i bugspytkirtlen |
| Birt-Hogg-Dubé Syndrom (BHDS) | FLCN | Nyrekræft, potentielt tarmkræft |
| Multipel Endokrin Neoplasi (MEN) | MEN1, RET (for MEN2) | Tumorer i endokrine kirtler (bugspytkirtel, biskjoldbruskkirtel, hypofyse), medullær skjoldbruskkirtelkræft (MEN2) |
| Arvelig Bryst- og Ovariekræft | BRCA1, BRCA2, PALB2 | Brystkræft, æggestokkræft, bugspytkirtelkræft, prostatakræft |
| Arveligt Retinoblastom | RB1 | Retinoblastom (en sjælden øjenkræft hos børn) |
Detaljeret Gennemgang af Syndromer
Li-Fraumeni Syndrom (LFS)
Forårsaget af en mutation i TP53-genet, som er en central 'vogter' af genomet. Personer med LFS har en meget høj livstidsrisiko for at udvikle en række kræftformer, ofte i en ung alder.
Familiær Adenomatøs Polypose (FAP)
Skyldes en mutation i APC-genet. Dette fører til udviklingen af hundredvis eller tusindvis af polypper i tyktarmen. Uden behandling vil næsten alle med klassisk FAP udvikle tarmkræft, typisk før 45-årsalderen.
PALB2-genet
Fejl i PALB2-genet øger risikoen for bryst-, bugspytkirtel- og æggestokkræft. Næsten 45 ud af 100 kvinder med en defekt i PALB2-genet vil udvikle brystkræft inden 80-årsalderen.
CHEK2-genet
CHEK2 er et DNA-reparationsgen. En mutation heri giver en 25-30% livstidsrisiko for brystkræft og øger også risikoen for prostata-, nyre-, skjoldbruskkirtel- og tyktarmskræft.
Ofte Stillede Spørgsmål (FAQ)
Er al kræft arvelig?
Nej, langt de fleste kræfttilfælde (over 90%) er sporadiske, hvilket betyder, at de skyldes genmutationer, der er erhvervet i løbet af en persons liv på grund af faktorer som aldring, livsstil eller miljøpåvirkninger. Kun en mindre del skyldes en arvelig genfejl, der øger risikoen.
Hvad er forskellen på et proto-onkogen og et onkogen?
Et proto-onkogen er et normalt, sundt gen, der hjælper med at regulere cellevækst og -deling – som en bils speeder, der fungerer korrekt. Et onkogen er en muteret version af et proto-onkogen, der er permanent 'tændt' – som en speeder, der sidder fast og får bilen til at køre ukontrolleret.
Kan jeg blive testet for arvelige kræftgener?
Ja, genetisk testning er tilgængelig for mange af de kendte kræftsyndromer. Det anbefales typisk, hvis der er en stærk familiehistorie med bestemte kræftformer, kræft i en ung alder eller flere tilfælde af kræft hos den samme person. Det er vigtigt at drøfte muligheden med en læge eller en genetisk rådgiver for at forstå fordele og ulemper ved en test.
Hvis du vil læse andre artikler, der ligner Genernes Rolle i Kræftudvikling, kan du besøge kategorien Sundhed.